Resumen
El concepto de cascada vascular (VW) describe un mecanismo clave de la autorregulación del flujo sanguíneo, que vincula la presión crítica de cierre arterial (Pcrit) con la presión media de llenado sistémico (Pmsf). Este gradiente de presión define la presión de perfusión tisular (Pa − Pcrit) y proporciona un marco para interpretar la dinámica circulatoria y la autorregulación del flujo sanguíneo en la salud y la enfermedad. Esta revisión explora el desarrollo histórico, los fundamentos fisiológicos, las implicaciones clínicas y las futuras direcciones del modelo AV en cuidados intensivos.
Originario del modelo de resistencia de Starling, el VW surge cuando la presión circundante, ya sea por el tono vasomotor o las fuerzas intersticiales, supera la presión arterial intraluminal, definiendo una Pcrit, lo que provoca que el flujo se vuelva independiente de la presión distal.
En estas condiciones, la Pcrit funciona como la contrapresión efectiva. El lecho capilar, altamente distensible, se adapta a bajas presiones de entrada, a menudo de 5 a 10 mmHg por encima de la Pmsf. Las técnicas a pie de cama, como las maniobras de pausa inspiratoria, permiten estimar la Pcrit y la Pmsf como parámetros circulatorios globales.
En la vasoplejía, como la sepsis, la disminución del tono vascular reduce la Pcrit, a menudo aproximándose a la Pmsf, lo que anula la VW y altera la autorregulación. Los vasopresores solo pueden restablecer la perfusión si la Pcrit aumenta más que la Pmsf. De manera similar, en la circulación pulmonar, la fisiología de la VW ayuda a explicar cómo las presiones alveolares y pleurales elevadas durante la ventilación mecánica, particularmente con PEEP alta, afectan el retorno venoso y la carga del ventrículo derecho, con implicaciones para el manejo del SDRA.
De cara al futuro, la medición no invasiva de la Pcrit, su integración con la monitorización hemodinámica continua y el modelado predictivo podrían permitir una terapia guiada por la VW en tiempo real. Al conectar la fisiología macro y microcirculatoria, el concepto de VW ofrece una base prometedora para intervenciones hemodinámicas de precisión en pacientes críticos.
Introducción
El sistema circulatorio suministra sangre oxigenada a los tejidos, eliminando el dióxido de carbono y los desechos, un proceso regido por complejos mecanismos reguladores a nivel global, regional y local.
La regulación global se refiere a determinantes sistémicos como la presión arterial media (PAM), la presión auricular derecha (PAD) y el gasto cardíaco (GC), que definen la presión y el flujo de perfusión generales. La regulación regional actúa a nivel de territorios vasculares específicos, como los lechos cerebral, renal o esplácnico, donde la vasoconstricción o vasodilatación selectiva redistribuye el flujo sanguíneo según las prioridades de los órganos durante el estrés. La regulación local se produce en la microcirculación, donde mecanismos como la autorregulación metabólica y las presiones de cierre controlan el reclutamiento capilar y la perfusión específica de los tejidos, definiendo el consumo de oxígeno de todo el organismo. En conjunto, estos niveles reguladores ajustan dinámicamente el flujo sanguíneo para satisfacer las demandas metabólicas, pero también introducen no linealidades que ponen en entredicho los modelos lineales simples de perfusión tisular, especialmente en la microvasculatura.
Clásicamente, la perfusión tisular se describía como un modelo hidráulico lineal, donde el flujo sanguíneo (Q) se determina por el gradiente de presión entre la presión arterial media (PAM) y la presión venosa central (PVC), dividido por la resistencia vascular sistémica (RVS), de forma similar a la ley de Ohm (Q = ΔP/R). Con el tiempo, se hizo evidente que este enfoque lineal pasaba por alto factores no lineales como el tono vasomotor variable, la distensibilidad vascular, el colapso vascular y las fuerzas compresivas externas. Si bien el modelo lineal asumía una resistencia constante, en realidad, prácticamente no existe resistencia medible en los grandes vasos arteriales, y la mayor parte de la resistencia arterial, definida como una disminución de la presión arterial intraluminal con la distancia, se produce en las arterias y arteriolas pequeñas a lo largo de distancias muy cortas. Por lo tanto, se necesitaba un marco más refinado para explicar con mayor precisión fenómenos como la autorregulación y los estados de shock.
En este contexto, el presente trabajo es una revisión narrativa del concepto de cascada vascular, con especial atención a sus aplicaciones clínicas en la unidad de cuidados intensivos (UCI). En este trabajo, describimos sus fundamentos mecanicistas, sus implicaciones clínicas y sus limitaciones, con el objetivo de avanzar en la comprensión fisiológica y proporcionar un marco para futuras investigaciones.
Fundamentos conceptuales
Historia y mecanismos fundamentales del concepto de cascada vascular.
Durante el último siglo, se ha prestado considerable atención a la relación entre el flujo sanguíneo y las diferencias de presión en los sistemas arterial y venoso (Tabla 1). En 1914, Starling desarrolló un modelo de corazón aislado perfundido para investigar la función del ventrículo izquierdo. Observó que cuando el circuito de salida drenaba directamente en un reservorio, la presión diastólica caía a cero y el corazón fallaba. Para mantener el flujo coronario, encerró la aorta descendente en una cámara de presión externa antes de que drenara en un reservorio venoso. Notó que el segmento de salida colapsable se ubicaba en el extremo de la cámara y que la presión diastólica se aproximaba a la presión de la cámara. Estos segmentos colapsables se denominaron posteriormente resistencias de Starling.
El colapso vascular puede ocurrir debido a la presión tisular externa, como en los síndromes compartimentales, o cuando el tono vasomotor arterial supera la presión intraarterial. En 1951, Burton definió este umbral limitante del flujo como la «presión crítica de cierre» (Pcrit), por debajo de la cual un vaso colapsa y el flujo sanguíneo cesa transitoriamente, incluso si se mantiene un gradiente de presión de entrada-salida (Fig. 1A). A medida que la presión intraluminal disminuye debido a la pérdida de energía inducida por el flujo, el segmento colapsable se cierra parcial o totalmente, de modo que el flujo pasa a estar regido por el gradiente entre la presión de entrada y Pcrit, en lugar de por la presión aguas abajo. Una vez que el flujo se detiene, la presión intraluminal rebota hacia el valor aguas arriba, lo que permite una breve reanudación del flujo, solo para detenerse de nuevo. Este comportamiento intermitente demuestra que Pcrit funciona como la contrapresión efectiva, ya que las presiones aguas abajo por debajo de ella no tienen efecto. Permutt y Riley formalizaron posteriormente este principio como «cascada vascular», utilizando la analogía de que, al igual que el agua que fluye por un acantilado depende solo de la altura aguas arriba y del borde de la caída, el flujo sanguíneo más allá de un segmento vascular colapsado depende únicamente de la presión de entrada en relación con Pcrit, no de la presión del vaso aguas abajo.
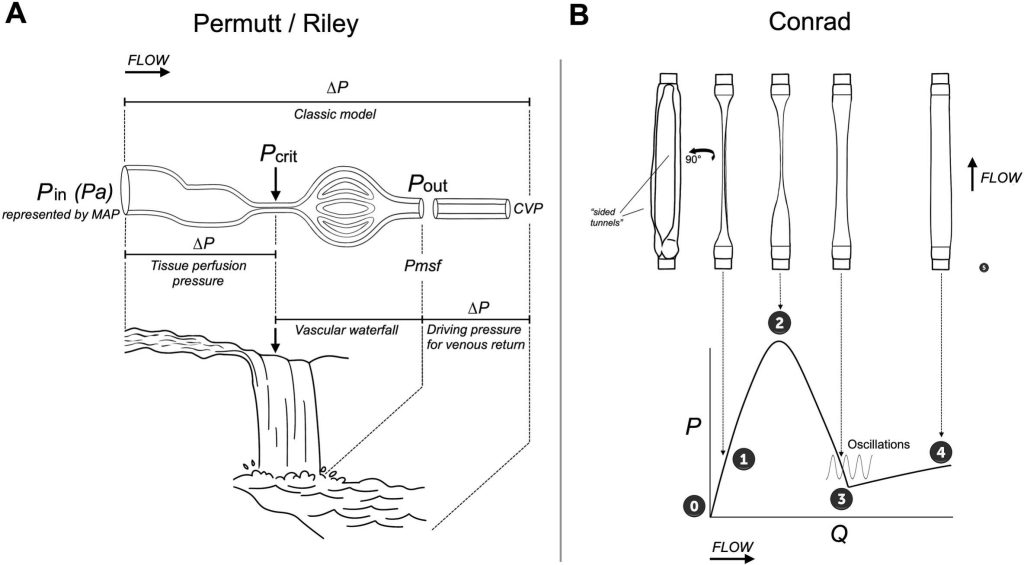
En conjunto, estos modelos explican el comportamiento del flujo sanguíneo en vasos colapsables bajo el concepto de cascada vascular, donde el flujo persiste a pesar de que la presión externa supere la presión aguas abajo, debido a:
Flujo intermitente: Cuando el flujo se detiene, la presión intraluminal regresa a la presión aguas arriba (Pin) y el flujo se reanuda, solo para cesar nuevamente de inmediato, lo que sugiere que Pcrit funciona como la contrapresión efectiva para el flujo.
Cambio en la contrapresión: La presión externa (p. ej., presión alveolar o Pcrit) se convierte en la presión aguas abajo limitante.
Flujo impulsado aguas arriba: Regido por el gradiente entre la presión aguas arriba (p. ej., presión arterial) y Pcrit, en lugar de la presión venosa.
Independencia aguas abajo: La presión aguas abajo por debajo de Pcrit no influye en el flujo, de forma similar al agua sobre una presa.
Permeabilidad del vaso: El flujo puede persistir a través de segmentos estrechos o túneles laterales si la presión aguas arriba supera Pcrit.
Pin: Presión aguas arriba; Pa: Presión arterial; MAP: Presión arterial media; Pcrit: Presión crítica de cierre; Pv: Presión venosa; Pout presión intravesical descendente; Pmsf presión media de llenado sistémico; CVP presión venosa central.
La circulación pulmonar es el paradigma de la fisiología de la cascada. En 1964, West describió cómo las presiones alveolar y pleural redefinen la presión efectiva aguas abajo, creando zonas donde el flujo pulmonar se independiza intermitentemente de la presión venosa. En la Zona 1, la presión arterial pulmonar cae por debajo de la presión alveolar (PA) y el flujo cesa. En la Zona 2, el flujo depende únicamente del gradiente entre la presión arterial pulmonar y la PA, independientemente de la presión venosa pulmonar, característica distintiva de la cascada vascular pulmonar. En la Zona 3, tanto la presión arterial como la venosa superan la PA, y el flujo depende de la diferencia de presión entre la arteria y la vena.
En términos circulatorios, la presión aguas arriba corresponde a la presión arterial (Pa), que se representa operacionalmente mediante la presión arterial media (PAM). La presión de salida corresponde a la Pcrit, la presión media de llenado sistémico (Pmsf) o la presión venosa (Pv), según cuál sea mayor. Dado que en condiciones normales Pmsf − Pv define el gradiente de presión para el retorno venoso, si la congestión venosa provoca un aumento de Pv, impedirá inmediatamente dicho retorno. La disociación del flujo sanguíneo de Pv permite que la modulación regional del flujo esté impulsada únicamente por las presiones aguas arriba y las fuerzas compresivas externas, que pueden alterar el tono vasomotor local de forma inversa a su demanda metabólica. A medida que aumenta la demanda metabólica local, los tejidos disminuyen retrógradamente el tono vasomotor de sus arteriolas aferentes, reduciendo así su Pcrit local e incrementando el flujo.
Las discrepancias entre las presiones arteriales centrales y periféricas ilustran cómo los territorios vasculares paralelos pueden generar cascadas distintas. En estados de vasoconstricción periférica intensa (choque hipovolémico o cardiogénico), las arterias musculares distales (p. ej., radial) se contraen con mayor intensidad que las arterias centrales (p. ej., femoral). Por consiguiente, su Pcrit local aumenta de forma desproporcionada, disminuyendo las presiones distales mientras que las presiones centrales permanecen elevadas. Esto produce un gradiente femoral-radial medible, no por una caída secuencial a lo largo de un vaso, sino por segmentos arteriales paralelos regidos por diferentes presiones de cierre. La hipotermia, junto con otras formas de insuficiencia circulatoria, también se asocia con discrepancias de presión paradójicas impulsadas por el mismo mecanismo. Estos escenarios ilustran cómo la fisiología de la cascada vascular explica la heterogeneidad de la perfusión regional y las distribuciones de presión inesperadas en estados de bajo flujo.
Sin embargo, las propiedades de limitación del flujo de los segmentos vasculares bajo colapso parcial también dependen del comportamiento no lineal, lo que requiere un análisis biofísico más detallado. Los experimentos de Conrad con tubos colapsables de paredes delgadas en entornos presurizados demostraron que el flujo sigue regímenes distintos en lugar de una relación lineal. Los segmentos completamente abiertos y completamente cerrados obedecen la ley de Poiseuille, pero los tubos parcialmente colapsados muestran resistencia negativa, donde la resistencia disminuye a medida que aumenta el flujo. Esto ocurre porque el diámetro del vaso se ensancha desde las regiones colapsadas hacia las abiertas, reduciendo la resistencia y preservando la perfusión en lechos marginalmente perfundidos, como se observa habitualmente en la circulación pulmonar, donde el aumento de la presión arterial disminuye la resistencia vascular mediante la distensión inducida por la presión. Incluso con una presión transmural cercana a cero, puede persistir un paso residual a través de «túneles laterales» en forma de hendidura (Fig. 1B). Cuando la presión intraluminal cae por debajo de la presión circundante, el vaso colapsa y el flujo se aproxima a cero. A medida que aumenta el flujo, la resistencia disminuye paradójicamente al reabrirse el tubo, creando un segmento de resistencia negativa. Con flujos más altos, puede producirse un aleteo oscilatorio debido a las interacciones entre la inercia del fluido y la elasticidad de la pared del vaso, similar a las vibraciones autoexcitadas de una manguera presurizada. A medida que el tubo se reexpande, se restablece el flujo laminar y la resistencia vuelve a aumentar proporcionalmente al flujo. Estas propiedades biomecánicas divergen de las predicciones hidráulicas lineales.
Aunque Conrad no se propuso describir una cascada vascular, sus hallazgos proporcionan un complemento mecánico al modelo fisiológico de Permutt y Riley. En conjunto, demuestran que los vasos colapsables presentan un comportamiento no lineal, caracterizado por oscilaciones, resistencia negativa y permeabilidad residual, lo que perfecciona la base mecanicista de la limitación del flujo bajo compresión externa. Este comportamiento, similar al movimiento peristáltico, puede impulsar la sangre transitoriamente. Estos hallazgos cuestionan la visión clásica de la resistencia vascular sistémica (RVS), y en su lugar respaldan la existencia de resistencias arteriales y venosas distintas, cuya suma se reduce cuando existe una cascada vascular. También ayudan a explicar cómo se mantiene el retorno venoso bajo presiones extravasculares elevadas y cómo se redistribuye la perfusión en estados dinámicos, como el choque séptico.
Correlatos fisiológicos y estimación de Pcrit y Pmsf
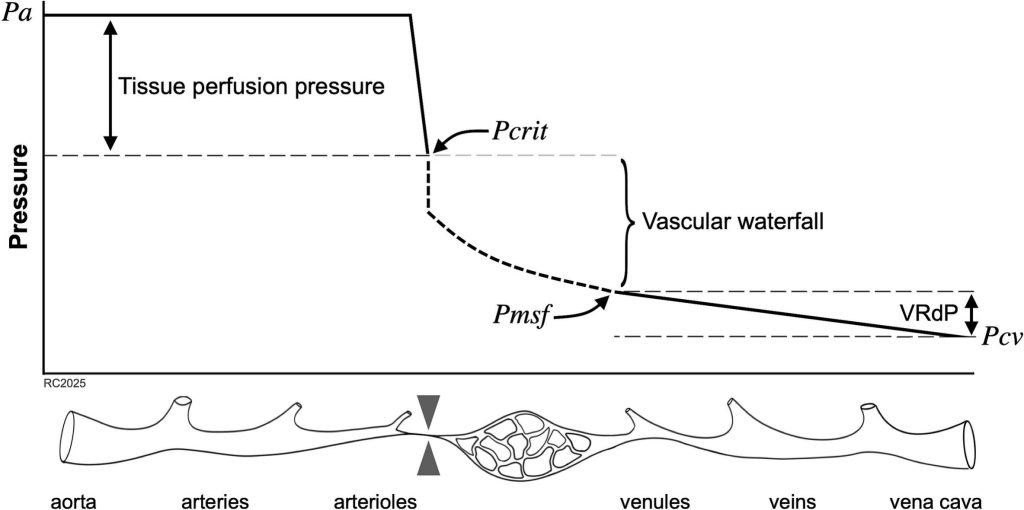
Los lechos capilares actúan como reservorios de baja resistencia y alta distensibilidad que permiten el reclutamiento y la distensión en respuesta al aumento de la presión de perfusión, especialmente durante el ejercicio o la activación simpática. Esta distensibilidad genera una marcada heterogeneidad regional en las presiones capilares y de cierre crítico, lo que refleja diferencias en el tono vascular local y la demanda metabólica. Por ejemplo, las presiones capilares pueden alcanzar 18-25 mmHg durante el flujo máximo del músculo esquelético cuando los vasos de resistencia están completamente dilatados. Debido a esta heterogeneidad espacial, la medición directa de la presión de cierre crítico (Pcrit) o de la presión de cascada vascular no es factible in vivo. Sin embargo, en condiciones de estado estacionario, los territorios vasculares tienden a converger hacia una presión de equilibrio común (Pmsf), que actúa como la presión efectiva aguas arriba para el retorno venoso y permanece relativamente estable debido a la distensibilidad de la red capilar.
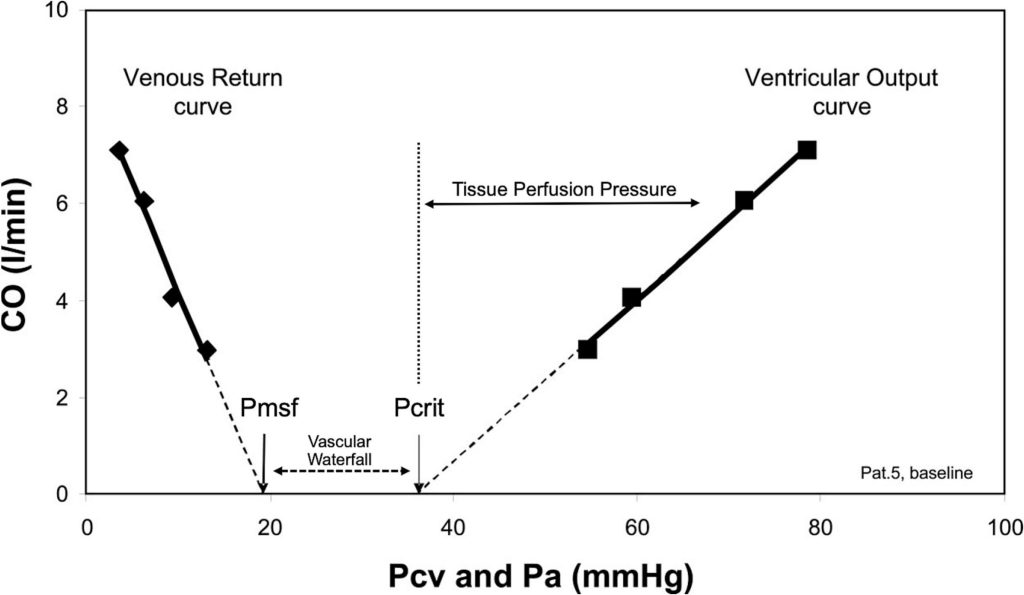
A pesar de estas limitaciones, la Pcrit y la Pmsf pueden estimarse indirectamente mediante el análisis de las relaciones presión-flujo obtenidas durante perturbaciones hemodinámicas transitorias. En la cabecera del paciente, las curvas de retorno venoso generadas durante las maniobras de pausa inspiratoria permiten extrapolar la intersección de flujo cero como un sustituto de Pmsf, mientras que la representación gráfica de la presión arterial media frente al gasto cardíaco permite estimar Pcrit como la presión arterial a la que cesa el flujo. El gradiente de presión entre Pcrit y Pmsf define la cascada vascular funcional y proporciona una partición mecanicista de la presión de perfusión tisular más allá de la MAP sola (Fig. 2, Fig. 3). Aunque estas estimaciones se basan en supuestos de linealidad, tono vascular estable y condiciones casi estacionarias, han permitido la comprobación fisiológica del concepto de cascada vascular y su modulación mediante intervenciones como los vasopresores.
Aplicaciones clínicas del marco de la cascada vascular
La aplicación de la fisiología de la cascada vascular a la práctica clínica requiere una atención minuciosa a los determinantes del flujo local y su redistribución en los territorios vasculares. Esto es fundamental en el shock, donde la Pcrit suele estar reducida. En la práctica clínica, muchas intervenciones afectan la PAM a la vez que modifican la Pcrit o la Pmsf; por lo tanto, las decisiones terapéuticas deben centrarse en restaurar y mantener la integridad de la cascada vascular (Pcrit − Pmsf) mientras se mantiene una PAM lo suficientemente alta como para ampliar o mantener la TPP y asegurar el flujo sobre la cascada vascular. La comprensión de estos gradientes subraya que la fisiología de la cascada vascular no es meramente teórica, sino esencial para el razonamiento clínico. La autorregulación proporciona la demostración más clara de este principio: es el mecanismo esencial mediante el cual una cascada vascular funcional protege la perfusión tisular y explica por qué las alteraciones de la Pcrit o la Pmsf conllevan consecuencias clínicas tan profundas.
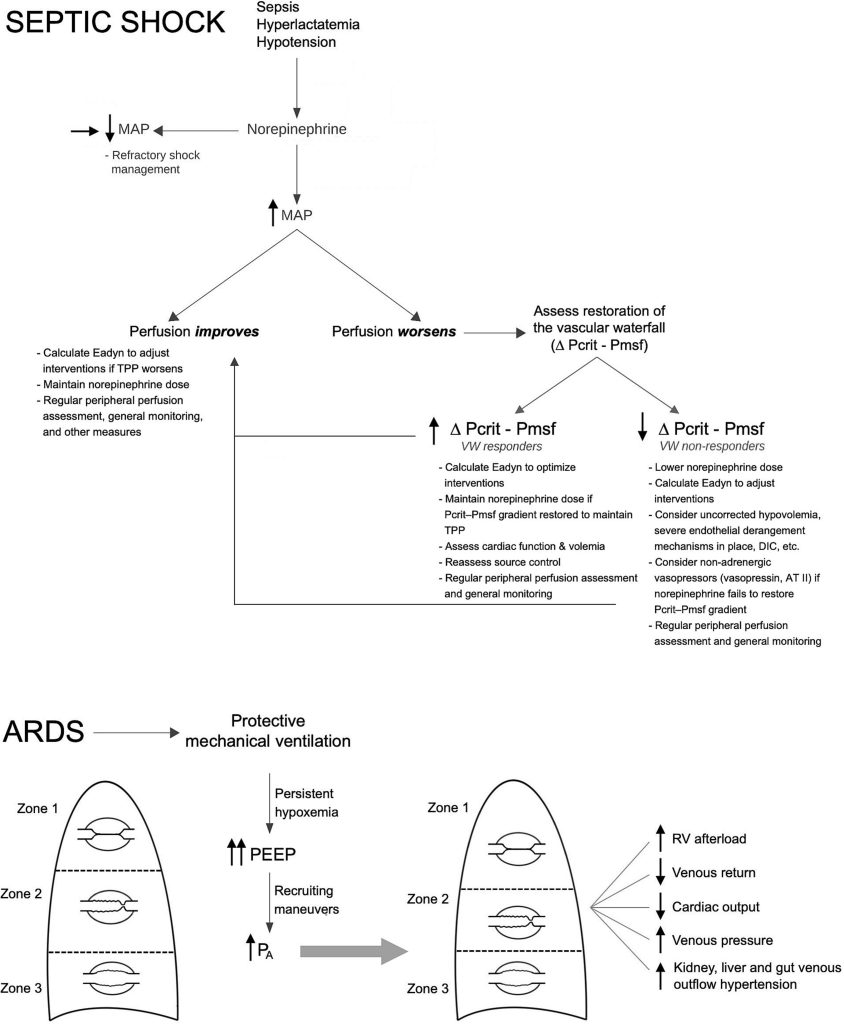
Panel superior: Choque séptico. La norepinefrina aumenta la presión arterial media (PAM), pero su efecto sobre la perfusión tisular depende de si la presión de perfusión tisular (PPT = PAM−Pcrit) se amplía de tal manera que el aumento de Pcrit sea mayor que la presión media de perfusión tisular (Pmsf). Si Pcrit aumenta, restableciendo el gradiente de cascada vascular (pacientes que responden a la cascada vascular), la perfusión mejora y se puede mantener la norepinefrina guiándose por la elastancia arterial dinámica (Eadyn). Cuando la PPT aumenta selectivamente al incrementar la PAM y no la Pcrit (pacientes que responden a la cascada vascular), la perfusión empeora a pesar de una PAM más alta, lo que requiere una reevaluación del estado de volumen, la función cardíaca, la integridad endotelial y la posible necesidad de vasopresores alternativos.
Panel inferior: SDRA. La ventilación mecánica protectora con presión positiva al final de la espiración (PEEP) modifica las zonas de West. La presurización alveolar excesiva puede desplazar la Zona 2 a la Zona 1, provocando la interrupción del flujo y el riesgo de colapso cardiovascular. Las maniobras de reclutamiento y los altos niveles de PEEP aumentan aún más la PA, lo que perjudica el retorno venoso, incrementa la poscarga del ventrículo derecho (VD), eleva las presiones venosas y conduce a hipertensión en el riñón, el hígado y el drenaje venoso intestinal. Estas interacciones resaltan la importancia de lograr un equilibrio entre la oxigenación y el compromiso hemodinámico.
Esta figura no presenta un algoritmo integral para el manejo del shock; su único propósito es ilustrar cómo la TPP puede integrarse en el pensamiento de reanimación. Dado que varios de estos mecanismos no se han demostrado formalmente, el contenido debe considerarse como una especulación fundamentada.
Abreviaturas: MAP, presión arterial media; Pcrit, presión crítica de cierre; Pmsf, presión media de llenado sistémico; TPP, presión de perfusión tisular; VW, cascada vascular; PEEP, presión positiva al final de la espiración; PA, presión alveolar; VD, ventrículo derecho; Eadyn, elastancia arterial dinámica. SDRA, síndrome de dificultad respiratoria aguda; CID, coagulación intravascular diseminada.
Autorregulación
La autorregulación representa la expresión de la fisiología de la cascada vascular a nivel tisular, demostrando cómo se preserva la perfusión local en un rango de presiones arteriales mediante ajustes dinámicos en el tono vasomotor, previniendo cambios no metabólicos en el flujo. Con el aumento de la demanda metabólica, el tono vasomotor disminuye y el flujo aumenta proporcionalmente. Sin embargo, una autorregulación eficaz requiere un gradiente de presión adecuado, de modo que la PaO₂ debe estar por encima de un cierto valor mínimo para que la Pcrit pueda mantener la presión de perfusión, y la Pcrit debe permanecer por encima de la Pmsf.
La autorregulación falla cuando la PaO₂ se aproxima a la Pcrit, cayendo por debajo del límite inferior de autorregulación del tejido. Por encima de ese punto, la cascada vascular (Pcrit − Pmsf) estabiliza la presión de salida efectiva, mientras que el control barorreflejo mantiene la presión de entrada (PaO₂ − Pcrit) (Fig. 1A). Esta doble estabilización hace que la cascada vascular sea independiente de la PaO₂ y de la variabilidad del flujo, mejorando la precisión y la adaptabilidad de la regulación local del flujo. Si bien las respuestas autorregulatorias locales pueden iniciarse de forma autónoma, su mantenimiento depende de un gradiente sostenido de Pa − Pcrit. La heterogeneidad regional de Pcrit y la resistencia vascular contribuyen aún más a la redistribución del flujo sanguíneo en respuesta a los cambios en Pa. Estas interacciones establecen un sistema de retroalimentación dinámico, mediante el cual la autorregulación modula el tono vasomotor, lo que altera Pcrit e influye en el gradiente de Pa − Pcrit. Los estados patológicos, como la sepsis o el uso de vasopresores, pueden influir aún más en esta redistribución y desacoplar los bucles reguladores simpáticos locales.
La cascada vascular en estado de shock
Cuando falla la autorregulación, las consecuencias sistémicas de la alteración de la cascada vascular se hacen evidentes, especialmente en el shock.
Los estados de bajo gasto cardíaco, como la hipovolemia profunda, la obstrucción vascular o la insuficiencia cardíaca, se caracterizan por una intensa vasoconstricción, un tono vasomotor elevado y una Pcrit alta. En estas condiciones, el flujo arterial puede cesar durante la diástole debido a la reducción crítica del gradiente Pa-Pcrit, pero el flujo anterógrado sigue siendo insuficiente debido a la disminución del gasto cardíaco. En contraste, el shock vasopléjico se caracteriza por una disminución profunda del tono vascular, a menudo con una respuesta deficiente a los estímulos α-adrenérgicos. En pacientes reanimados con fluidos, el gasto cardíaco puede conservarse o incluso elevarse, pero tanto la Pa como la Pcrit son anormalmente bajas y la Pcrit se aproxima a la Pmsf, lo que anula la cascada vascular; la hipotensión y la alteración de la autorregulación se presentan a pesar de un flujo global aparentemente adecuado.
La norepinefrina solo puede mejorar la perfusión cuando eleva la Pcrit por encima de la Pmsf, restableciendo así la cascada vascular, mientras que la PAM aumenta lo suficiente por encima de la nueva Pcrit. Los pacientes en quienes la Pcrit aumentó (típicamente hacia ∼40 mmHg) mostraron una restauración de la perfusión periférica; aquellos en quienes la Pcrit se mantuvo cerca de la Pmsf (∼20 mmHg) no la mostraron, incluso si la MAP aumentó por encima de 70 mmHg. Por lo tanto, en la vasoplejía, el objetivo clínicamente relevante es el restablecimiento de un gradiente Pcrit-Pmsf efectivo, junto con una MAP que supere la Pcrit para proporcionar una presión de perfusión adecuada. La respuesta hemodinámica a la norepinefrina, por consiguiente, depende primero de restaurar Pcrit > Pmsf y luego asegurar que MAP > Pcrit. Así, una vez restaurada la cascada, la TPP puede utilizarse para cuantificar la presión impulsora de la perfusión tisular efectiva.
Los efectos de la norepinefrina sobre la MAP y la Pcrit son desiguales. En algunos pacientes, tanto la MAP como la Pcrit aumentan, y la Pcrit se eleva lo suficiente por encima de la Pmsf para restaurar el gradiente Pcrit-Pmsf. Esto restablece la cascada vascular, restaura los umbrales autorregulatorios y mejora la perfusión tisular, como se observa en algunos estudios; esto es consistente con el fenotipo de «respondedor de cascada» descrito por Andrei y colegas. Sin embargo, en otros, la Pcrit permanece baja y cercana a la Pmsf a pesar del aumento de la MAP, por lo que la cascada vascular no se restablece y la perfusión periférica permanece deteriorada. Esto explica por qué algunos pacientes en choque séptico muestran alteraciones microcirculatorias persistentes a pesar de los aumentos de la MAP inducidos por la norepinefrina. Esto representa un mecanismo distinto de los estados de bajo flujo con respuesta adrenérgica intacta, en los que la Pcrit se eleva por encima de la presión diastólica y la limitación principal es el CO en lugar de la ausencia de una cascada vascular.
La restauración del gradiente MAP-Pcrit con norepinefrina se ha asociado con una mejoría en los marcadores e indicadores indirectos de perfusión tisular, incluyendo CO, tiempo de llenado capilar, brecha de pCO₂ y lactato. Al aumentar el tono vascular y elevar Pcrit, la norepinefrina restablece el gradiente Pa-Pcrit y aumenta la TPP efectiva. Evidencia reciente refuerza la relevancia clínica de este concepto: en una gran cohorte de pacientes sometidos a cirugía cardíaca, Miles et al. demostraron que una TPP más baja se asoció de forma independiente con una mayor incidencia de IRA, independientemente de los niveles de MAP. Por consiguiente, la efectividad de la norepinefrina debe evaluarse determinando si Pcrit aumenta lo suficiente por encima de Pmsf para restaurar la cascada vascular, y si MAP supera esta nueva Pcrit para generar una TPP adecuada. El fracaso de cualquiera de estas condiciones predice anomalías microcirculatorias persistentes a pesar de los aumentos aparentes en MAP. En este sentido, la mejoría observada con una TPP más alta en algunos estudios probablemente refleja un aumento concomitante de la Pcrit, ya que una MAP elevada sin el restablecimiento del gradiente Pcrit-Pmsf probablemente no se traduce en una perfusión efectiva.
Por lo tanto, evaluar la efectividad de la norepinefrina requiere medir tanto la MAP como marcadores indirectos que reflejen cambios en el tono vascular y anticipen las respuestas hemodinámicas a la terapia vasopresora. Eadyn se ha consolidado como un marcador indirecto del tono arterial y la integridad de la cascada vascular al monitorizar los cambios en el gradiente Pcrit-Pmsf y predecir la respuesta de la MAP a la norepinefrina. Esto convierte a Eadyn en una valiosa herramienta clínica para identificar a los pacientes en quienes la terapia vasopresora restaurará eficazmente la cascada vascular. Sin embargo, en la vasoplejía relacionada con la sepsis, la estimulación α-adrenérgica excesiva puede afectar la redistribución del flujo sanguíneo y empeorar la isquemia si se ajusta sin considerar las consecuencias microcirculatorias.
Más allá de la norepinefrina, el modelo de cascada vascular también podría explicar los efectos diferenciales de los vasopresores no catecolamínicos. La vasopresina, mediante la vasoconstricción mediada por V1, puede elevar la PAM con un impacto diferencial en la Pcrit en algunos lechos vasculares, lo que podría explicar, al menos en parte, las señales de protección renal observadas en los ensayos VANISH, VANCS y OVISS. La angiotensina II, a través de los receptores AT1, probablemente eleva tanto la PAM como la Pcrit, con una distribución que favorece las circulaciones esplácnica y eferente renal. Estas consideraciones siguen siendo especulativas, ya que ningún estudio ha examinado directamente cómo los vasopresores no catecolamínicos modulan la Pcrit o los gradientes Pa-Pcrit. Por lo tanto, los enfoques basados en la cascada vascular proporcionan un marco fisiológico que complementa la monitorización convencional, guiando la reanimación con mayor precisión que los índices globales como la RVS. Esto podría ayudar a conciliar los parámetros macrocirculatorios (Pa y CO) con los objetivos microcirculatorios, especialmente cuando se altera la coherencia hemodinámica.
Cascada vascular en la ventilación mecánica
Como se describió anteriormente, las zonas de West ilustran cómo las presiones alveolar y pleural redefinen la presión efectiva aguas abajo, con la PA actuando como presión de cierre en la Zona 2. Esta disposición también confiere una capacidad amortiguadora: cuando cesa el flujo, la presión arterial pulmonar puede aumentar intermitentemente por encima de la presión alveolar, reabrir los vasos y mantener el flujo anterógrado. La presurización alveolar excesiva, como durante una PEEP alta, anula esta reapertura y desplaza la Zona 2 hacia la Zona 1, lo que resulta en el cese completo del flujo. La ventilación con presión positiva modifica aún más estas relaciones en el SDRA, donde la distensibilidad alterada y las presiones intratorácicas elevadas influyen notablemente en la fisiología vascular pulmonar y sistémica.
En estados de baja distensibilidad, como el SDRA, la PEEP eleva la PA por encima de la presión venosa pulmonar (Ppv), generando extensas regiones de la Zona 2. Simultáneamente, la presión pleural (Ppl) puede superar la Pmsf, creando impedimentos vasculares similares a una cascada para el retorno venoso sistémico a medida que las venas torácicas colapsan. La elevación de la presión arterial pulmonar (PA) y la presión transpulmonar (PA − Ppl) pueden provocar un mayor colapso de los vasos alveolares, aumentar la resistencia vascular pulmonar y, si el flujo persiste, elevar la presión arterial pulmonar (Ppa), incrementando la poscarga del ventrículo derecho (VD) y favoreciendo su disfunción.
Por lo tanto, la titulación de la PEEP requiere un equilibrio preciso. Al aumentar el volumen pulmonar y la presión intratorácica, la PEEP estabiliza los alvéolos y mejora la oxigenación, pero simultáneamente eleva las presiones distales para el retorno venoso y el drenaje de los órganos. Cabe destacar que, incluso con estrategias de ventilación protectora, estos efectos hemodinámicos persisten. Niveles más altos de PEEP comprometen la perfusión esplácnica, hepática y renal mediante efectos combinados sobre la reducción del CO₂, la vasoconstricción refleja y el aumento de las presiones venosas. Además, las maniobras de reclutamiento o la sobredistensión alveolar pueden expandir aún más las zonas 1 y 2, empeorando el desequilibrio ventilación-perfusión. Esta redistribución reduce la perfusión pulmonar, aumenta el espacio muerto fisiológico y eleva la poscarga del VD. Cuando la PA aumenta bruscamente durante el reclutamiento, la capacidad de amortiguación de la cascada vascular pulmonar puede verse superada, lo que provoca reducciones drásticas del retorno venoso y riesgo de colapso cardiovascular. Cabe destacar que la relación entre la PEEP, la resistencia vascular pulmonar y la función del ventrículo derecho no es lineal: tanto la sobredistensión como el colapso alveolar pueden empeorar la carga del ventrículo derecho. La Ppl modula además el impacto hemodinámico de las maniobras de reclutamiento. Curiosamente, se ha demostrado que una Ppl elevada en la obesidad severa protege contra la sobredistensión y el colapso hemodinámico durante las maniobras de alta presión, permitiendo un reclutamiento pulmonar efectivo con estabilidad cardiovascular preservada. Por lo tanto, la heterogeneidad del SDRA implica que prácticamente cualquier nivel de presión en las vías respiratorias influirá de manera diferente en la cascada vascular pulmonar en las distintas regiones pulmonares.
Implicaciones clínicas
En la práctica, las decisiones clínicas deben apuntar a restaurar la presión de perfusión efectiva y el gradiente de cascada vascular, en lugar de dirigirse a una PAM o presiones de llenado fijas. Dado que las terapias modifican la PaO2, la Pcrit y la Pmsf de manera diferente, la misma intervención puede mejorar la perfusión en un paciente y empeorarla en otro. Los fluidos, los vasopresores y las estrategias ventilatorias deben interpretarse a través de su efecto neto sobre estos gradientes, guiados por la vulnerabilidad específica de cada órgano y los marcadores sustitutivos disponibles. La PEEP debe titularse al nivel más bajo que mantenga la estabilidad alveolar y la oxigenación, prestando especial atención al estado volémico, la función del ventrículo derecho y la congestión; el mismo principio se aplica a las maniobras de reclutamiento. Las herramientas de monitorización, como la pulsatilidad de la vena porta, el gasto urinario, la perfusión mesentérica y los índices de retorno venoso dinámico, pueden guiar la titulación, especialmente cuando se requieren presiones de conducción más altas.
Direcciones futuras para el modelo de cascada vascular
Cascadas microvasculares
La fisiología clásica de la cascada vascular describe la limitación del flujo y el desacoplamiento de la presión cuando la presión crítica de cierre disocia la presión arterial proximal de la perfusión distal. En consonancia con este marco, algunos autores han propuesto un modelo de circulación cerebral que incorpora resistencias de Starling en serie, extendiendo el concepto de cascada arterial más allá de los vasos de resistencia proximales e implicando la existencia de cascadas microvasculares inmediatamente proximales a la verdadera red microcirculatoria. Se han identificado segmentos discretos de resistencia crítica precapilares, estructuralmente restringidos y regulados activamente por esfínteres precapilares, en la profundidad del árbol microvascular, distales a los capilares de primer orden, lo que sugiere que el desacoplamiento de la presión puede ocurrir mucho más cerca del lecho capilar de lo que se suponía anteriormente. Estos elementos de resistencia definidos por esfínteres generan grandes caídas de presión localizadas entre las arteriolas penetrantes cerebrales y la microcirculación distal, protegiendo así las redes capilares de la transmisión directa de la presión arterial y preservando la regulación del flujo. Es importante destacar que su impacto hemodinámico solo se manifiesta cuando existe un gradiente de presión proximal-inferior suficiente, una propiedad definitoria del comportamiento de la cascada. Extender el concepto de cascada a esta escala espacial invita a reinterpretar el acoplamiento presión-flujo microcirculatorio, sugiriendo que los fenómenos de resistencia crítica y el desacoplamiento de la presión pueden ser fundamentales para la regulación microvascular. Reconocer y caracterizar las cascadas microvasculares puede explicar la perfusión capilar preservada a pesar de las marcadas fluctuaciones de presión aguas arriba, refinar los modelos de regulación microcirculatoria en enfermedades agudas y crónicas, y facilitar la integración del control microvascular estructural en los marcos hemodinámicos contemporáneos.
Congestión venosa
Otro aspecto de la investigación es el papel de las cascadas vasculares en la congestión venosa sistémica, que ofrece nuevas perspectivas sobre la vulnerabilidad de los órganos. En lugar de una consecuencia uniforme de la PVC elevada, la congestión puede replantearse como un proceso heterogéneo y específico de cada órgano. Diversas resistencias de Starling venosas amortiguan parcialmente la transmisión retrógrada de la PVC para el hígado y el intestino, retrasando la disfunción. Por el contrario, el riñón carece de defensas similares, por lo que la hipertensión venosa se transmite directamente hacia atrás, sin amortiguación, elevando la presión de la cápsula de Bowman y perjudicando la filtración y el suministro de oxígeno. Estos mecanismos subyacen a la nefropatía congestiva y la lesión renal aguda (LRA), y explican por qué valores de PVC similares pueden producir respuestas orgánicas divergentes. En este contexto, la evaluación de la congestión mediante ultrasonido es esencial para identificar señales de intolerancia a los líquidos. Enmarcar la congestión venosa como un fenómeno de cascada es una perspectiva fisiológicamente fundamentada y conceptualmente novedosa que justifica un estudio más profundo.
Conclusiones
El modelo de cascada vascular, derivado de la analogía de la resistencia de Starling, proporciona un marco unificador para comprender la limitación del flujo, la autorregulación y la heterogeneidad de la perfusión regional en estados fisiológicos y patológicos. Al formalizar cómo el flujo sanguíneo puede independizarse de la presión aguas abajo y, en cambio, estar regido por gradientes aguas arriba vinculados al tono vascular local y la demanda metabólica, el modelo ofrece una comprensión mecanicista de las circulaciones sistémica, pulmonar, cerebral, coronaria y venosa. La división de la circulación en gradientes de presión distintos mejora la interpretación clínica del estado hemodinámico y ha permitido aplicaciones clínicamente relevantes, como la estimación de la presión transpulmonar (PTP), la evaluación de la eficacia de la norepinefrina en el shock y la predicción de los resultados renales tras la cirugía cardíaca.
Sin embargo, este marco presenta limitaciones importantes. Asume implícitamente condiciones de estado estacionario y una Pcrit fija, mientras que los estados clínicos dinámicos, como el shock cardiogénico, obstructivo o hipovolémico, así como el trauma grave, la sepsis y los cambios rápidos en el tono y la distensibilidad vascular, incluidos los cambios relacionados con la edad, pueden alterar notablemente la Pcrit en escalas de tiempo cortas. Estas fuentes de variabilidad aún no se han caracterizado completamente y limitan la generalización del modelo en condiciones no estacionarias.
El progreso futuro dependerá del desarrollo y la validación de métodos no invasivos o mínimamente invasivos para la estimación de Pcrit en tiempo real, lo que permitirá la evaluación continua a pie de cama de los gradientes de presión relevantes para la perfusión. Igualmente importante es la evaluación rigurosa de los supuestos del modelo fuera de la fisiología estacionaria. Abordar estos desafíos fortalecerá el marco de la cascada vascular como una herramienta clínicamente útil para el manejo hemodinámico de precisión y guiará el desarrollo de futuras estrategias de monitorización en la UCI.


