Resumen
Los modelos convencionales de la función cardiovascular priorizan la interacción entre la contractilidad cardíaca y las curvas de retorno venoso como determinantes principales del volumen sistólico. Sin embargo, este enfoque no considera la influencia de la carga arterial en la generación del flujo, lo que dificulta una comprensión más completa de la dinámica macrovascular. Dado que tanto el corazón como las arterias son cavidades elásticas con geometrías distintivas que albergan el volumen sanguíneo, su acoplamiento podría derivarse de las curvas presión-volumen, que en última instancia denotan relaciones de elastancia variables en el tiempo. En consecuencia, el acoplamiento ventrículo-arterial izquierdo (AVVI), representado por la relación entre las elastancias arterial y ventricular, podría estimar indirectamente la transmisión de energía del corazón al árbol arterial proximal, reflejando así la eficiencia cardiovascular. La evaluación del AVVI mediante la combinación de ecocardiografía a pie de cama y monitorización de la presión arterial puede mejorar la comprensión de la macrohemodinámica durante el shock y podría ayudar a evaluar el impacto de las terapias cardiovasculares. Sin embargo, la disfunción cardiovascular en el choque séptico resulta de interacciones complejas y grados muy variables de hipovolemia, vasodilatación patológica, desacoplamiento vascular periférico, mala distribución del flujo sanguíneo microvascular y disfunción de la bomba cardíaca, por lo que optimizar la LVAC durante el proceso de reanimación no necesariamente revertiría la hipoperfusión tisular. Esta revisión proporciona un análisis de los componentes de la LVAC, incluidos los fundamentos fisiológicos de las elastancias arteriales y ventriculares, explora su relación con la eficiencia y la energética cardiovascular, sintetiza los datos disponibles sobre la evaluación de la LVAC en el choque séptico, aborda algunas controversias sin resolver y propone un marco conceptual para futuras investigaciones.
Antecedentes
Los modelos clásicos que describen la función cardiovascular enfatizan la interacción entre la contractilidad cardíaca y las curvas de retorno venoso como los principales determinantes del volumen sistólico. Sin embargo, esta visión subestima el papel de la transmisión de energía del corazón a la periferia vascular y los efectos de la carga arterial en la generación del flujo sanguíneo. El corazón puede conceptualizarse como un generador de flujo que opera en conjunto con la poscarga arterial, es decir, la oposición mecánica que enfrenta el corazón al bombear sangre, denominada impedancia arterial. Si bien el flujo total generado por el sistema cardiovascular está impulsado en última instancia por las demandas metabólicas de los tejidos, la eficiencia mecánica ventricular está determinada fundamentalmente por la interacción entre la contractilidad cardíaca y la impedancia arterial. Esta interacción dinámica entre la contractilidad miocárdica y la carga vascular define el concepto de acoplamiento ventrículo-arterial izquierdo (AVAI).
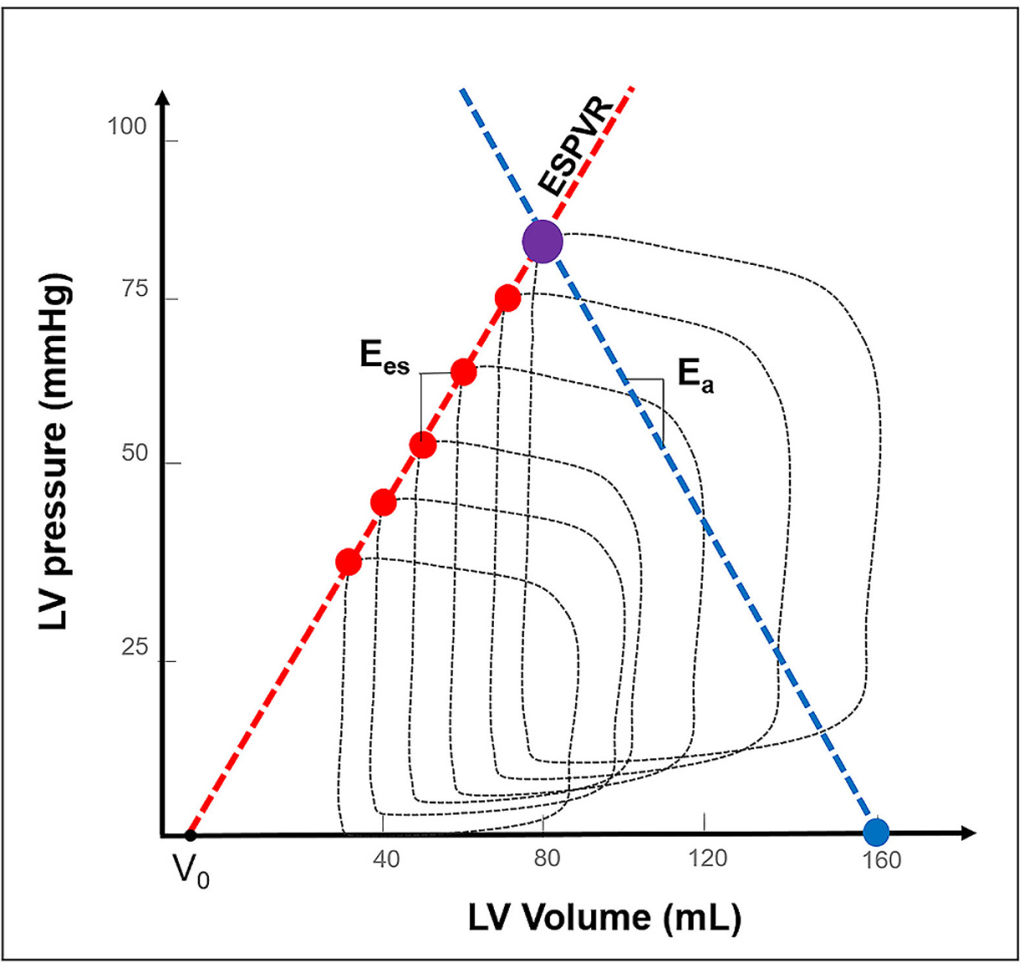
El AVAI describe la relación entre las condiciones de carga arterial, estimadas mediante la elastancia arterial (Ea), y la contractilidad cardíaca, estimada mediante la elastancia telesistólica (Ees). La relación Ea/Ees, una representación cuantitativa de la LVAC, proporciona un valor adimensional que puede ilustrarse en el diagrama presión-volumen (Fig. 1) y que, en última instancia, refleja la energía transmitida desde el corazón al árbol vascular proximal. En individuos sanos, los valores de LVAC (es decir, la relación Ea/Ees) deberían ser ligeramente inferiores a 1,0, lo que indica que, en condiciones fisiológicas, el sistema cardiovascular optimiza el gasto energético. Por el contrario, los valores de LVAC suelen superar 1,0 durante estados de shock, lo que refleja una contractilidad cardíaca deteriorada y/o condiciones de carga relativamente elevadas, una situación denominada desacoplamiento ventrículo-arterial izquierdo. Esta revisión tiene como objetivo proporcionar una comprensión fisiológica de la LVAC, detallando sus componentes (Ea y Ees), describiendo los métodos utilizados para su estimación y esbozando las bases fisiológicas que potencialmente respaldan la evaluación no invasiva de la LVAC para monitorizar la hemodinámica cardiovascular.
Elastancia arterial: el concepto fisiológico
El origen de la carga arterial
La carga arterial puede definirse como la restricción al flujo generado por una bomba hidráulica, que consecuentemente presuriza el sistema. El concepto fisiológico de carga arterial abarca componentes tanto resistivos como pulsátiles. El componente resistivo comprende las fuerzas hidráulicas que se oponen al flujo no pulsátil y representa la mayor parte de la carga arterial (80-90%). Por otro lado, el componente pulsátil surge de la actividad contráctil intermitente del corazón y de la incapacidad del sistema arterial para amortiguar completamente las oscilaciones generadas por la eyección ventricular cíclica. Cabe destacar que, en condiciones fisiológicas, la contribución del componente pulsátil a la carga hidráulica es baja (10-20%) debido a la alta distensibilidad de la aorta proximal. La suma de los componentes resistivo y pulsátil de la carga arterial representa la impedancia (Z) del sistema vascular. Por lo tanto, la carga arterial que soporta el corazón puede cuantificarse a partir de la estimación de Z a nivel aórtico (es decir, la impedancia de entrada). Z es un número complejo compuesto por componentes de magnitud (real) y fase (imaginaria), que se puede obtener mediante el análisis de frecuencia de la presión (P) y el flujo (Q) simultáneos durante uno o varios latidos cardíacos. Por lo tanto, los fenómenos oscilatorios de P y Q, representados en la ecuación 1, indican la magnitud (o valor absoluto) de Z.
La impedancia vascular proporciona información sobre la estructura y la función arterial. Intrínsecamente, es una magnitud en el dominio de la frecuencia que caracteriza la oposición al flujo pulsátil al cuantificar el nivel de almacenamiento y disipación de la energía hidráulica.
Estimación de la impedancia arterial mediante el análisis de la transformada de Fourier.
Según el teorema de Fourier, una función periódica puede expresarse como la suma de una serie de términos seno o coseno. Por lo tanto, cualquier señal periódica puede descomponerse en una serie de ondas sinusoidales (también llamadas armónicos) con frecuencias crecientes como múltiplos de la frecuencia fundamental original (en este caso, la frecuencia cardíaca). Dado que las ondas de presión y flujo arterial son de naturaleza oscilatoria en condiciones de estado estacionario cardiovascular, la cuantificación de la impedancia (Z) es posible transformando dichas ondas de presión y flujo en múltiples ondas sinusoidales superpuestas o armónicos, mediante la transformada de Fourier. La relación entre la presión y el flujo del armónico correspondiente proporciona la impedancia (Z) para las frecuencias presentes en el espectro, correspondiendo los armónicos inferiores y superiores a frecuencias inferiores y superiores de Z, respectivamente.
El análisis de Fourier permite descomponer Z en dos componentes clave en el dominio de la frecuencia: la magnitud (│Z│) y la fase (θ) (Fig. 2, Panel A). La magnitud │Z│ representa el valor absoluto de la impedancia en cada frecuencia, cuantificando la oposición total al flujo pulsátil independientemente del retardo entre las ondas de presión y flujo. Por otro lado, la fase (θ) refleja la dirección del retardo entre dichas ondas, donde θ < 0 implica que el retardo de fase de la presión es mayor que el retardo de fase del flujo, por lo que el flujo se adelanta a la presión. Este comportamiento indica un sistema que actúa como un capacitor, donde se necesita flujo para cargar la capacitancia y generar presión. Por otro lado, θ > 0 implica que el retardo de fase de la presión es menor que el retardo de fase del flujo, por lo que la presión se adelanta al flujo. Este comportamiento indica un sistema donde predomina la inercia y donde se requiere un cierto aumento de presión para generar el flujo. En conjunto, todos estos componentes describen si el sistema cardiovascular se comporta predominantemente como un capacitor o un inductor a una frecuencia dada (Fig. 2, Panel A).
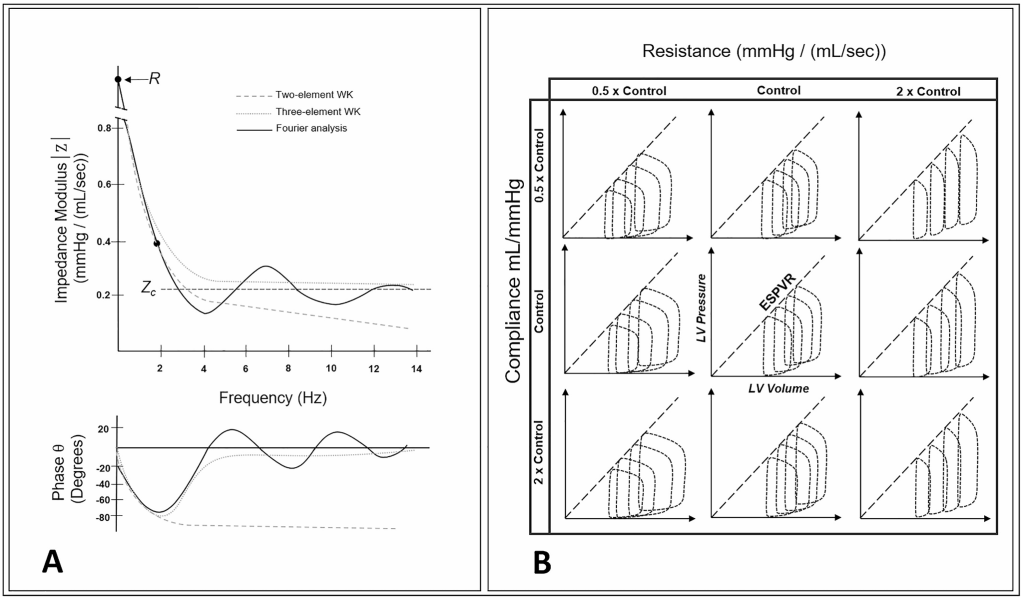
Panel A. El módulo de impedancia (│Z│) y la fase (θ) se representan en función de la frecuencia. El valor de │Z│ a frecuencia cero corresponde a la resistencia vascular sistémica (R). A medida que aumenta la frecuencia, │Z│ disminuye gradualmente, alcanzando su mínimo donde la fase (θ) cruza cero. Esta región de frecuencia intermedia de │Z│ está fuertemente influenciada por la compliancia arterial, que refleja la capacidad de las arterias para almacenar y liberar sangre durante el flujo pulsátil. A frecuencias más altas, │Z│ se aproxima a la impedancia característica (Zc), que está determinada por las propiedades físicas del sistema arterial, incluyendo la rigidez de la pared arterial y la densidad sanguínea. Adaptado de Westerhof et al.
Panel B. Múltiples bucles P-V representados a diferentes condiciones de carga. Cada gráfica muestra 4 volúmenes telediastólicos diferentes con distintas combinaciones de compliancias y resistencias. Adaptado de Sunagawa et al.
La transformada de Fourier proporciona un análisis detallado de Z. Sin embargo, la evaluación de Z mediante este método en la práctica clínica no es sencilla, ya que implica la cuantificación simultánea de presiones y flujos en un vaso arterial determinado. Además, la evaluación de Z en diferentes dominios de frecuencia complica su interpretación a pie de cama. Por consiguiente, los métodos para estimar la carga arterial suelen priorizar modelos fisiológicos simplificados en los que Ea (como indicador de Z) se evalúa en el dominio del tiempo.
El modelo de Windkessel y el cálculo de la impedancia
El modelo de Windkessel, introducido por Otto Frank en 1899, debe su nombre a la columna de aire utilizada para impulsar agua continuamente desde una bomba hidráulica cíclica. En su conceptualización inicial, el modelo constaba de solo dos componentes principales: (i) un componente proximal, que determina la compliancia del sistema (C), representada principalmente por las propiedades elásticas de la aorta; y (ii) un componente distal, representado por arteriolas y capilares, que determina predominantemente la resistencia del sistema (R). Teóricamente, la interacción entre estos elementos dilucidaría cómo el sistema cardiovascular mantiene un flujo relativamente constante durante la diástole. Sin embargo, la simplificación excesiva de la función cardiovascular a estos dos únicos componentes (R y C) resultó insuficiente para capturar completamente la complejidad subyacente a la impedancia total del sistema vascular. Esta limitación impulsó la modificación del modelo original mediante la introducción de un tercer elemento: la impedancia característica (Z C ), definida como la relación entre los armónicos de la presión incidente y el flujo incidente. Z C puede cuantificarse mediante la impedancia de entrada en ausencia de reflexiones de onda, y generalmente se estima mediante la media aritmética de los valores │Z│ a frecuencias superiores a 2 Hz. Es importante destacar que, dado que Z C excluye la información de las reflexiones de onda, es independiente de la frecuencia cardíaca y de las propiedades de los lechos vasculares distales. Este componente adicional explica la aceleración del flujo sanguíneo al inicio de la sístole y se define por las propiedades físicas de la raíz aórtica. La incorporación de Z C al modelo de Windkessel de tres elementos permitió una mejor aproximación de Z. Desafortunadamente, debido a la naturaleza ramificada y a las propiedades elásticas espacialmente variables del árbol arterial, no es posible un cálculo directo de Z C a partir de datos hemodinámicos medidos. En su lugar, Z C debe inferirse a partir del espectro de impedancia de entrada a altas frecuencias (donde las reflexiones tienen menor impacto) o a partir de datos de presión y flujo medidos durante la fase inicial de eyección antes de que las ondas reflejadas hayan regresado al punto de medición. Sin embargo, las limitaciones para medir Z C se han superado mediante enfoques más sencillos que se analizarán a continuación.
Elastancia arterial como aproximación de la impedancia (Z)
Siguiendo el modelo de Windkessel de tres elementos, Sunagawa y sus colegas propusieron la elastancia arterial efectiva (Ea) como un sustituto de Z en el dominio del tiempo. Dado que el concepto de elastancia abarca las relaciones entre presiones y volúmenes, Ea podría considerarse una representación de las condiciones externas que se oponen a la eyección del volumen sistólico (VS). De hecho, Ea podría representarse mediante la relación entre la presión telesistólica del ventrículo izquierdo (Pes) y VS (Ec. 2) (véase el Apéndice A). Por lo tanto, Ea sirve como un parámetro integrador que abarca los principales componentes de la carga arterial: (i) el elemento resistivo; (ii) la compliancia arterial total; y (iii) la impedancia característica. En consecuencia, cuantificar Z en términos de Ea permite expresar Z a través de las relaciones presión-volumen (P-V) de una manera más sencilla en el dominio del tiempo, sin utilizar el análisis de Fourier ni las representaciones en el dominio de la frecuencia. Así, Ea podría expresarse fácilmente como:
Elastancia telesistólica
Elastancia telesistólica y los bucles presión-volumen
El concepto de Ees, introducido por Suga y colaboradores, se basa en la independencia de la contractilidad ventricular respecto a las condiciones de carga (tanto precarga como poscarga). Las primeras observaciones experimentales sugirieron que la pendiente de la relación presión-volumen telesistólica (ESPVR) se ve influenciada por variaciones en la contractilidad ventricular intrínseca. Cabe destacar que el punto de presión-volumen telesistólico de cualquier ciclo cardíaco se sitúa a lo largo de la misma ESPVR en un amplio rango de estados de carga, como demostraron Sunagawa y colaboradores, quienes corroboraron la independencia entre la carga y la ESPVR al conectar el tracto de salida del ventrículo izquierdo de un corazón canino ex vivo a una máquina servocontrolada para recrear condiciones de carga variables mientras se registraban las curvas P-V mediante catéteres de presión-conductancia.
La pendiente de la ESPVR izquierda permanece prácticamente constante a través de múltiples combinaciones de volúmenes telediastólicos (VTD), resistencias y compliancias (Fig. 2, Panel B). Por lo tanto, la pendiente de la ESPVR izquierda refleja fielmente la contractilidad del ventrículo izquierdo y adquiere la denominación de elastancia telesistólica (Ees), ya que representa la relación entre las variaciones concurrentes en las presiones y volúmenes telesistólicos del ventrículo izquierdo. La Ees podría entonces estimarse como la razón entre Pes y la diferencia entre el volumen telesistólico (VTS) y el volumen restante en la intersección del eje de la ESPVR (que denota el volumen ventricular a presión cero, es decir, el Vo) (Ec. 3, Fig. 1).
Desafortunadamente, la estimación directa de Ees implica un procedimiento complejo y engorroso en el que se adquieren múltiples bucles presión-volumen ventriculares a diferentes volúmenes telediastólicos (VTD), generalmente reduciendo el retorno venoso mediante la oclusión con balón de la vena cava inferior (Fig. 2, Panel B). Además, la estimación de Ees requiere una cuantificación precisa de las presiones y volúmenes intraventriculares izquierdos mediante catéteres de impedancia invasivos, lo que hace que este método sea poco práctico para su uso rutinario en la práctica clínica. Por ello, los métodos no invasivos para estimar Ees mediante el análisis de latidos únicos del ventrículo izquierdo sin manipular las condiciones de carga han ganado mayor popularidad.
Estimación de la elastancia telesistólica mediante métodos no invasivos de un solo latido.
Se han utilizado múltiples técnicas para estimar Ees sin modificar las condiciones de carga. Estas estiman LVAC durante un ciclo cardíaco y se denominan colectivamente métodos de Ees de latido único (Ees (SB)), aunque algunas de ellas aún requieren la cuantificación simultánea de la presión y el volumen intraventriculares. Los métodos no invasivos que estiman Ees (SB) se basan en aproximaciones matemáticas del comportamiento de la elastancia ventricular izquierda en el dominio del tiempo (E (t)), que permiten estimar Ees ajustando variables que hacen que E (t) sea independiente de las condiciones de carga. Entre ellos, la evaluación ecocardiográfica de Ees (SB) es quizás la más utilizada en el ámbito clínico. Este enfoque, introducido por Chen y colaboradores, evalúa el comportamiento de E (t) en función de parámetros relativamente simples: tiempos de preeyección y eyección, presiones aórticas sistólica y diastólica, volumen sistólico y volúmenes telesistólico y telediastólico del ventrículo izquierdo (véase el Apéndice C del Material Suplementario: evaluación ecocardiográfica de LVAC). Sorprendentemente, este enfoque asume que E(t) permanece constante durante la contracción isovolumétrica, independientemente de las condiciones de carga. Desafortunadamente, la Ees evaluada mediante este método podría ser algo imprecisa en comparación con otras estimaciones de Ees(SB). No obstante, a pesar de sus limitaciones, un documento de consenso reciente sobre el papel de la evaluación del acoplamiento ventrículo-arterial en la cardiopatía y la insuficiencia cardíaca acepta, e incluso recomienda, el enfoque ecocardiográfico no invasivo para estimar la Ees, ya que es relativamente fácil de usar a pie de cama.
El acoplamiento ventrículo-arterial izquierdo (LVAC)
LVAC y el concepto de transmisión de energía del corazón al árbol arterial proximal
La relación entre la función del ventrículo izquierdo y las propiedades mecánicas del árbol arterial proximal representa un factor crítico para comprender el rendimiento y la energética cardiovascular. Los estudios originales de Suga y Sunagawa sentaron las bases del concepto de LVAC y su evaluación a través del análisis de la relación P-V del ventrículo izquierdo. En esencia, el diagrama P-V del ventrículo izquierdo proporciona información sobre la transmisión de energía desde el ventrículo izquierdo al árbol arterial proximal (Fig. 3, Panel A). Así, el área cuadrangular contenida por el bucle P-V representa el trabajo sistólico externo o mecánico del ventrículo izquierdo, LVSW (es decir, el trabajo producido para expulsar el volumen sistólico en la aorta presurizada), mientras que el área bajo ESPVR circunscrita entre V0 y ESV representa la energía potencial del ventrículo izquierdo (PE). Mientras tanto, el área total circunscrita por la suma de LVSW y PE, es decir, el área total de presión-volumen (PVA), representa la energía mecánica total generada por el ventrículo izquierdo durante un ciclo cardíaco (Fig. 3, Panel A), mientras que la relación LVSW/PVA refleja la eficiencia bioenergética del ventrículo izquierdo.
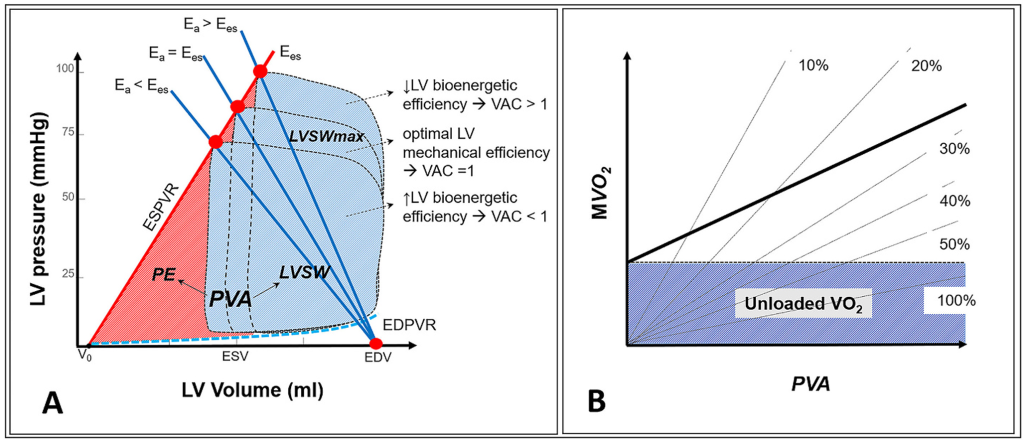
Panel A. El área presión-volumen (APV) equivale a la suma del trabajo sistólico del ventrículo izquierdo (TSVI) (área delimitada en azul) y la energía potencial (EP) (área delimitada en rojo). El trabajo sistólico máximo externo o mecánico del ventrículo izquierdo, TSVI (TSVImáx), se alcanza cuando Ea = Ees (es decir, AVAC = 1), lo que refleja la máxima eficiencia mecánica del ventrículo izquierdo. En condiciones de Ea < Ees (AVAC < 1), el ventrículo izquierdo optimiza su eficiencia bioenergética (es decir, mayor relación TSVI/APV). Por otro lado, cuando Ea > Ees (AVAC > 1), el ventrículo izquierdo prioriza la transferencia de energía a la periferia (es decir, menor relación TSVI/APV); en esta última condición, el aumento del consumo de oxígeno miocárdico no mejora significativamente la cantidad de TSVI.
Panel B. Consumo de oxígeno miocárdico (MVO₂) frente a PVA. La pendiente de la línea resultante representa el equivalente de la fracción de energía derivada del consumo de oxígeno miocárdico que se convierte en trabajo mecánico total. El MVO₂ bajo la intersección con el eje “X” representa el MVO₂ sin carga (es decir, el consumo de oxígeno miocárdico no relacionado con los procesos de contractilidad mecánica: metabolismo basal, ciclo del calcio, etc.). (Para la interpretación de las referencias de color en esta leyenda, consulte la versión web de este artículo).
Curiosamente, Suga y colaboradores demostraron que la PVA está estrechamente relacionada con el consumo de oxígeno miocárdico (MVO₂). De hecho, al representar gráficamente MVO₂ frente a PVA, se obtiene una línea recta incluso bajo diversas condiciones de precarga y poscarga, así como en distintos estados contráctiles. La pendiente de esta línea representa la fracción de energía derivada del consumo de oxígeno miocárdico que se convierte en trabajo mecánico total (Fig. 3, panel B). Por consiguiente, la relación LVSW/PVA debería reflejar la eficiencia mecánica de la conversión de la energía total disponible (es decir, la PVA) en trabajo externo del ventrículo izquierdo (Fig. 3, paneles A y B).
La evaluación/monitorización de LVAC y su potencial valor clínico.
LVAC refleja la transmisión de energía del corazón al árbol arterial proximal. En un rango de estados contráctiles, el LVSW máximo teóricamente ocurre cuando Ea coincide con Ee (es decir, cuando Ea = Ees, o LVAC = 1). Mientras tanto, la eficiencia miocárdica máxima, es decir, la cantidad de trabajo externo realizado dividida por el oxígeno miocárdico consumido, ocurre cuando Ea es aproximadamente la mitad de Ees, durante cada estado contráctil (es decir, LVAC ≅ 0,5). Cabe destacar que, durante los estados de shock, el sistema cardiovascular puede operar con valores altos o bajos de LVAC (es decir, relaciones Ea/Ees altas o bajas), lo que sugiere un gasto energético alto o bajo (Fig. 4). Sin embargo, tanto un LVAC alto como uno bajo no reflejan necesariamente la adecuación o inadecuación de la macrohemodinámica para satisfacer las demandas metabólicas tisulares; es decir, los valores anormales de LVAC no deben confundirse con la presencia o ausencia de shock.
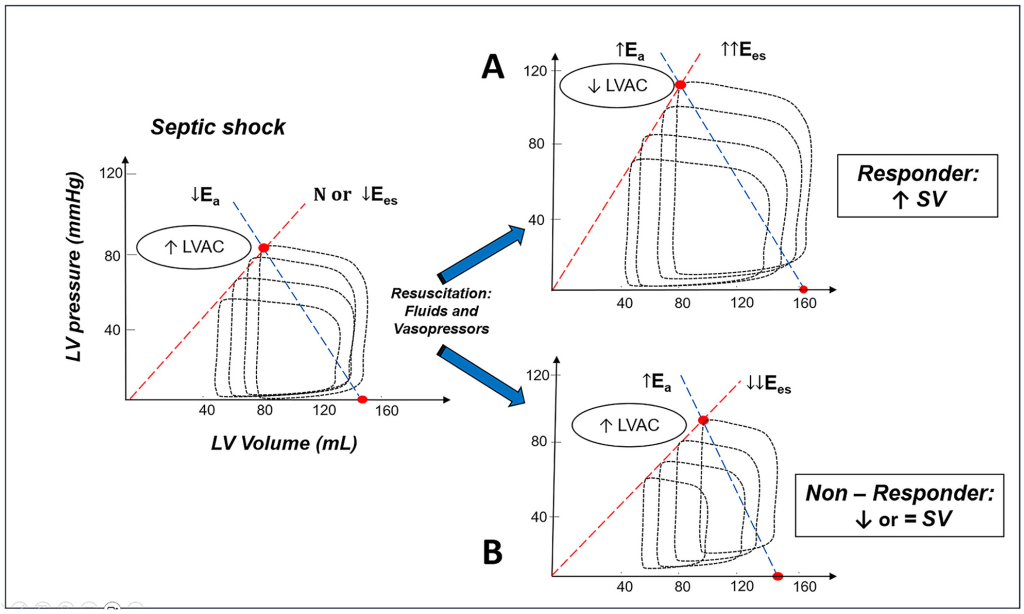
Se muestran dos escenarios hipotéticos: Panel A. Aumento significativo del volumen sistólico (VS), como consecuencia del aumento predominante de la Ees y la consiguiente disminución de la LVAC, lo que conduce a una mejoría del VS; Panel B. Aumento no significativo del volumen sistólico, ya que el aumento de la Ea no se corresponde con la Ees, lo que conlleva un deterioro posterior de la LVAC.
Desde un punto de vista fisiológico, cualquier condición en la que Ea supere Ees (es decir, LVAC > 1) podría definirse como desacoplamiento ventrículo-arterial. Sin embargo, las observaciones en personas sanas han revelado índices Ea/Ees promedio de entre 1,0 y 1,36, lo que dificulta la identificación de un punto crítico exacto por encima del cual se pueda establecer el desacoplamiento ventrículo-arterial. A pesar de esta limitación evidente, un estado de desacoplamiento implica que un mayor consumo de oxígeno miocárdico no se traducirá en una mejora del trabajo ventricular transmitido posteriormente al árbol arterial proximal. Esto podría explicar por qué valores de LVAC progresivamente más bajos se han asociado con tasas de supervivencia más favorables en pacientes con insuficiencia cardíaca crónica, mientras que valores de LVAC progresivamente más altos durante la ecocardiografía de estrés podrían anticipar peores resultados clínicos.
No obstante, más allá de los valores estáticos, las variaciones de LVAC en respuesta a las intervenciones terapéuticas podrían reflejar el desempeño del sistema cardiovascular durante la reanimación hemodinámica en estados de shock. Así, por ejemplo, la infusión de norepinefrina en pacientes hipotensos posoperatorios solo aumentó el volumen sistólico en aquellos con una LVAC alterada al inicio, aunque la hipotensión arterial se corrigió en toda la cohorte. De hecho, aquellos que aumentaron el volumen sistólico durante la infusión de norepinefrina mostraron aumentos simultáneos, pero no simétricos, en la elastancia ventricular arterial y telesistólica, con la consiguiente disminución de la LVAC. No debe descuidarse el impacto de la norepinefrina en la poscarga del ventrículo izquierdo. De hecho, si bien la corrección de la hipotensión puede restablecer el flujo orgánico, los aumentos exagerados de la poscarga ventricular pueden limitar la generación de flujo. Por lo tanto, el impacto de la terapia vasopresora en el gasto cardíaco depende del equilibrio entre los efectos directos sobre el propio corazón (es decir, aumento de la perfusión coronaria, mejora de la energética cardíaca, etc.) y el impacto en la carga arterial, una situación que puede detectarse o incluso anticiparse cuando se monitoriza cuidadosamente la LVAC. Sin embargo, la evaluación de la presión arterial ventricular izquierda (PAVI) no forma parte de la monitorización hemodinámica convencional, a pesar de la información reciente que destaca su valor en la reanimación, el pronóstico y los algoritmos de manejo en diversos contextos clínicos. Por el contrario, las intervenciones dirigidas al manejo de la disfunción cardiovascular en estados de shock se centran principalmente en las curvas de retorno venoso y gasto cardíaco, sin tener en cuenta el papel de la carga arterial en la generación de flujo y su efecto en el rendimiento cardíaco.
Acoplamiento ventrículo-arterial izquierdo en el choque séptico
En general, el desacoplamiento ventrículo-arterial es común durante los estados de shock como reflejo de grados variables de Ea y Ees ( Fig. 4 ). Curiosamente, tanto la vasoplejía séptica como la no séptica también pueden mostrar valores de LVAC aumentados debido a la coexistencia de disfunción miocárdica alterada. Además, las intervenciones terapéuticas comúnmente utilizadas en el shock séptico, como vasopresores e inodilatadores, pueden influir tanto en Ea como en Ees, lo que resulta en condiciones variables de LVAC. Sin embargo, los datos sobre las variaciones dinámicas y el curso temporal de LVAC en pacientes con sepsis son limitados y provienen principalmente de estudios de cohortes de tamaño pequeño. Utilizando ecocardiografía a pie de cama y monitorización de la presión arterial, Guarracino y colegas informaron de desacoplamiento ventrículo-arterial en 21 de 25 pacientes con shock séptico (LVAC medio de 1,81; RIC: 1,49–2,03). Posteriormente, estudiaron el efecto de diferentes intervenciones sobre LVAC en 55 pacientes con sepsis [44] . Los pacientes con LVAC casi normal al inicio mostraron mayores aumentos en el gasto cardíaco (GC) y la presión arterial media (PAM) después de la carga de volumen y el inicio de norepinefrina en comparación con aquellos con valores altos de LVAC. Cabe destacar que el LVAC disminuyó después de la administración de líquidos (1,57 ± 0,37 a 1,27 ± 0,36, p < 0,05) en aquellos pacientes en quienes el GC aumentó significativamente. Por otro lado, el LVAC aumentó significativamente después de la administración de norepinefrina en aquellos incapaces de aumentar el VS (1,15 ± 0,38 a 1,80 ± 0,62, p < 0,05), o incapaces de normalizar la PAM (1,38 DE: 0,44 a 2,12 DE: 0,59 < 0,05). Más recientemente, Zhou y colegas analizaron el desempeño operativo del LVAC para predecir cambios en el VS en respuesta a la infusión de norepinefrina en 38 pacientes con choque séptico. Descubrieron que un LVAC >1,11 predecía aumentos >15% en el VS tras el inicio de la norepinefrina (AUC: 0,816; IC del 95%: 0,646–0,927; p < 0,001). Como se describió previamente, esta respuesta podría explicarse por el efecto de la norepinefrina sobre la Ees. Curiosamente, a pesar de los aumentos en la presión arterial, solo los pacientes con mejoría del LVAC mostraron un aumento significativo del CO tras la administración de norepinefrina.
Los datos sobre el valor pronóstico del LVAC sugieren la amplia heterogeneidad de las alteraciones hemodinámicas en el choque séptico. Nasu y colaboradores informaron que el desacoplamiento ventrículo-arterial izquierdo ocurre con frecuencia en la sepsis y su causa —ya sea un aumento relativo de la Ea o una disminución de la Ees— varía a lo largo del curso clínico. Sorprendentemente, un estudio reciente describió una correlación en forma de U entre la LVAC evaluada durante las primeras 24 horas de ingreso en la UCI y los resultados clínicamente relevantes en pacientes con choque séptico, lo que sugiere que los valores bajos de LVAC (como resultado de una Ees alta combinada con una Ea baja, durante condiciones hiperdinámicas) también son desfavorables y, por consiguiente, los resultados clínicos no están necesariamente vinculados a la eficiencia bioenergética cardiovascular.
La evaluación de la LVAC podría proporcionar información valiosa para guiar la terapia después de los esfuerzos iniciales de reanimación (Fig. 5). Así, por ejemplo, el soporte inotrópico podría ser beneficioso en pacientes con Ees persistentemente baja después de la reanimación inicial con fluidos y el soporte vasopresor. Mientras tanto, los pacientes con Ea aumentada pero Ees conservada podrían beneficiarse teóricamente de una disminución de la dosis de vasopresor (Fig. 5), aunque, por supuesto, bajo una estrecha monitorización de la perfusión tisular. Sin embargo, la información sobre el impacto clínico de la monitorización de la LVAC durante la reanimación del choque séptico es limitada. Recientemente, Zhou et al. Se aleatorizaron 83 pacientes con sepsis y evidencia de desacoplamiento ventrículo-arterial (definido por LVAC >1,36) a reanimación guiada por LVAC frente a atención habitual. Los pacientes sometidos a reanimación guiada por LVAC presentaron una eliminación de lactato más rápida (27,7 % RIC: 11,9–45,7 frente a 18,3 % RIC: 5,7–32,1, p = 0,038), aunque sin impacto en la mortalidad. Por lo tanto, si bien es fisiológicamente plausible, se necesita más información para estimar el valor clínico de la reanimación guiada por LVAC en el choque séptico.
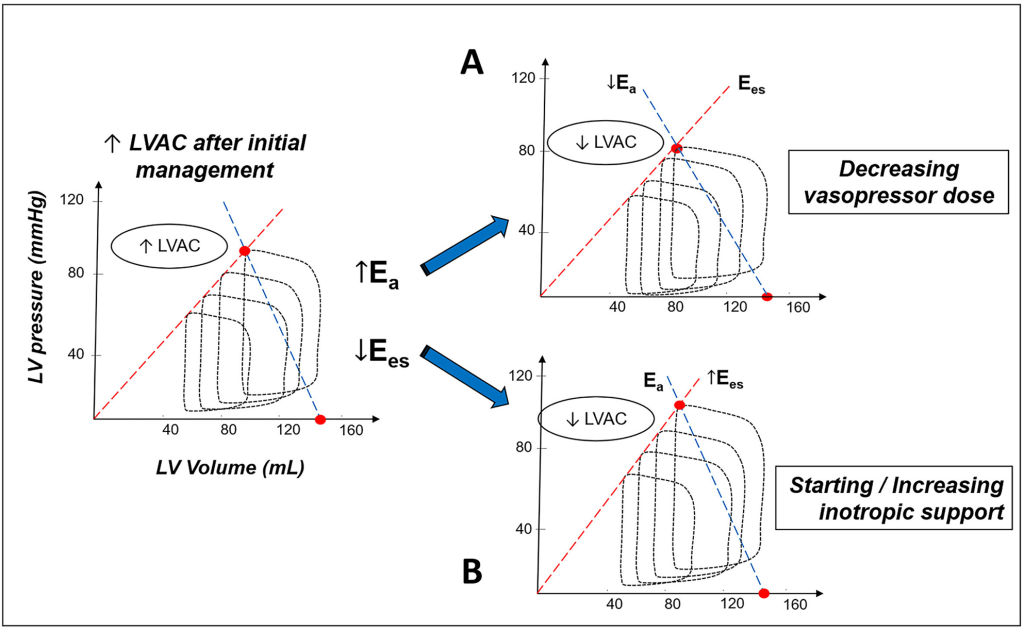
Panel A. Aumento de la elastancia arterial (Ea) con elongación espiratoria (Ees) conservada. En este caso, la disminución de la dosis de vasopresores podría aumentar el volumen sistólico (VS); sin embargo, este ajuste debe realizarse bajo estricta monitorización de la perfusión tisular. Panel B. Disminución de la Ees. En este caso, el inicio o ajuste del soporte inotrópico debería disminuir la PAVI, aumentando así el VS.
Ventilación asistida con presión negativa en el choque séptico: incertidumbres y perspectivas
Aunque existe un creciente interés en la dinámica del acoplamiento ventrículo-arterial en pacientes críticos, la evaluación del LVAC y su utilidad potencial durante la reanimación del shock plantean aspectos conceptuales que merecen mayor exploración. En primer lugar, la concordancia entre los diversos métodos para estimar la Ees (SB) no está exenta de controversia. Además, la precisión y equivalencia de los métodos no invasivos, como la ecocardiografía o el análisis de la onda de pulso periférica, para estimar la elastancia ventricular siguen siendo cuestionables. En segundo lugar, la estimación no invasiva del LVAC mediante ecocardiografía puede resultar engorrosa, ya que se requieren mediciones repetidas para evaluar su evolución durante el proceso de reanimación. En tercer lugar, el shock séptico puede inducir un desacoplamiento central-periférico en la propagación de la onda de presión. Este fenómeno podría conducir a una estimación inexacta de las elastancias al utilizar presiones periféricas (es decir, radiales, femorales) en lugar de presiones aórticas centrales en condiciones de vasodilatación severa; si bien, ciertamente, el error afectaría de forma casi simétrica la precisión de los valores de Ea y Ees y, en consecuencia, no debería afectar ampliamente el cálculo del LVAC en sí. En cuarto lugar, aunque los fundamentos de LVAC parecen tener plausibilidad biológica, no existe evidencia convincente de que la normalización del cociente Ea/Ees se traduzca en una perfusión tisular óptima, especialmente en condiciones de mayor heterogeneidad del flujo microvascular. En quinto lugar, si bien un estudio reciente de pequeña escala sugirió que la reanimación guiada por LVAC podría mejorar la eliminación de lactato, la hiperlactatemia en la sepsis es un fenómeno complejo que va más allá de la hipoxia tisular. En sexto lugar, aunque algunos datos de cirugía cardíaca posoperatoria sugieren que las variaciones en LVAC se correlacionan con el consumo global de oxígeno, las interacciones entre el suministro y el consumo de oxígeno en la sepsis y el choque séptico dependen de muchas otras variables complejas. Por lo tanto, si bien la reanimación macrohemodinámica representa un elemento clave para revertir la hipoperfusión tisular en el choque séptico, la optimización de LVAC no puede garantizar una perfusión y oxigenación tisular adecuadas. De hecho, la macrohemodinámica se disocia frecuentemente del flujo sanguíneo microcirculatorio en el choque séptico, como lo han expuesto ampliamente otros autores. En séptimo lugar, la disfunción cardiovascular en la sepsis y el choque séptico resulta de la combinación de diversos grados de hipovolemia absoluta o relativa (debido a la pérdida de líquidos externos y al aumento de la fuga capilar), vasodilatación patológica, disfunción miocárdica y mala distribución del flujo sanguíneo microvascular. Por consiguiente, la normalización u optimización de la presión arterial ventricular izquierda (PAVI) podría ser insuficiente para revertir el proceso de choque a nivel celular, por lo que se deben realizar importantes esfuerzos de investigación para dilucidar el verdadero valor clínico de la evaluación de la PAVI para guiar las terapias durante la reanimación del choque séptico.
Conclusión
El acoplamiento ventrículo-arterial izquierdo (AVAI) es un concepto fisiológico que integra las elastancias arteriales y ventriculares, permitiendo comprender las interacciones entre la contractilidad cardíaca y la impedancia del árbol arterial proximal. Este concepto proporciona una visión holística de la relación entre el trabajo mecánico sistólico y el consumo de oxígeno miocárdico, detallando la contractilidad cardíaca y sus propiedades bioenergéticas. Si bien el AVAI se asocia con resultados en pacientes críticos y se ha utilizado para analizar el efecto de las intervenciones hemodinámicas, actualmente no existe evidencia clínica que demuestre que la normalización del AVAI durante la reanimación del choque séptico siempre revierta la hipoperfusión tisular. Se requieren estudios más detallados que analicen las relaciones entre el AVAI y la perfusión tisular para dilucidar el papel de la monitorización del AVAI en pacientes con sepsis y choque séptico.


