La deficiencia de yodo es aún la causa más frecuente de hipotiroidismo en el mundo. En regiones con suficiente yodo, son más frecuentes la enfermedad autoinmunitaria (tiroiditis de Hashimoto) y las causas yatrógenas (tratamiento del hipertiroidismo) (cuadro 1).
Primario |
Hipotiroidismo autoinmunitario: tiroiditis de Hashimoto, tiroiditis atrófica |
Yatrógeno: tratamiento con 131I, tiroidectomía total o subtotal, radiación externa del cuello para tratamiento de un linfoma o de cáncer |
Fármacos: exceso de yodo (incluidos los medios de contraste con yodo), amiodarona, litio, fármacos antitiroideos, acido p-aminosalicílico, interferón α y otras citocinas, aminoglutetimida, inhibidores de tirosina cinasa (p. ej., sunitinib), inhibidores de puntos de verificación inmunitaria (p. ej., ipilimumab, nivolumab, pembrolizumab) |
Hipotiroidismo congénito: ausencia o ectopia de la glándula tiroides, dishormonogénesis, mutación del gen del TSH-R |
Deficiencia de yodo |
Trastornos infiltrativos: amiloidosis, sarcoidosis, hemocromatosis, esclerodermia, cistinosis, tiroiditis de Riedel |
Expresión excesiva de desyodinasa tipo 3 en hemangioma infantil y otros tumores |
Transitorio |
Tiroiditis asintomática, incluida la tiroiditis puerperal |
Tiroiditis subaguda |
Interrupción del tratamiento suprafisiológico con tiroxina en personas con glándula tiroides intacta |
Después de 131I o de la tiroidectomía subtotal para la enfermedad de Graves |
Secundario |
Hipopituitarismo: tumores, cirugía o irradiación hipofisaria, trastornos infiltrativos, síndrome de Sheehan, traumatismos, formas genéticas de deficiencia de hormonas hipofisarias combinadas |
Déficit o inactividad aislada de TSH |
Fármacos: bexaroteno, mitotano |
Enfermedades hipotalámicas: tumores, traumatismos, trastornos infiltrativos, síndrome de Prader-Willi |
Cuadro 1. Causas de hipotiroidismo. Abreviaturas: TSH, hormona estimulante de tiroides; TSH-R, receptor de hormona estimulante de tiroides.
Hipotiroidismo congénito
Prevalencia
El hipotiroidismo ocurre en cerca de 1 de 2 000 a 4 000 recién nacidos, y en la mayor parte de los países industrializados se realiza detección neonatal. Puede ser transitorio, en especial si la madre tiene anticuerpos bloqueadores del receptor de la hormona estimulante del tiroides (TSH-R) o ha recibido fármacos antitiroideos, pero en la mayoría de los casos el hipotiroidismo es permanente. Las causas del hipotiroidismo neonatal incluyen disgenesia de la glándula tiroides en 65% de los casos, metabolopatías congénitas de la síntesis de hormona tiroidea en 30%, y está regulado por anticuerpos contra TSH-R en 5% de los recién nacidos afectados. Las anomalías del desarrollo son dos veces más frecuentes en las niñas. Cada vez se identifican con mayor frecuencia mutaciones que causan hipotiroidismo congénito, pero la mayor parte son idiopáticas. En términos generales, estas pueden clasificarse como mutaciones que causan 1) hipotiroidismo central por desarrollo hipotálamo-hipófisis anormal o la pérdida de componentes específicos de las vías de la hormona liberadora de tirotropina (TRH)/TSH; 2) desarrollo anormal de la glándula tiroides o disgenesia, o 3) síntesis y procesamiento anormales de hormonas tiroideas o trastornos hormonales (cuadro 2). El paso transplacentario de la hormona tiroidea materna ocurre antes que la glándula tiroides fetal comience a funcionar y proporciona un apoyo hormonal parcial al feto con hipotiroidismo congénito.
Proteína génica defectuosa |
Tipo de hipotiroidismo |
Forma de herencia |
Consecuencias |
PROP-1 |
Central, hipotiroidismo |
Homocigoto recesivo |
|
PIT-1 |
Central, hipotiroidismo |
Pérdida de función homocigota o heterocigota |
Deficiencias combinadas de hormona del crecimiento, prolactina y hormona estimulante de la glándula tiroides (TSH) |
IGSF1 |
Central, hipotiroidismo |
Pérdida de función ligada al cromosoma X |
Pérdida de la expresión del receptor de TSH (TSH-R), agrandamiento de testículos |
TSHβ |
Central, hipotiroidismo |
Pérdida de función heterocigota |
Deficiencia de TSH |
TTF-1 (TITF-1) |
Primario, disgenesia tiroidea |
Pérdida de función heterocigota |
Hipoplasia tiroidea variable, coreoatetosis, problemas pulmonares |
TTF-2 (FOXE-1) |
Primario, disgenesia tiroidea |
Homocigoto recesivo |
Agenesia tiroidea, atresia de coanas, pelo erizado |
PAX-8 |
Primario, disgenesia tiroidea |
Pérdida de función heterocigota |
Disgenesia tiroidea, anormalidades renales |
NKX2–1 |
Primario, disgenesia tiroidea |
Pérdida de función heterocigota |
Disgenesia tiroidea, anormalidades cerebrales y pulmonares |
NKX2–5 |
Primario, disgenesia tiroidea |
Pérdida de función heterocigota |
Disgenesia tiroidea, anormalidades cardiacas |
GLIS3 |
Primario, disgenesia tiroidea |
Homocigoto recesivo |
Disgenesia tiroidea, diabetes neonatal, anormalidades faciales |
JAG-1 |
Primario, disgenesia tiroidea |
Pérdida de función heterocigota |
Disgenesia tiroidea, síndrome de Alagille tipo 1, anormalidades cardiacas |
Receptor de TSH |
Primario, disgenesia tiroidea y trastornos en la producción de hormonas |
Homocigoto recesivo |
Resistencia a la TSH |
Gsα (osteodistrofia hereditaria de Albright) |
Primario, trastornos en la producción de hormonas tiroideas |
Pérdida de función heterocigota, sellado genómico |
TSH resistance |
Cotransportador unidireccional Na+/I− symporter (SLC5A5) |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Incapacidad para transportar yoduro |
DUOX2 (THOX2) |
Primario, trastornos en la producción de hormonas tiroideas |
Pérdida de función heterocigota |
Defecto de la organificación |
DUOXA2 |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Defecto de la organificación |
Peroxidasa tiroidea |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Organificación defectuosa del yoduro |
Tiroglobulina |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Síntesis defectuosa de la hormona tiroidea |
Pendrina (SLC26A4) |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Síndrome de Pendred: hipoacusia neurosensitiva y defecto parcial de la organificación en la glándula tiroides |
Deshalogenasa 1 (IYD) |
Primario, trastornos en la producción de hormonas tiroideas |
Homocigoto recesivo |
Pérdida de la reutilización de yodo |
Cuadro 2. Ejemplos de causas genéticas de hipotiroidismo congénito.
Manifestaciones clínicas
La mayoría de los recién nacidos parece normal al nacer, y con el uso de la detección bioquímica ahora pocos casos se diagnostican con base en manifestaciones clínicas, que incluyen ictericia prolongada, problemas para la alimentación, hipotonía, macroglosia, retraso en la maduración ósea y hernia umbilical. Es importante destacar que si el tratamiento se retrasa, se produce daño neurológico permanente. También pueden aparecer las características típicas del hipotiroidismo del adulto (cuadro 3). Otras malformaciones congénitas, especialmente cardiacas, son cuatro veces más frecuentes en el hipotiroidismo congénito.
Síntomas |
Signos |
Cansancio, debilidad Sequedad de piel Sensación de frio Caída del pelo Dificultad para concentrarse y mala memoria Estreñimiento Aumento de peso y escaso apetito Disnea Voz ronca Menorragia (mas adelante oligomenorrea o amenorrea) Parestesias Déficit auditivo |
Piel seca y áspera; extremidades periféricas frías Cara, manos y pies hinchados (mixedema) Alopecia difusa Bradicardia Edema periférico Retraso de la relajación de los reflejos tendinosos Síndrome del túnel carpiano Derrames de cavidades serosas |
Cuadro 3. Signos y síntomas del hipotiroidismo (en orden descendente de frecuencia)
Diagnóstico y tratamiento
Por las graves consecuencias neurológicas del hipotiroidismo congénito no tratado, se han establecido programas de detección sistemática neonatal. Estos suelen basarse en la cuantificación de las concentraciones de TSH o de T4 en muestras de sangre obtenidas por punción del talón. Cuando se confirma el diagnóstico, se administra T4 en una dosis de 10 a 15 mcg/kg/día y la dosis se ajusta por medio de vigilancia de las concentraciones de TSH. Las necesidades de T4 son relativamente altas durante el primer año de vida y suele requerirse una concentración circulante elevadas para normalizar la TSH. El tratamiento precoz con T4 resulta en niveles normales de IQ, pero pueden producirse anormalidades sutiles del neurodesarrollo en aquellos con el hipotiroidismo más grave en el momento del diagnóstico o cuando el tratamiento se retrasa o es subóptimo. Si se sospecha hipotiroidismo transitorio o si el diagnóstico no está claro, es seguro detener el tratamiento después de los tres años de edad y continuar la valoración.
Hipotiroidismo autoinmunitario
Clasificación
El hipotiroidismo autoinmunitario (tiroiditis de Hashimoto) puede estar asociado a bocio (tiroiditis nitrópica) o a un tejido tiroideo residual mínimo (tiroiditis atrófica). Como el proceso autoinmunitario reduce gradualmente la función tiroidea, existe una fase de compensación durante la cual las concentraciones de hormonas tiroideas se mantienen por medio de una elevación de la TSH. Aunque algunos pacientes pueden presentar síntomas leves, esta fase recibe el nombre de hipotiroidismo subclínico. Más adelante, las concentraciones de T4 no ligada disminuyen y las de TSH se incrementan aún más; los síntomas se hacen mucho más evidentes en esta fase (habitualmente TSH > 10 mUI/L), que se denomina hipotiroidismo clínico o hipotiroidismo manifiesto.
Prevalencia
La tasa de incidencia anual media de hipotiroidismo autoinmunitario es de 4 por 1 000 mujeres y 1 por 1 000 varones. Es más frecuente en algunas poblaciones, como la japonesa, probablemente como consecuencia de factores genéticos y la exposición prolongada a una dieta con alto contenido de yodo. El hipotiroidismo suele aparecer entre los 30 y los 50 años, y su prevalencia aumenta con la edad. El promedio de edad en el momento del diagnóstico es de 60 años, y la prevalencia del hipotiroidismo manifiesto aumenta con la edad. Se detecta hipotiroidismo subclínico en 6% a 8% de las mujeres (10% alrededor de los 60 años) y 3% de los varones. El riesgo anual de desarrollar hipotiroidismo clínico es cercano al 4%, cuando el hipotiroidismo subclínico se relaciona anticuerpos positivos contra la peroxidasa tiroidea (TPO, tiroperoxidasa).
Patogenia
En la tiroiditis de Hashimoto existe una infiltración linfocítica marcada de la glándula tiroides con formación de centros germinales, atrofia de folículos tiroideos acompañada de metaplasia oxífila, ausencia de coloide y fibrosis leve o moderada. En la tiroiditis atrófica, la fibrosis es mucho más extensa, la infiltración linfocítica es menos pronunciada y los folículos tiroideos faltan casi por completo. La tiroiditis atrófica casi siempre representa la etapa final de la tiroiditis de Hashimoto, no un trastorno separado, aunque existe una forma distintiva de fibrosis marcada en la que la glándula se infiltra con células plasmáticas positivas para IgG4.
Como sucede con la mayoría de los trastornos autoinmunitarios, la susceptibilidad a hipotiroidismo autoinmunitario se establece por una combinación de factores genéticos y ambientales, y el riesgo de hipotiroidismo autoinmunitario o de enfermedad de Graves está aumentado entre hermanos. Los polimorfismos HLA-DR son los factores de riesgo genéticos mejor documentados para el hipotiroidismo autoinmunitario, especialmente HLA-DR3, DR4 y DR5 en caucásicos. Existe también una relación débil entre los polimorfismos en PTPN22 y CTLA-4, que tienen funciones inmunorreguladoras e hipotiroidismo autoinmunitario. Todas estas relaciones genéticas son compartidas por otras enfermedades autoinmunitarias, lo que podría explicar la relación entre hipotiroidismo autoinmunitario y otras enfermedades autoinmunitarias, en particular diabetes mellitus tipo 1, enfermedad de Addison, anemia perniciosa y vitíligo. Queda por aclarar la paritipación de otros loci contribuyentes. Un gen situado sobre el cromosoma 21 podría ser el causante de la relación entre el hipotiroidismo autoinmunitario y el síndrome de Down. La preponderancia femenina de la autoinmunidad tiroidea se debe, con mayor probabilidad, a los efectos de los esteroides sexuales sobre la reacción inmunitaria, pero es también posible que exista un factor genético relacionado con el cromosoma X, que explicaría la gran frecuencia de hipotiroidismo autoinmunitario en el síndrome de Turner. Los factores de susceptibilidad ambiental están mal definidos en la actualidad. El consumo alto de yodo o deficiente de selenio y la menor exposición a microorganismos en la infancia incrementa el riesgo de hipotiroidismo autoinmunitario. La suspensión del tabaquismo produce un aumento transitorio de la incidencia, mientras que el consumo de alcohol parece protector. Estos factores pueden explicar el incremento en la prevalencia en las últimas dos o tres décadas.
El infiltrado linfocítico tiroideo en el hipotiroidismo autoinmunitario está compuesto por linfocitos T activados y linfocitos B. La destrucción de las células tiroideas está mediada sobre todo por los linfocitos T citotóxicos CD8+, pero la producción local de citocinas, como el factor de necrosis tumoral (TNF, tumor necrosis factor), interleucina-1 (IL-1) e interferón γ (IFN-γ), derivadas del infiltrado inflamatorio puede hacer que las células tiroideas sean más susceptibles a la apoptosis mediada por receptores de la muerte, como Fas y por la agresión oxidativa. Estas citocinas también afectan directamente la función de las células tiroideas e inducen la expresión de otras moléculas proinflamatorias por las propias células tiroideas, como citocinas, moléculas de HLA clases I y II, moléculas de adherencia, CD40 y óxido nítrico. La administración de concentraciones elevadas de citocinas con finalidades terapéuticas (en particular IFN-α) se relaciona con incremento de la enfermedad tiroidea autoinmunitaria, tal vez por mecanismos semejantes a los que participan en la enfermedad esporádica. Los nuevos tratamientos contra el cáncer e inmunomoduladores, como los inhibidores de la tirosina cinasa, inhibidores de puntos de verificación inmunitaria y el alemtuzumab, también pueden inducir tiroiditis a través de sus efectos sobre la regulación de los linfocitos T.
Los anticuerpos contra TPO y tiroglobulina (Tg) son marcadores clínicamente útiles de autoinmunidad tiroidea, pero cualquier efecto patógeno se limita a una participación secundaria al amplificar una respuesta autoinmunitaria en proceso. Los anticuerpos TPO fijan el complemento y los complejos de ataque de membrana del complemento están presentes en la tiroides en el hipotiroidismo autoinmunitario. Sin embargo, el paso transplacentario de anticuerpos contra Tg o TPO carece de efecto sobre la glándula tiroides del feto, lo que sugiere que se requiere una lesión mediada por linfocitos T para iniciar el daño autoinmunitario de la tiroides.
Hasta el 20% de los pacientes con hipotiroidismo autoinmunitario tiene anticuerpos contra el TSH-R, que, a diferencia de la inmunoglobulina estimulante de la tiroides (TSI), no estimula el receptor, pero evita la unión de la TSH. Por tanto, los anticuerpos antagonistas de TSH-R producen hipotiroidismo y, sobre todo en pacientes asiáticos, atrofia tiroidea. Su paso transplacentario puede provocar hipotiroidismo neonatal transitorio. En muy pocas ocasiones, los pacientes tienen una mezcla de anticuerpos antagonistas de TSI y TSH-R, y en ellos la función tiroidea puede oscilar entre hipertiroidismo e hipotiroidismo a medida que uno u otro anticuerpo se vuelve dominante. Es difícil predecir el curso de la enfermedad en estos individuos, y es necesaria la vigilancia estrecha de la función tiroidea. Pueden utilizarse bioanálisis para documentar que los anticuerpos bloqueadores del TSH-R reducen el efecto inductor del AMP cíclico de TSH en células cultivadas que expresan TSH-R, pero estos estudios son difíciles de efectuar. Los inmunoanálisis para anticuerpos del receptor de la TSH, que miden si el suero del paciente contiene un anticuerpo que puede desplazar a la TSH marcada o a un anticuerpo monoclonal del receptor de la TSH del receptor de la TSH, no hacen diferencia entre estos tipos de anticuerpos funcionales, pero un resultado positivo en un paciente con hipotiroidismo espontáneo es fuerte evidencia de la presencia de anticuerpos bloqueadores. El uso de estos análisis no suele alterar el tratamiento médico, aunque pueden ser de utilidad para confirmar la causa del hipotiroidismo neonatal transitorio.
Manifestaciones clínicas
Las principales manifestaciones se resumen en el cuadro 3. El comienzo suele ser insidioso y es posible que el paciente se dé cuenta de sus síntomas únicamente cuando se haya restablecido el eutiroidismo. Los pacientes con tiroiditis de Hashimoto pueden presentar bocio en lugar de síntomas de hipotiroidismo. Aunque el bocio no sea grande, suele ser irregular y de consistencia firme. Es raro que la tiroiditis de Hashimoto no complicada se acompañe de dolor.
Los pacientes con tiroiditis atrófica y los que se encuentran en la fase tardía de la tiroiditis de Hashimoto presentan signos y síntomas de hipotiroidismo. La piel está seca y existe una disminución de la sudoración, adelgazamiento de la epidermis e hiperqueratosis del estrato córneo. El aumento del contenido de glucosaminoglucanos en la dermis atrapa agua, provocando un engrosamiento de la piel sin fóvea (mixedema). Las características típicas son cara hinchada con párpados edematosos y edema pretibial sin fóvea (Fig. 1). Por lo general, se observa palidez con un tinte amarillo en la piel por la acumulación de caroteno. Se retrasa el crecimiento de las uñas y el pelo está seco, quebradizo, difícil de controlar y se cae con facilidad. Además de la alopecia difusa hay adelgazamiento del tercio externo de las cejas, aunque este no es un signo específico de hipotiroidismo.
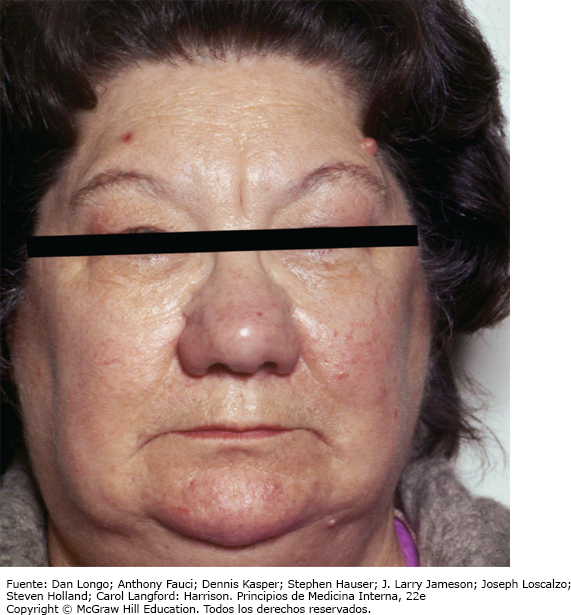
Otras manifestaciones comunes son estreñimiento y aumento de peso (a pesar de tener poco apetito). A diferencia de la creencia popular, el aumento de peso es por lo general moderado y se debe principalmente a retención de líquidos en los tejidos mixedematosos. La libido está disminuida en ambos sexos y puede haber oligomenorrea o amenorrea en la enfermedad de larga duración, pero la menorragia puede ocurrir en una etapa temprana. La fertilidad disminuye y la incidencia de abortos espontáneos aumenta. Las concentraciones de prolactina a menudo presentan una elevación discreta y pueden contribuir a las alteraciones de la libido y la fertilidad, así como provocar galactorrea.
La contractilidad miocárdica y la frecuencia del pulso están disminuidas, lo que causa reducción del volumen sistólico y bradicardia. El aumento de la resistencia periférica puede acompañarse de hipertensión, en especial de tipo diastólico. El flujo sanguíneo se desvía de la piel, provocando frialdad de las extremidades. El 30% de los pacientes sufre derrames pericárdicos que rara vez alteran la función cardiaca. Aunque se han documentado alteraciones en la expresión de la isoforma de las cadenas pesadas de la miosina, la miocardiopatía no es frecuente. El líquido puede acumularse también en otras cavidades serosas y en el oído medio, produciendo sordera de conducción; también puede ocurrir hipoacusia neurosensitiva. La función pulmonar suele ser normal, pero puede ocurrir disnea por derrame pleural, deterioro de la función de los músculos respiratorios, reducción del estímulo ventilatorio o apnea del sueño.
Son frecuentes el síndrome del túnel carpiano y otros síndromes de atrapamiento, al igual que el deterioro de la función muscular, con rigidez, calambres y dolor. En la exploración puede observarse lentitud de relajación de los reflejos tendinosos y seudomiotonía. La memoria y la concentración están deterioradas. De manera experimental, la tomografía por emisión de positrones que examina el metabolismo de la glucosa en sujetos hipotiroideos muestra menor actividad regional en la amígdala, hipocampo y en la corteza cingulada perigenual anterior, entre otras regiones, y esta actividad se corrige después de la sustitución con tiroxina. Los problemas neurológicos rara vez incluyen ataxia cerebelosa reversible, demencia, psicosis y coma mixedematoso. La encefalopatía de Hashimoto se ha definido como un síndrome sensible a los esteroide vinculados con anticuerpos contra TPO, mioclono y una actividad electroencefalográfica de ondas lentas, pero no se ha definido la relación con la autoinmunidad tiroidea o el hipotiroidismo, y si un paciente se encuentra eutiroideo, el tratamiento con levotiroxina (LT4) no ha demostrado ser eficaz. La disfonía y a veces la emisión torpe de palabras en el hipotiroidismo reflejan acumulación de líquidos de las cuerdas vocales y en la lengua.
Las manifestaciones descritas son consecuencia de la deficiencia de hormona tiroidea. No obstante, el hipotiroidismo autoinmunitario puede estar asociado con signos o síntomas de otras enfermedades autoinmunitarias, particularly vitiligo, anemia perniciosa, enfermedad de Addison (síndrome de Schmidt), alopecia areata y diabetes mellitus de tipo 1 (T1DM). En el trastorno poligénico denominado síndrome poliendocrino autoinmunitario tipo 2, está presente la enfermedad tiroidea autoinmunitaria en 70% a 75%, diabetes mellitus tipo 1 en 40% a 60% y enfermedad de Addison en 40 a 50%, de los casos. Asociaciones menos frecuentes incluyen enfermedad celiaca, dermatitis herpetiforme, hepatitis crónica activa, artritis reumatoide, lupus eritematoso generalizado (LES, lupus eritematoso sistémico), miastenia grave, hipoparatiroidismo autoinmunitario, hipogonadismo primario y síndrome de Sjögren. La oftalmopatía asociada con enfermedad tiroidea suele aparecer en la enfermedad de Graves, pero en casi 5% de los pacientes se relaciona con hipotiroidismo autoinmunitario.
El hipotiroidismo autoinmunitario es infrecuente en niños y por lo general se presenta con crecimiento lento y retraso en la maduración facial y dental. La hipófisis puede estar agrandada debido a la hiperplasia tirotrópica. La miopatía, con inflamación muscular, es más frecuente en niños que en adultos. En gran parte de los casos se retrasa la pubertad, aunque en ocasiones existe pubertad precoz. Puede haber afección intelectual si el trastorno se inicia antes de los tres años de edad y la deficiencia hormonal es severe.
Valoración de laboratorio
En la figura 2 se ofrece un resumen de las investigaciones utilizadas para establecer la existencia y causa del hipotiroidismo. Una concentración normal de TSH excluye el hipotiroidismo primario (pero no el secundario o central). Si la TSH está elevada, se necesita una concentración de T4 libre o no ligada (FT4) para confirmar la presencia de hipotiroidismo clínico, pero cuando la T4 se utiliza como prueba de cribado es inferior a la TSH porque no detectará el hipotiroidismo subclínico. Las concentraciones de T3 libre circulante son normales en casi 25% de los pacientes, hecho que refleja las respuestas adaptativas de las desyodasas al hipotiroidismo. Por lo tanto, no están indicadas las mediciones de T3.
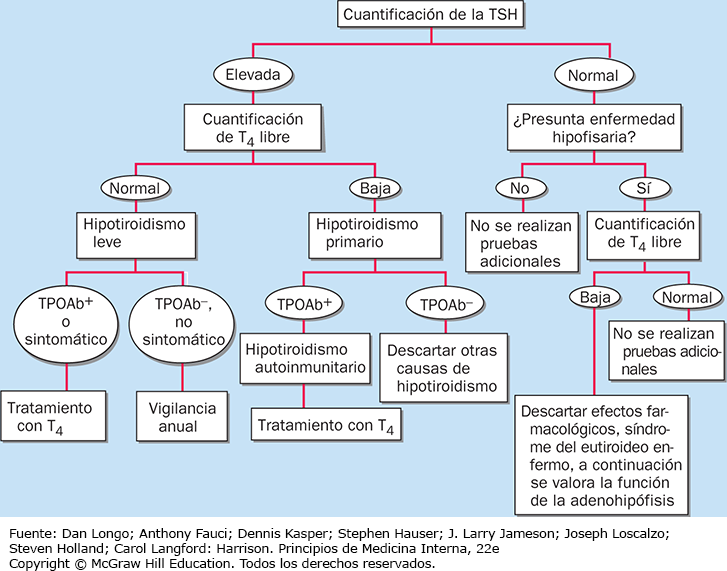
Una vez que se confirma el hipotiroidismo subclínico, casi siempre es fácil establecer la etiología al demostrar la presencia de anticuerpos contra TPO y Tg, que están presentes en más de 95% de los pacientes con hipotiroidismo autoinmunitario. Otros datos anormales de laboratorio en el hipotiroidismo pueden incluir aumento de la creatina fosfocinasa, elevación del colesterol y triglicéridos, y anemia (habitualmente normocítica o macrocítica) dependiendo del grado y duración del hipotiroidismo. Con la sustitución de tiroxina se resuelven gradualmente la anemia y otras anomalías, excepto cuando se acompaña de deficiencia de hierro o de B12 por anemia perniciosa concomitante.
Diagnóstico diferencial
Un bocio asimétrico en la tiroiditis de Hashimoto puede confundirse con un bocio multinodular (MNG, multinodular goiter) o con un carcinoma de tiroides, en el cual los anticuerpos tiroideos también pueden estar presentes. El linfoma primario de tiroides es poco frecuente, pero está fuertemente relacionado con tiroiditis autoinmunitaria preexistente. La ecografía puede mostrar la presencia de nódulos solitarios o múltiples en lugar del agrandamiento tiroideo con ecogenicidad heterogénea típico de la tiroiditis de Hashimoto. Sin embargo, las imágenes ecográficas también pueden detectar pseudonódulos, zonas hipoecoicas que probablemente representen áreas de infiltrados linfocíticos, que deben distinguirse de los verdaderos nódulos superpuestos, ya que en estos casos no se justifica la aspiración con aguja fina. La biopsia por aspiración con aguja fina (PAAF) debe realizarse en todos los nódulos verdaderos que cumplan los criterios de PAAF. Se revisan a continuación otras causas de hipotiroidismo y en el cuadro 1, pero rara vez causan confusión diagnóstica.
Otras causas de hipotiroidismo
El hipotiroidismo yatrógeno es una causa frecuente de hipotiroidismo y con frecuencia se diagnostica por detección, antes del desarrollo de los síntomas. En los primeros tres o cuatro meses después del tratamiento con yodo radiactivo para la enfermedad de Graves, puede haber hipotiroidismo transitorio por el daño reversible secundario a la radiación. Cuando el paciente se recupera puede retirarse el tratamiento con tiroxina en dosis bajas. Como las concentraciones de TSH están suprimidas por el hipertiroidismo, las concentraciones de T4 libre son mejores indicadores de la función tiroidea que la TSH en los meses siguientes al tratamiento con yodo radiactivo. El hipotiroidismo leve luego de tiroidectomía subtotal o lobectomía también puede resolverse después de varios meses, ya que la glándula remanente es estimulada por el aumento de las concentraciones de TSH.
La deficiencia de yodo es la causa del bocio endémico y del cretinismo, pero es una causa poco frecuente de hipotiroidismo del adulto, a menos que la ingesta de yodo sea muy baja o existan factores de complicación, como el consumo de tiocianatos de yuca o déficit de selenio. Aunque el hipotiroidismo secundario a deficiencia de yodo se puede tratar con tiroxina, para eliminar este problema se debe abogar por medidas de salud pública que mejoren la ingesta de yodo. Se han utilizado con éxito la sal o el pan yodados o un único bolo de aceite yodado oral o intramuscular.
De forma paradójica, el exceso crónico de yodo también puede inducir bocio e hipotiroidismo. Los acontecimientos intracelulares que causan este efecto no se conocen con exactitud, pero los sujetos con tiroiditis autoinmunitaria son especialmente vulnerables. El exceso de yodo causa el hipotiroidismo que aparece en pacientes tratados con amiodarona. Otros fármacos, en especial el litio, también pueden causar hipotiroidismo. La causa del hipotiroidismo transitorio puede ser la tiroiditis.
El hipotiroidismo secundario o central suele diagnosticarse en el contexto de otras deficiencias de hormonas hipofisarias; el déficit aislado de TSH es muy raro. Las concentraciones de TSH pueden ser bajas, normales, o incluso estar ligeramente aumentadas en el hipotiroidismo secundario; esto último se debe a la secreción de formas inmunoactivas pero bioinactivas de TSH. El diagnóstico se confirma detectando una baja concentración de T4 libre. El objetivo del tratamiento consiste en mantener las concentraciones de T4 libre en la mitad superior del intervalo de referencia, ya que las concentraciones de TSH no se pueden utilizar para vigilar el tratamiento.
Tratamiento del hipotiroidismo
Hipotiroidismo Clínico
Si no existe función tiroidea residual, la dosis de sustitución diaria de LT4 suele ser de 1.6 mcg/kg de peso corporal (normalmente 100 a 150 mcg), idealmente ingeridas al menos 30 min antes del desayuno. No obstante, en muchos pacientes basta con administrar dosis menores hasta que se destruya el tejido tiroideo residual. En los pacientes en quienes se desarrolla hipotiroidismo tras el tratamiento de la enfermedad de Graves a menudo existe una función autónoma subyacente, que requiere dosis de sustitución más bajas (normalmente 75 a 125 mcg/día).
Los pacientes adultos < 60 años sin signos de cardiopatía pueden comenzar el tratamiento con 50 a 100 mcg de LT4 al día. La dosis se ajusta en función de las concentraciones de TSH, y el objetivo del tratamiento será una TSH normal, idealmente en la mitad inferior del rango de referencia. Las respuestas de TSH son graduales y deben medirse seis a ocho semanas después de instituir el tratamiento o después de cualquier cambio posterior en la dosis de LT4. Los efectos clínicos de la administración de LT4 toman tiempo en aparecer. Es posible que los pacientes no experimenten un alivio completo de los síntomas hasta varios meses después de que se hayan restablecido las concentraciones normales de TSH. El ajuste de la dosis de LT4 se realiza en incrementos de 12.5 o 25 mcg si la TSH es alta; si la TSH está suprimida deben realizarse disminuciones de la misma magnitud. Los pacientes con supresión de TSH por cualquier causa, incluido el tratamiento excesivo con LT4, presentan mayor riesgo de fibrilación auricular y de reducción de la densidad ósea.
Alrededor de 10% a 15% de los pacientes pueden tener síntomas persistentes a pesar de la restauración del eutiroidismo con LT4 por razones que aún no están claras. Aunque existen preparados desecados de tiroides animal (extracto de tiroides USP), no se recomiendan porque la proporción de T3 a T4 no es fisiológica. Se ha investigado el uso de LT4 combinado con liotironina (triyodotironina, T3), pero no se ha confirmado su beneficio en estudios prospectivos. No hay lugar para la liotironina sola como reemplazo a largo plazo, porque la semivida corta requiere tres o cuatro dosis diarias y se asocia con concentraciones fluctuantes de T3.
Una vez que se logra el reemplazo completo y las concentraciones de TSH son estables, se recomienda hacer cuantificaciones anuales de TSH de seguimiento. Es importante asegurar una adherencia continua ya que los pacientes no sienten ninguna diferencia sintomática después de omitir algunas dosis de LT4, y esto a veces conduce a la auto-interrupción.
En pacientes con peso corporal normal que toman ≥ 200 mcg de LT4 al día, una concentración elevada de TSH a menudo es un signo de mal apego terapéutico. Esta es también la explicación probable de las fluctuaciones en la concentración de TSH, a pesar de una dosis constante de LT4. Estos pacientes a menudo have concentraciones normales o elevadas de T4 libre, pese a la elevación de la TSH, porque recuerdan tomar la medicación unos días antes de las pruebas, y esas dosis son suficientes para normalizar la T4, pero no las concentraciones de TSH. Es importante tener en cuenta adherencia variable ya que este perfil de las pruebas de función tiroidea es por lo demás, segetivo de trastornos relacionados con secreción inadecuada de TSH. Como la T4 tiene una semivida larga (siete días), a los pacientes que se salten una dosis se les puede aconsejar que tomen dos dosis de los comprimidos saltados a la vez. Es preciso descartar otras causas de aumento en los requerimientos de LT4, en particular la malabsorción (p. ej., enfermedad celiaca, cirugía de intestino delgado, gastritis atrófica o relacionada con Helicobacter pylori), medicamentos orales que contienen estrógenos o tratamiento modulador selectivo del receptor estrogénico, ingestión con una comida y fármacos que interfieren con la absorción o el metabolismo de T4, como los secuestradores de ácidos biliares, sulfato ferroso, complementos de calcio, selevamer, sucralfato, inhibidores de la bomba de protones, lovastatina, hidróxido de aluminio, rifampicina, amiodarona, carbamazepina, fenitoína e inhibidores de la tirosina cinasa.
Hipotiroidismo subclínico
Se refiere a la evidencia bioquímica de deficiencia de hormona tiroidea en pacientes que tienen pocas o ninguna manifestación clínica aparente de hipotiroidismo. No hay recomendaciones aceptadas universalmente del tratamiento del hipotiroidismo subclínico, pero la LT4 se recomienda si la paciente es una mujer que desea concebir o está embarazada, o cuando las concentraciones de TSH son > 10 mUI/L. La mayoría de los demás pacientes pueden simplemente someterse a un seguimiento anual. Cuando un paciente joven o de mediana edad tiene síntomas de hipotiroidismo o riesgo de cardiopatía, se considera un régimen terapéutico. Es importante confirmar que cualquier incremento de TSH se mantiene durante un periodo de tres meses antes de administrar el tratamiento; este se administra comenzando con una dosis baja de LT4 (25 a 50 mcg/día) con el objetivo de normalizar la TSH.
Consideraciones de tratamiento especial
Rara vez la sustitución con LT4 se relaciona con un seudotumor cerebral en los niños. La presentación parece ser idiosincrásica y ocurre meses después de iniciado el tratamiento.
Como el hipotiroidismo materno puede afectar de forma negativa el desarrollo neural del feto y relacionarse con resultados gestacionales adversos (aborto, parto prematuro), es preciso vigilar la función tiroidea para conservar el eutiroidismo en las mujeres con antecedente o riesgo alto de hipotiroidismo. Aunque los estudios epidemiológicos han demostrado la relación del aborto y el patrto prematuro con la presencia de autoanticuerpos tiroideos detectados durante o antes de la gestación en mujeres eutiroideas, los estudio multicéntricos con asignación al azar y grupo testigo que valoran el tratamiento con LT4 antes de la concepción en esta población no han demostrado beneficios. Debido al aumento conocido de las necesidades de hormonas tiroideas durante el embarazo en mujeres hipotiroideas, el tratamiento con LT4 debe enfocarse en mantener la TSH sérica en el rango normal, pero < 2.5 mIU/L antes de la concepción.
En mujeres sin evidencia de disfunción tiroidea, la TSH sérica disminuye a finales del primer trimestre, y si no se dispone de rangos específicos para el trimestre, se puede aproximar un rango apropiado para las semanas siete a 12 de gestación, al disminuir el límite superior del rango de referencia de no embarazadas en 0.5 mUI/L (casi 4.0 mUI/L) y el límite inferior en 0.4 mUI/L (casi 0.1 mUI/L). Sin embargo, es importante reconocer que el rango normal de TSH en el embarazo para el segundo y tercer trimestre no es significativamente diferente del rango de referencia sin embarazo. Por lo tanto, cuando se atienda a mujeres con hipotiroidismo que consumen LT4, la función tiroidea debe valorarse de inmediato después de confirmarse el embarazo y luego cada cuatro semanas durante la primera mitad del embarazo, con pruebas menos frecuentes después de las 20 semanas de gestación (cada seis a ocho semanas dependiendo de si se está ajustando la dosis de LT4). El aumento de la dosis de LT4 depende de la causa del hipotiroidismo, y las mujeres atireóticas requieren más (casi 45%) que aquellas con tiroiditis de Hashimoto que pueden tener alguna función tiroidea residual. Las pacienetes deben incrementar la LT4 de una dosis diaria a nueve dosis por semana en cuanto se confirme el embarazo a fin de anticipar este cambio. A partir de entonces, la dosis debe vigilarse estrechamente con un objetivo de TSH en la mitad inferior del intervalo normativo específico del trimestre, si está disponible, o < 2,5 mUI/L, que permita una reserva si se requieren aumentos adicionales de la dosis de LT4 a medida que avanza el embarazo. Después del parto, las dosis de LT4 típicamente regresan a las concentraciones antes del embarazo. Se debe instruir a las mujeres pregnant que separen la ingestión de vitaminas prenatales y complementos de hierro de la LT4.
En pacientes mayores pueden requerirse 20% menos tiroxina que en las más jóvenes. En pacientes de edad avanzada, en especial en pacientes con enfermedad arterial coronaria conocida, la dosis inicial de LT4 es de 12.5 a 25 mcg/día, con incrementos similares cada dos a tres meses hasta que se normalice la TSH. En algunos pacientes puede ser imposible lograr la sustitución total, a pesar de un tratamiento antianginoso óptimo. La cirugía urgente suele ser segura en los pacientes con hipotiroidismo no tratado, aunque la cirugía rutinaria en un paciente hipotiroideo debe aplazarse hasta que se alcance el estado eutiroideo.
El coma mixedematoso sigue teniendo una tasa de mortalidad de 20 a 40% a pesar del tratamiento intensivo, y los desenlaces son independientes de las concentraciones de T4 y TSH. Las manifestaciones clínicas consisten en disminución del estado de conciencia, en ocasiones relacionado con convulsiones, así como las demás características del hipotiroidismo (cuadro 3). La hipotermia puede alcanzar los 23°C (74°F). Puede haber antecedentes de hipotiroidismo tratado con poco cumplimiento, o el paciente pudo no haberse diagnosticado antes. El coma mixedematoso ocurre casi siempre en el anciano y suele desencadenarse por factores que alteran la respiración, como fármacos (especialmente sedantes, anestésicos y antidepresivos), neumonía, insuficiencia cardiaca congestiva, infarto del miocardio, hemorragia gastrointestinal o apoplejía. También debe sospecharse la existencia de septicemia. La exposición al frío también puede ser un factor de riesgo. La hipoventilación, que conduce a hipoxia y a hipercapnia, desempeña un papel importante en la patogenia; la hipoglucemia y la hiponatremia por dilución también pueden contribuir al desarrollo de coma mixedematoso.
Al inicio, la LT4 puede administrarse como bolo IV único de 200 a 400 mcg, lo cual sirve como dosis de carga, seguido de una dosis VO diaria de 1.6 mcg/kg al día, reducida en 25% si se administra por vía IV. Si no se dispone de un preparado intravenoso adecuado, la misma dosis inicial de LT4 puede administrarse por sonda nasogástrica (aunque la absorción puede estar deteriorada en el mixedema). Como la conversión T4→T3 está alterada en el coma mixedematoso, es razonable agregar liotironina (T3) intravenosa o por sonda nasogástrica al régimen de LT4, aunque el exceso de liotironina tiene la capacidad para causar arritmias. Una dosis de carga inicial de 5 a 20 mcg de liotironina debe ir seguida por 2.5 a 10 mcg cada 8 h, con dosis más bajas en casos de pacientes pequeños o mayores o con riesgo cardiovascular.
Se proporciona tratamiento de sostén para corregir cualquier alteración metabólica. El calentamiento externo está indicado únicamente si la temperatura es inferior a 30 °C, ya que puede provocar colapso cardiovascular. Deben utilizarse mantas espaciales para evitar una mayor pérdida de calor. Se administra hidrocortisona parenteral (50 mg cada 6 h) porque hay una reserva suprarrenal alterada en el hipotiroidismo profundo. Se trata cualquier factor precipitantes, incluido el uso precoz de antibióticos de amplio espectro, hasta descartar la infección. El apoyo ventilatorio con análisis periódico de gases en sangre suele ser necesario en las primeras 48 h. Si existe hiponatremia o hipoglucemia grave se administra solución salina hipertónica o glucosa intravenosa; los líquidos intravenosos hipotónicos deben evitarse, ya que pueden exacerbar la retención de agua secundaria a reducción de la perfusión renal y a la secreción inadecuada de vasopresina. El metabolismo de la mayor parte de los fármacos está deteriorado, y si es posible, se evitan los sedantes o se administran en dosis reducidas. Se documentan las concentraciones de fármacos en sangre, para orientar la dosificación.