Introducción
El primer cateterismo cardíaco fue realizado en 1920 por el doctor Werner Forssmann a través de la introducción de una sonda urológica en la vena antecubital hasta la aurícula derecha. Posteriormente se realizaron rutinariamente cateterismos con dispositivos semirrígidos, y en 1953 Lategola y Rahn innovaron por experimentación animal, un sistema de catéter con balón para facilitar el uso de cateterismo derecho y pulmonar sin fluoroscopia asistida. En 1970 Harold James Swan y William Ganz, como resultado de la serendipia y basados en los antecedentes descritos, crearon el sistema de catéter flexible con balón distal inflable en humanos teniendo como motivación el desarrollo de una técnica para el cuidado y estudio de pacientes cardiópatas agudos en quienes la fluoroscopia no estaba disponible o se encontraban en condiciones de inamovilidad por inestabilidad hemodinámica u otras causas.
El cateterismo de arterial pulmonar (CAP) por catéter Swan-Ganz (CSG) fue considerado un método revolucionario en su momento; sin embargo, en años subsiguientes, con el avance de técnicas diagnósticas y terapéuticas, tuvo un declive en su uso. En la última década su utilidad volvió a tener protagonismo como monitoreo invasivo hemodinámico en pacientes con falla cardiaca, asociado a una disminución de la mortalidad y un aumento de la estancia hospitalaria. Asimismo, su uso ha tomado relevancia en pacientes con choque cardiogénico (CC) hospitalizados en unidades de cuidado intensivo.
Historia
El primer cateterismo cardíaco en humanos fue realizado por el médico alemán Werner Forssmann en 1929. Forssmann, entonces un joven radiólogo, llevó a cabo el procedimiento en sí mismo en el hospital de Eberswalde, Alemania. Desafiando la desaprobación de sus superiores, convenció a una enfermera para que le ayudara, aunque finalmente la engañó haciéndole creer que el procedimiento sería en ella, cuando en realidad se lo practicó a sí mismo.
Forssmann se anestesió el brazo, realizó una incisión en la vena antecubital izquierda e introdujo un catéter urinario de 65 cm, avanzándolo hasta la aurícula derecha bajo control radiológico. Posteriormente, se dirigió al departamento de radiología para registrar con rayos X la posición del catéter en su corazón.
Este acto, considerado temerario en su momento, le costó la expulsión del hospital, pero sentó las bases para el desarrollo de una técnica que revolucionaría la cardiología. Inicialmente, el objetivo de Forssmann no era estudiar el corazón, sino demostrar que era posible administrar medicamentos directamente en el órgano de manera segura.
El trabajo de Forssmann fue ignorado durante años, hasta que en la década de 1940 André Cournand y Dickinson Richards, en Estados Unidos, perfeccionaron la técnica y demostraron su utilidad clínica para medir presiones intracardíacas y estudiar enfermedades pulmonares y cardíacas. Por este avance, Forssmann, Cournand y Richards recibieron el Premio Nobel de Fisiología o Medicina en 1956.
Antecedentes y evolución:
✅ 1733: Stephen Hales realizó el primer cateterismo cardíaco en animales, midiendo la presión sanguínea en un caballo.
✅ Siglo XIX: Claude Bernard y otros investigadores avanzaron en el registro de presiones intracardíacas en animales.
✅ 1929: Forssmann realizó el primer cateterismo cardíaco en humanos.
✅ Década de 1940: Cournand y Richards estandarizaron el procedimiento para estudios fisiopatológicos en humanos.
✅ 1950: Henry Zimmerman realizó el primer cateterismo cardíaco izquierdo en humanos.
El cateterismo cardíaco se consolidó como una herramienta diagnóstica y terapéutica esencial en la cardiología moderna, permitiendo desde la evaluación anatómica y funcional del corazón hasta el tratamiento de enfermedades coronarias mediante técnicas intervencionistas como la angioplastia y la colocación de stents
El catéter de Swan-Ganz, también conocido como catéter de arteria pulmonar, fue inventado en 1967 por los doctores Jeremy Swan y William Ganz en el Cedars-Sinai Medical Center de Los Ángeles. Este dispositivo revolucionó el monitoreo hemodinámico en pacientes críticos al permitir la medición directa de presiones intracardíacas y parámetros fundamentales para el manejo clínico.
La historia detrás de su creación tiene una curiosa y célebre anécdota relacionada con los veleros. Jeremy Swan, tras un procedimiento particularmente difícil de cateterismo, observó los barquitos de vela en la playa de Santa Mónica. Se imaginó lo sencillo que sería dirigir el catéter dentro del torrente sanguíneo si pudiera «navegar» como un velero, dejándose llevar por la corriente sanguínea en vez de forzarlo manualmente a través de los vasos, como se hacía con los catéteres rígidos de la época.
Esta observación llevó a Swan a idear un catéter flexible con un pequeño balón inflable en la punta. Al inflarse, el balón permitía que el catéter «flotara» y fuera arrastrado por la corriente sanguínea hasta la arteria pulmonar y poder estimar la presión de fin de diástole del ventrículo izquierdo, de manera similar a cómo el viento impulsa a un velero. William Ganz contribuyó perfeccionando el diseño y añadiendo el método de termodilución para medir el gasto cardíaco, lo que consolidó la utilidad del dispositivo.
“Realmente fue Swan el que ideó este método, observando los barquitos de vela en la playa de Santa Mónica, un día después de haber realizado un cateterismo especialmente difícil: se imaginó lo sencillo que sería dirigir el catéter si pudiera navegar como un barco en el torrente circulatorio. Ganz le ayudaría a sustituir su idea del barco por un pequeño balón hinchable…”
El diseño inspirado en los veleros permitió:
✅ Disminuir el tiempo y la dificultad del procedimiento de cateterismo.
✅ Reducir complicaciones asociadas a los catéteres rígidos.
✅ Realizar el procedimiento sin necesidad de fluoroscopía, facilitando su uso en pacientes inestables o en la cabecera del paciente.
El catéter de Swan-Ganz se convirtió en una herramienta fundamental en la medicina intensiva y cardiología, y su origen náutico sigue siendo un ejemplo de cómo la observación cotidiana puede inspirar grandes avances médicos.
Concepto
El catéter de arteria pulmonar es un catéter dirigido por flujo con punta de balón que permite un acceso rápido a la circulación venosa central, al corazón derecho y a la arteria pulmonar (AP). Su longitud es de aproximadamente 110 cm, con un diámetro externo estándar de 7 o 7,5 French. El balón en la punta, cuando se infla, guía el catéter desde las venas intratorácicas mayores a través de la aurícula derecha (AD) y las cámaras ventriculares hacia la AP. La mayoría tiene cuatro lúmenes separados, cada uno de los cuales tiene funciones individuales:
✅ El lumen proximal (azul) se encuentra en la AD y mide la presión intraauricular. También se puede utilizar para administrar medicamentos.
✅ El lumen distal (amarillo) se encuentra en el extremo distal y reside en la AP. Se utiliza para controlar las presiones y para obtener una muestra venosa mixta.
✅ El puerto rojo es para inflar y desinflar el balón. Cada catéter está acompañado de una jeringa de 1,5 mL que se utiliza para inflar el balón.
✅ El sensor de temperatura (termistor) se usa para medir la temperatura central en la AP.
El objetivo del CAP es la monitorización hemodinámica y sus parámetros fisiológicos derivados de la evaluación de la función ventricular izquierda y derecha. La técnica de termodilución que calcula el gasto cardiaco (GC) mide la variabilidad de temperatura sanguínea de la AP y la de la solución salina inyectada por AD que produce un cambio de resistencia y voltaje generando una curva de tiempo-temperatura a partir de la cual se estima el GC mediante la ecuación de Stewart Hamilton. Si el área bajo la curva es pequeña, la temperatura se equilibra rápidamente con la temperatura corporal ambiental lo que indica un GC alto, y si el área bajo la curva es grande implica un GC bajo.
Termodilucion transpulmonar
Para simplificar y reducir la manipulación de la monitorización, la investigación condujo al desarrollo de un dispositivo basado en la técnica de la termodilución transpulmonar (TDTP) con un solo indicador térmico. El GC intermitente se mide utilizando una técnica de termodilución transpulmonar también basada en la ecuación de Stewart-Hamilton:
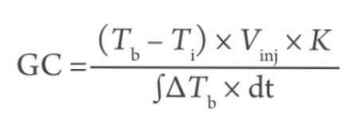
donde Tb es la temperatura de la sangre, Ti es la temperatura del inyectado, Vinj es el volumen del inyectado, K es la constante de corrección y la integral de ∆Tdt (área bajo la curva de la termodilución). El primer dispositivo disponible en el mercado que utilizó la termodilución transpulmonar fue el sistema PICCO (PULSION Medical Systems, Feldkirchen, Alemania, más tarde integrado en Maquet, Rastatt, Alemania, y ahora en Getinge, Gotemburgo, Suecia). El dispositivo PiCCO permite la medición del VGFD y el volumen sanguíneo intratorácico (VSIT), con un VSIT = 1,25 x VGFD como marcadores equivalentes de la precarga junto con el agua pulmonar extravascular (APEV) y el índice de permeabilidad vascular pulmonar (IPVP). La obtención del APEV por termodilución transpulmonar simple depende de la medición del volumen térmico intratorácico (VTIT) y el volumen térmico pulmonar (VTP), que es el volumen accesible más grande por el cual transita el indicador térmico. El VTIT y el VTP se calculan a partir del tiempo medio de tránsito (TMT) y el tiempo de la pendiente exponencial (DST) de la curva de termodilución del indicador inyectado frío:
VTIT=GCx TMT
VTP=GCX DST
El VTIT consiste en el VTP y la suma de los volúmenes al final de la diástole de todas las cámaras cardíacas. En consecuencia, el volumen global al final de la diástole (VGFD) se puede calcular como:
VGFD=VTIT – VTP
Con base en la relación lineal mencionada anteriormente entre el VGFD y el VSIT, el APEV se puede calcular de la siguiente manera:
VSIT = 1,25 x VGFD
APEV = VTIT – VSIT
En la siguiente figura se muestra esquemáticamente los diferentes índices volumétricos y cómo están conectados/correlacionados entre sí. Recientemente, Edwards Lifesciences (Irvine, California, EE. UU.) ha desarrollado un sistema alternativo para la termodilución transpulmonar, que consiste en el VolumeView, un catéter arterial con un termistor en la punta y el software/ plataforma de monitorización EV1000. El concepto es muy similar a la técnica de la TDTP empleada por el sistema PiCCO, como se discutió anteriormente; ambos usan la ecuación de Stewart-Hamilton para calcular el GC derivado de la termodilución. Sin embargo, para calcular el VGFD, el sistema VolumeView/EV1000 utiliza una fórmula implementando la pendiente ascendente máxima (S1) y la pendiente descendente máxima (S2) de la curva de termodilución, mientras que el sistema PiCCO emplea constantes de tiempo derivadas de la apariencia media, el tiempo medio de tránsito, y la pendiente exponencial de la curva de termodilución:
VGFD VolumeView = GCx TMT x f (S1/S2)
donde TMT es el tiempo medio de transito, S1 es la pendiente ascendente maxima y S2 es la pendiente descendente maxima. El APEV se calcula utilizando la misma formula de la PiCCO.
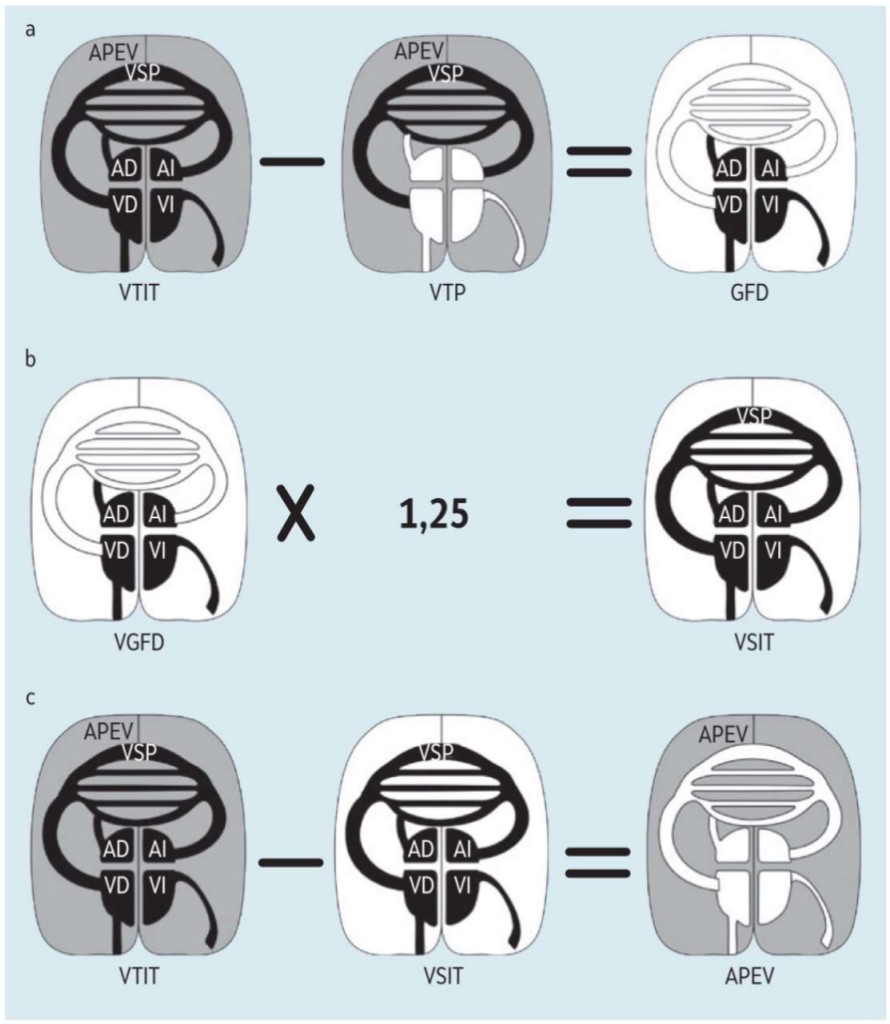
Tanto la PiCCO como el VolumeView también calculan el volumen san- guíneo pulmonar (VSP), IPVP, VS, fracción de eyección global (FEG), índice de función cardíaca (IFC), índice de potencia cardíaca (IPC) y resistencia vascular sistémica (RVS). Estos parámetros se derivan de los valores obtenidos con la TDTP:
VSP = VSIT – VGFD
IPVP = APEV/VSP
VS = GC/frecuencia cardíaca
FEG = 4 x VS/VGFD
IFC = GC/VGFD
IPC = PAM x GC
RVS = PAM-PVC/GC x 80
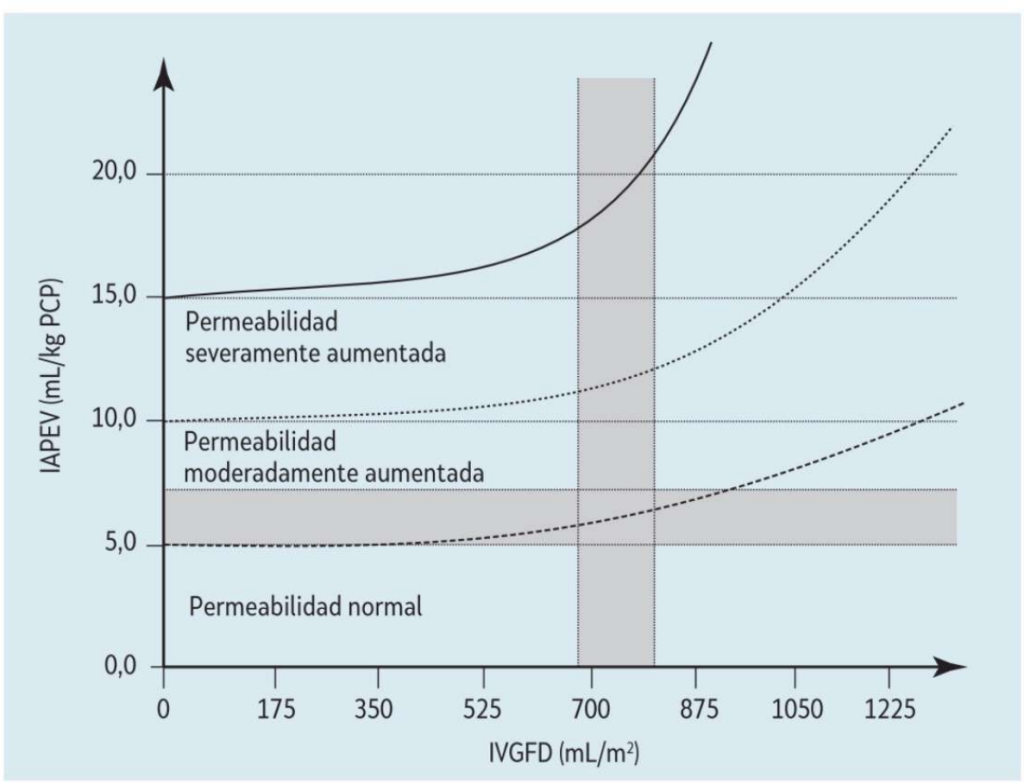
El IPVP (valores normales alrededor de 1-1,5) permite discriminar entre el edema pulmonar hidrostático (IPVP 2-2,5) y el edema pulmonar de hiperpermeabilidad (IPVP >3). En la siguiente figura se muestra la relación entre el APEV y el VGFD durante la permeabilidad normal y aumentada. Los valores absolutos para el GC, VGFD, VSIT, VS y RVS se indexan según el ASC o área de superficie corporal (IC, IVGFD, IVSIT, IVS e IRVS) y para el APEV según el peso corporal predicho (IAPEV), aunque, idealmente, la mejor forma de indexar el APEV parece ser la altura. En las ecuaciones anteriores, el VGFD se mide/calcula correctamente, mientras que el VSIT se estima con base en la correlación obtenida entre la técnica transpulmonar simple y la de doble indicador; es decir, VSIT = 1,25 × VGFD. Es asumible que esta relación lineal no es constante, pero podría depender de las características del paciente, las patologías subyacentes y las comorbilidades.
La técnica de la TDTP ha sido ampliamente validada en diferentes poblaciones de patentes: trasplante de pulmón, sepsis y choque séptico y cirugía cardíaca, entre otras. Las indicaciones para la termodilución transpulmonar son estados de choque con una fase de fluidos poco clara, falla orgánica de inicio reciente (por ejemplo, insuficiencia renal) o insuficiencia respiratoria (SDRA, edema pulmonar, pérdida capilar). La termodilución transpulmonar es menos invasiva que el CAP. La medición del GC por TDTP es menos dependiente del ciclo respiratorio. Los parámetros están disponibles rápidamente y son directamente aplicables a la clínica. La cuantificación volumétrica es independiente de la PIT, la PEEP o la PAI y se puede utilizar en una amplia gama de pacientes (desde adultos hasta niños pequeños). En el caso de una derivación de derecha a izquierda (como puede ser en el caso del SDRA con hipertensión pulmonar y foramen oval permeable), no hay pérdida del indicador. Además, después de la calibración con TDTP, el análisis del contorno de pulso proporciona latido a latido el GC en tiempo real, la hemodinámica funcional y la poscarga (como se discutirá en otra parte). La comparación cabeza a cabeza entre el IVVDFD, obtenido con el CAP, y el IVGFD, obtenido con PiCCO, mostró que el IVGFD refleja mejor los cambios ecocardiográficos en la precarga ventricular izquierda en respuesta a la administración de líquidos en 20 pacientes sometidos a cirugía cardíaca electiva. Como la técnica de la TDTP es menos invasiva, ha evolucionado como el nuevo estándar de oro para la validación de otras técnicas de monitorización del GC menos invasivas y no calibradas.
Volviendo a la ecuación de Stewart-Hamilton, dentro de ella encontramos la contante de corrección, la cual es un factor matemático que ajusta las mediciones del gasto cardíaco (GC) obtenidas por termodilución para compensar las pérdidas de calor y las características físicas del sistema de medición. Esta ecuación, fundamental en el uso del catéter de Swan-Ganz, se expresa como:
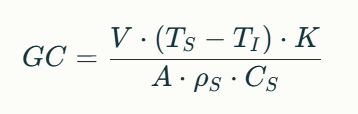
Donde:
✅ V: volumen del líquido inyectado
✅ Ts y Ti: temperaturas de la sangre y del inyectado
✅ K: constante de corrección
✅ A: área bajo la curva de termodilución
✅ Ps y Cs: densidad y calor específico de la sangre
La constante K se calcula a partir de:
✅ Densidad (ρ) y calor específico (C) del inyectado y de la sangre
✅ Factores de conversión de unidades (por ejemplo, de mL a L, o de segundos a minutos)
✅ Ajustes por pérdidas térmicas en el sistema
Una forma simplificada de la constante es:
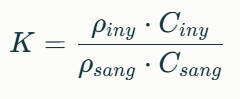
Donde:
✅ Piny y Ciny: densidad y calor específico del inyectado
✅ Psang y Csang: densidad y calor específico de la sangre
Función de la constante de corrección:
-
Compensación de pérdidas térmicas: Durante el proceso de inyección, parte del calor del líquido inyectado se disipa en el catéter o en los tejidos circundantes antes de llegar a la arteria pulmonar. La constante corrige esta pérdida para evitar subestimaciones del GC.
-
Ajuste por propiedades físicas del sistema: Incluye variables como el material del catéter, la longitud del mismo y las características del líquido inyectado (ej. solución salina vs. glucosada).
-
Calibración específica del equipo: Cada sistema de medición (ej. PiCCO, sistemas convencionales) requiere una constante determinada experimentalmente para garantizar precisión, ya que las propiedades térmicas y hidrodinámicas varían entre dispositivos.
Factores que influyen en su valor:
✅ Temperatura ambiente: Puede alterar la transferencia de calor en el catéter.
✅ Velocidad de inyección: Inyecciones más lentas aumentan las pérdidas térmicas, requiriendo correcciones mayores.
✅ Características del paciente: Estados de hipotermia o hipertermia modifican la diferencia térmica basal.
Colocación del catéter
Previo al procedimiento, se debe tener clara la indicación de colocación del CSG, descartar cualquier posible contraindicación y valorar el riesgo de complicaciones (Tabla 1). El introductor del CSG debe ser colocado percutáneamente vía vena cava inferior a través de las venas femorales o vía vena cava superior a través de la vena subclavia o yugular interna (acceso interfascicular), estos últimos accesos son de elección para el manejo a la cabecera del paciente. El abordaje interfascicular derecho por vena yugular interna es el preferido debido al fácil y rápido acceso a la AD. La punción se debe realizar en posición supina o Trendelenburg con guía ecográfica, confirmando un adecuado retorno venoso, y dilatando la zona de acceso a través de un dilatador para facilitar el ingreso del introductor venoso.
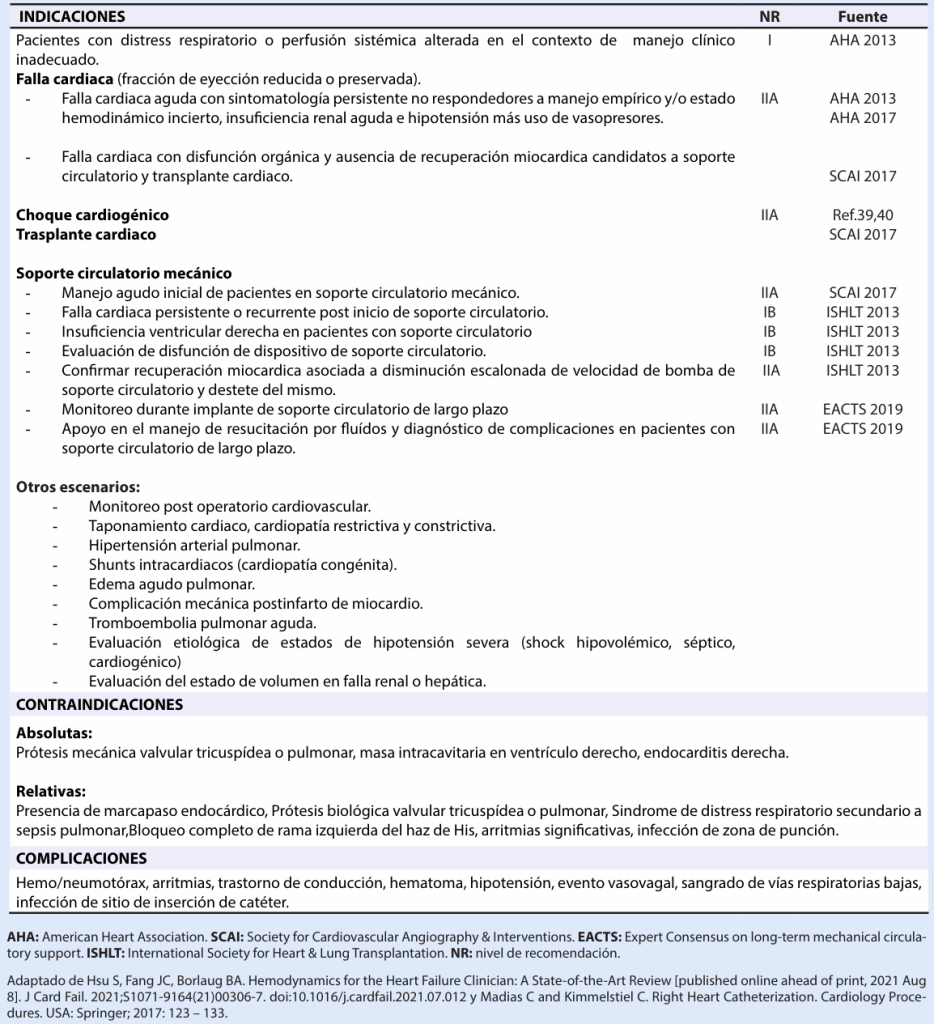
El CSG debe ser introducido hasta aproximadamente 15 cm y obtener ondas de presión de AD, luego de ello, el balón distal será inflado y se continuará el ingreso rápido del catéter a través del ventrículo derecho (VD), para evitar ectopias ventriculares, hasta obtener ondas de presión de AP. Luego se progresará lentamente hasta obtener una curva de presión capilar pulmonar (PCP), esto sucede a los 50 o 55 cm de ingresado el cateter.
La puesta a cero del sistema de presiones es importante para obtener un valor adecuado de la PCP y se realiza posicionando el transductor a nivel de AD (línea medio-axilar, 4to espacio intercostal). Se debe fijar el CSG con el capuchón de protección para mitigar el riesgo de infecciones y se confirmará la adecuada posición localizando radiológicamente el catéter distal en la zona pulmonar III de West.
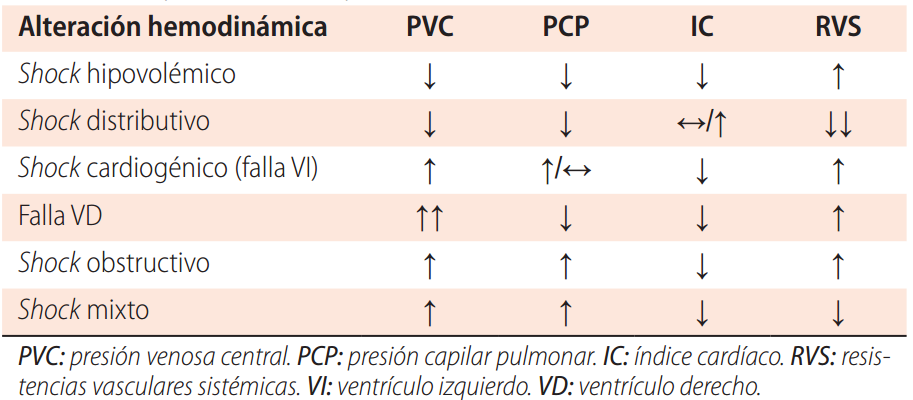
El GC por termodilución, se realiza infundiendo 10 mL de suero salino por el lumen proximal con una jeringa en menos de 4 segundos. La modificación de la constante de cálculo de GC depende de la temperatura de infusión, siendo 0,532 para 0 °C y 0,586 para 24 °C (esto puede variar según la marca y tipo de monitor). Con el GC obtenido se realizarán los cálculos hemodinámicos, se debe tener en cuenta que la presencia de insuficiencia tricuspídea, estados de bajo gasto o shunts intracardiacos pueden alterar la exactitud de los resultados.
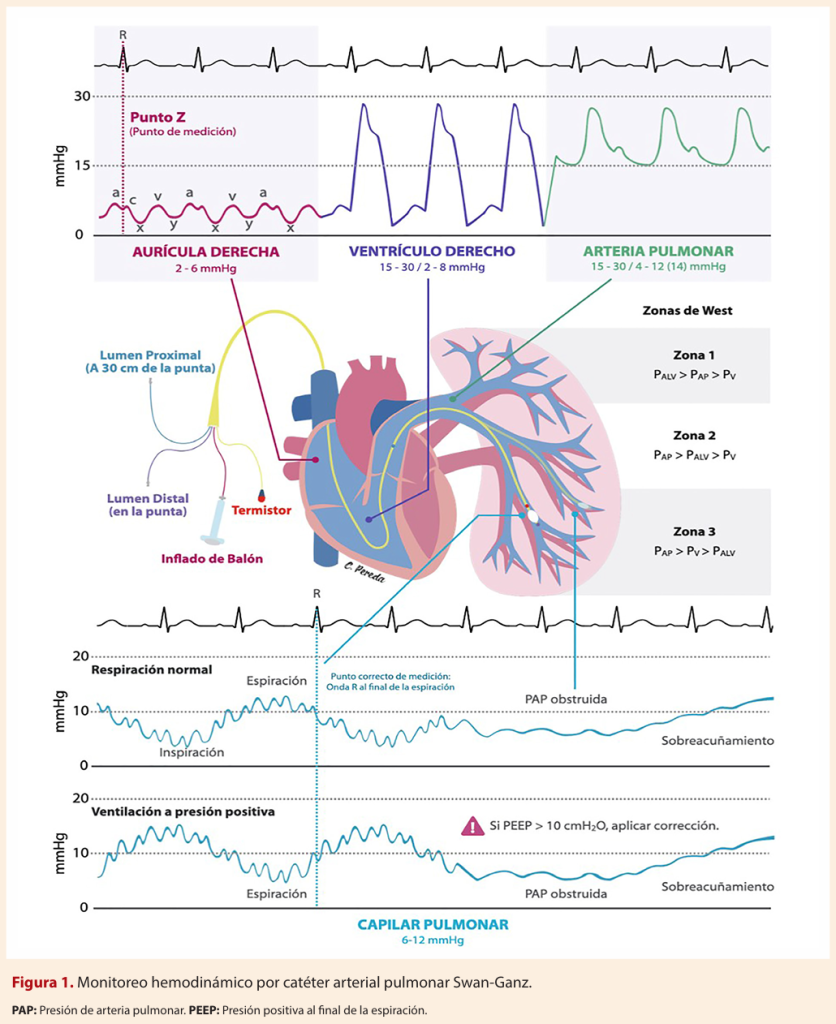
Monitoreo hemodinámico
Morfología de las ondas
La morfología de las ondas registradas por el catéter de Swan-Ganz varía según la localización de la punta del catéter en el sistema cardiovascular derecho y la arteria pulmonar. En la aurícula derecha, la onda es de baja amplitud y presenta componentes a, c y v, reflejando la contracción auricular, el abombamiento de la válvula tricúspide y el llenado auricular, respectivamente. Al avanzar al ventrículo derecho, la onda muestra un ascenso rápido en sístole y un descenso abrupto en diástole, con presiones sistólicas elevadas y diastólicas bajas. En la arteria pulmonar, la morfología es pulsátil, con una incisura dícrota característica que corresponde al cierre de la válvula pulmonar; la presión diastólica es mayor que en el ventrículo derecho. Finalmente, en la posición de cuña (wedge), la onda se aplana y se asemeja a la presión auricular izquierda, con menor amplitud y sin pulsatilidad significativa, reflejando la presión de llenado del ventrículo izquierdo. La interpretación precisa de estas morfologías es esencial para el análisis hemodinámico y la toma de decisiones clínicas, como se detalla en la literatura sobre análisis de ondas hemodinámicas.
Durante la diástole, el ventrículo derecho se relaja y su presión cae rápidamente, alcanzando valores bajos (normalmente entre 2 y 8 mmHg). En cambio, la arteria pulmonar mantiene una presión diastólica más alta (usualmente entre 8 y 15 mmHg). Esta diferencia se debe a que, tras el cierre de la válvula pulmonar, la sangre que ha sido eyectada permanece en la arteria pulmonar, donde la pared elástica de la arteria y la resistencia vascular pulmonar mantienen una presión residual. El ventrículo derecho, al estar separado por la válvula cerrada, no recibe esta presión y su presión diastólica refleja únicamente el llenado pasivo desde la aurícula derecha, que es mucho menor.
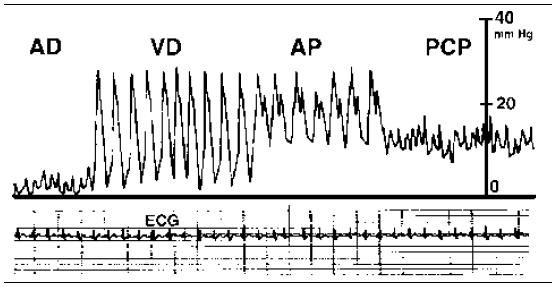
Aurícula derecha
El trazado de presión de la AD presenta diferentes curvas de presión (secuencia A-X-V-Y). La onda A representa la contracción auricular, el descenso X la caída de presión durante la sístole ventricular temprana y la relajación auricular; la onda V el llenado auricular durante la sístole ventricular y el descenso Y la diástole temprana con el vaciamiento rápido de la AD. Así, el descenso X y la pendiente ascendente de la onda V son eventos sistólicos, mientras que el pico de la onda V, el descenso Y y la onda A son eventos diastólicos. La presión venosa central (PVC) refleja la presión intrauricular derecha, se prefiere su medición a nivel del punto Z representado por la correlación del inicio del segmento QRS en el ECG y la intersección entre la onda A y C. La PVC manifiesta el estado volémico del paciente y su relación directa con el VD, se puede interpretar como las presiones de llenado del lado derecho del corazón (Tabla 2).
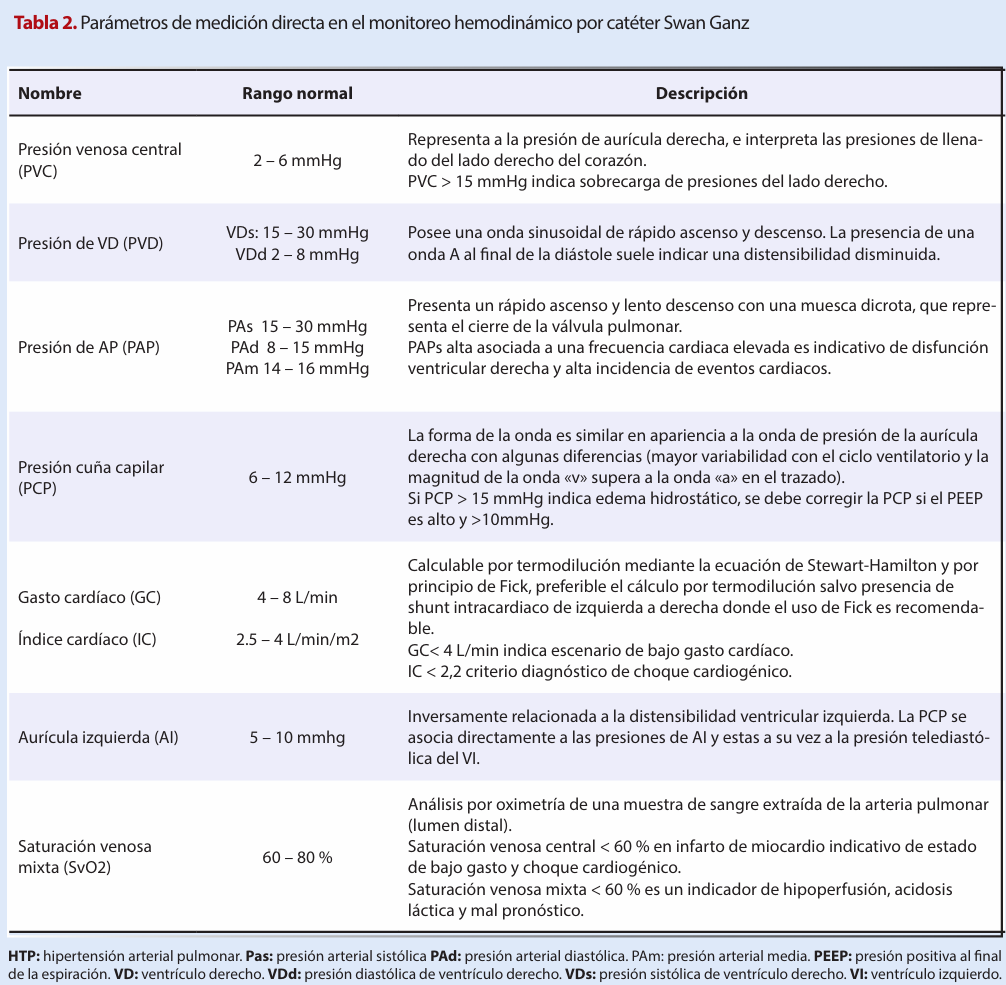
Ventrículo derecho
Los trazos del VD exhiben un rápido aumento de la presión durante la contracción ventricular y un rápido descenso de la presión durante la relajación, con una fase diastólica caracterizada por una presión inicialmente baja que aumenta gradualmente. La presión de la AD debe ser bastante cercana a la presión telediastólica del VD, a menos que exista estenosis tricuspídea. Con la contracción auricular, puede aparecer una onda A al final de la diástole ventricular, siendo un hallazgo anormal y suele indicar una distensibilidad disminuida, como en pacientes con hipertensión pulmonar (HTP), hipertrofia del VD o sobrecarga de volumen.
La distensibilidad de arteria pulmonar (DAP), determinado por los componentes resistivos y pulsátiles de la carga del VD, representa la relación entre el volumen eyectivo y la presión de pulso pulmonar (PPP). Ha demostrado ser un fuerte indicador pronóstico de mortalidad y disfunción de VD en HTP tipo II y falla cardiaca con fracción de eyección reducida (FCFEVIr); un valor menor a 2,15 se asocia con una menor supervivencia, incluso en aquellos pacientes con RVP normal.
Por otro lado, la elastancia efectiva de arteria pulmonar (EAP), medida que relaciona la presión sistólica de AP (PAPs) con el volumen eyectivo de VI, representa al igual que la DAP la poscarga y función del VD y, por ello, es un factor predictivo más específico de mortalidad y disfunción de VD (independientemente de la RVP y la GDP) en pacientes con HTP tipo II y FC incluso con FCFEVIp. Valores mayores a 1 apoyan la necesidad de una terapia dirigida a mejorar la carga total del VD en lugar del componente precapilar, y se recomienda su uso en pacientes con FC descompensada e HTP II, así como falla de VD.
El índice de pulsatibilidad arterial pulmonar (PAPi) determinado por la relación entre la PPP y la AD, es un parámetro que predice la disfunción severa de VD en el contexto de un infarto de miocardio inferior y/o soporte circulatorio mecánico (SCM) de VI, desarrollado con el fin de identificar pacientes con requerimiento de asistencia mecánica derecha; asimismo, tiende a ser más predictivo en pacientes con soporte inotrópico y es útil como indicador pronóstico de supervivencia de HTP cuando los valores son < 0,95.
ITSVD
La ITSVD en el monitoreo hemodinámico por Swan-Ganz es el Índice de Trabajo Sistólico del Ventrículo Derecho. Este parámetro cuantifica el trabajo que realiza el ventrículo derecho para eyectar la sangre hacia la circulación pulmonar en cada latido, ajustado por la superficie corporal del paciente25.
¿Qué representa la ITSVD?
✅ Refleja la función contráctil y la capacidad de bombeo del ventrículo derecho.
✅ Integra tanto la presión generada (postcarga) como el volumen de sangre eyectado (volumen sistólico).
✅ Es útil para evaluar el estado hemodinámico del ventrículo derecho, especialmente en patologías como la insuficiencia cardíaca derecha, hipertensión pulmonar y shock.
¿Cómo se calcula la ITSVD?
La fórmula es:
ITSVD = (PAPm−PVC) × IVS × 0.0136
Donde:
✅ PAPm: Presión Arterial Pulmonar Media (mmHg)
✅ PVC: Presión Venosa Central (mmHg)
✅ IVS: Índice de Volumen Sistólico (ml/latido/m²)
✅ 0.0136: Factor de conversión para expresar el resultado en gramos-metro por metro cuadrado por latido (g·m/m²/latido)
Valores normales de ITSVD: 7–12 g·m/m²/latido.
Utilidad clínica
✅ Un ITSVD bajo puede indicar disfunción del ventrículo derecho, sobrecarga de presión o volumen, o insuficiencia cardíaca derecha.
✅ Un ITSVD alto puede reflejar un aumento de la demanda o estados hiperquinéticos.
Arteria pulmonar
El trazado de la presión de la AP muestra un rápido aumento de la presión, un pico sistólico, una disminución de la presión después de la eyección máxima y una muesca dicrótica bien definida por el cierre de la válvula pulmonar durante la disminución de la presión. No debe existir una diferencia de presión sistólica entre el ventrículo derecho y la AP, a menos que exista estenosis de la arteria o válvula pulmonar.
La forma de onda de la AP, al igual que otras formas de onda de presión del corazón derecho, está sujeta a cambios respiratorios, por ello los pacientes en ventilación mecánica, con enfermedad pulmonar grave, obesidad mórbida o dificultad respiratoria, pueden generar cambios sustanciales en la presión intratorácica con diferencias marcadas en las presiones de la AP durante las fases respiratorias. La mayoría de los expertos consideran que el final de la espiración es el punto adecuado para evaluar las presiones de la arteria pulmonar (y de otras cámaras cardíacas) porque es en esta fase donde la presión intratorácica se encuentra más cerca de cero.
La PAPs se produce al mismo tiempo que la onda T en el ECG y ha demostrado ser un parámetro relacionado a eventos cardíacos mayores. Una PAPs asociada a una frecuencia cardiaca alta determina un mayor consumo de oxígeno por el VD en HTP tipo I y, por ende, mayor riesgo de disfunción de VD.
La medición de la presión arterial pulmonar media (PAPm) es relevante en el diagnóstico y manejo de HTP. Según el último consenso del Sexto Simposio Mundial de Hipertensión Pulmonar (WSPH), un valor > 20 mmHg representa un punto de corte para el diagnóstico de HTP ya que el manejo médico adecuado a partir de este valor muestra beneficios en la sobrevida.
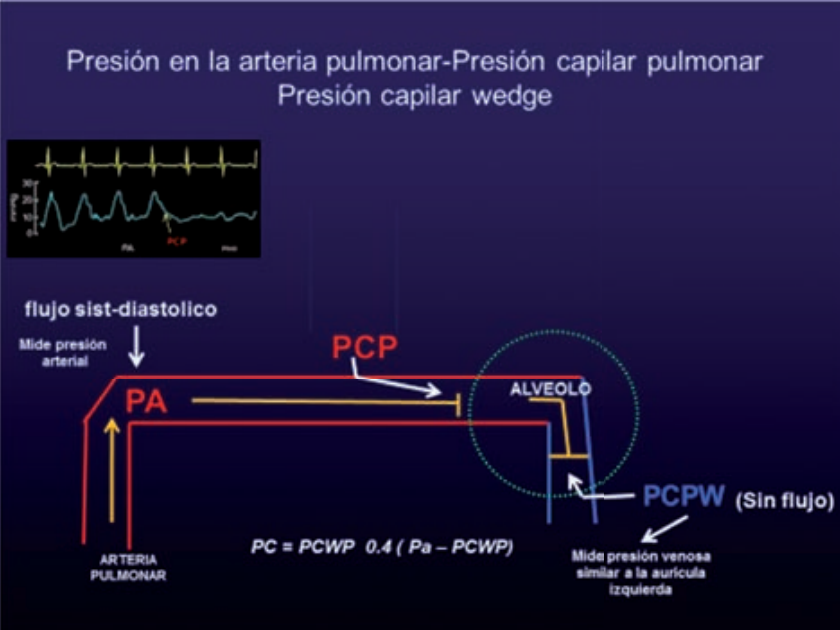
Presion capilar pulmonar
La PCP es medida directamente en ausencia del flujo anterógrado de la AP, de modo que se transmita desde la aurícula izquierda, a través de las venas pulmonares y el lecho capilar pulmonar. Normalmente se encuentra a unos milímetros de mercurio por debajo de la presión de la aurícula izquierda (0 a 5 mmHg). Las características de una buena onda incluyen la presencia de ondas A y V, la confirmación fluoroscópica de la ubicación de la punta del catéter en AP distal con el globo inflado, la observación de una curva PAPm cuando se desinfla el balón o se retira el catéter de su posición, y una saturación de oxígeno con el globo inflado > 90%, siendo esta última la más específica (Tabla 2). Si la punta del catéter se encuentra mal posicionada en una rama periférica de AP con el globo sobre distendido se produce un fenómeno de «sobreacuñamiento» observándose una curva de PCP falsa con una línea oscilante sin ondas A y V, lo cual puede provocar la ruptura abrupta de la AP.
La presión capilar por enclavamiento (PCP) se logra midiendo la presión en el extremo distal del catéter con el balón insuflado en la AP; de esta manera, se obstruye el flujo y ello crea una columna estática de sangre entre el extremo del catéter y la aurícula izquierda (AI), permitiendo que las presiones entre ambos extremos se equilibren logrando una presión que, en condiciones óptimas, es igual a la presión de la AI. La PCP es similar a la presión de fin de diástole (PFD) del ventrículo izquierdo (VI). La misma correlaciona con el volumen de fin de diástole del VI cuando su distensibilidad es normal. Si bien la precarga es un concepto de estiramiento de una fibra muscular generada por un volumen determinado, la PCP nos da una estimación de la PFD del VI y de la precarga del VI.
En pacientes con ventilación mecánica con presión positiva al final de la espiración (PEEP) >10 cmH2O se produce un aumento significativo de la presión alveolar, lo cual reduce la proporción de la zona pulmonar 3 de WEST, siendo afectadas directamente las presiones del lado derecho provocando una sobreestimación de la PCP. La corrección directa de la PCP por PEEP elevado se realiza sustrayendo de la PCP la presión esofágica medida con un balón intraesofágico; no obstante, existen otros métodos prácticos como la sustracción de 2 a 3 mmHg de PCP por cada 5 cmH2O de aumento del PEEP o argumentando que la PCP corregida es igual al PCP medido menos la mitad del cociente del PEEP dividido por 1,36.
Si la PCP está elevada, el aumento de la relación entre AD y PCP sirve como indicador de disfunción de VD e incremento de complicaciones en IC avanzada, su valor se asocia con mayor resistencia pulmonar y mortalidad intrahospitalaria.
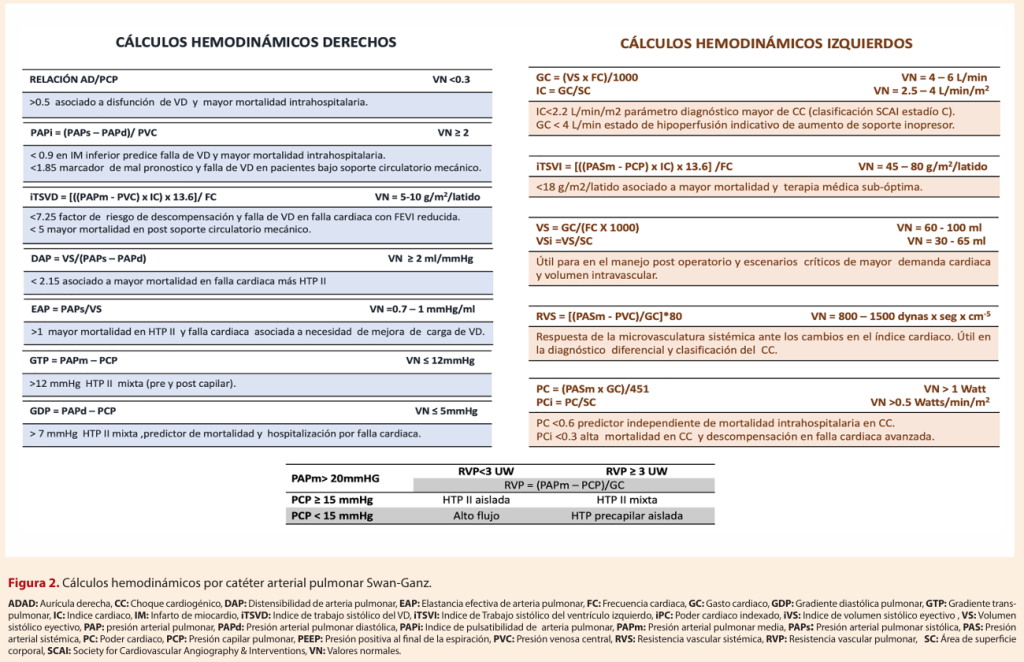
Para evaluar si el aumento de la presión de AP es secundaria a una elevación aislada de la presión de enclavamiento pulmonar, clásicamente se utilizaba la gradiente de presión arterial transpulmonar cuyo valor varía según el flujo de PAPm y las presiones de llenado de VI; actualmente, su relevancia ha disminuido notablemente. Sin embargo, la gradiente de presión arterial pulmonar diastólica es un marcador más exacto que permite clasificar adecuadamente a la HTP según su componente pre y poscapilar; además, un valor elevado es considerado como predictor de mortalidad, mal pronóstico y hospitalización por falla cardiaca.
Por último, la resistencia vascular pulmonar (RVP) es un marcador que desde el sexto WSPH ha ganado protagonismo; determinando la presencia de enfermedad vascular pulmonar al ser un mejor indicador de HTP precapilar, en contraste a la GDP. Es utilizado, además, como parámetro terapéutico en pacientes con cardiopatías congénitas y en pacientes en espera de un trasplante cardiaco.
RVS
La RVS en el monitoreo hemodinámico por Swan-Ganz corresponde a la Resistencia Vascular Sistémica. Es un parámetro fundamental que estima la postcarga del ventrículo izquierdo, es decir, la resistencia que debe vencer el corazón para eyectar la sangre hacia la circulación sistémica.
¿Qué representa la RVS?
✅ Refleja la resistencia total que ofrece el lecho vascular sistémico al flujo sanguíneo.
✅ Es un indicador clave para clasificar y manejar diferentes tipos de shock (cardiogénico, séptico, etc.) y para evaluar la respuesta a tratamientos vasopresores o vasodilatadores.
¿Cómo se calcula la RVS?
La fórmula clásica es:
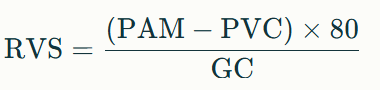
Donde:
✅ PAM: Presión Arterial Media (mmHg)
✅ PVC: Presión Venosa Central (mmHg)
✅ GC: Gasto Cardíaco (L/min)
✅ 80: Factor de conversión para expresar el resultado en din·seg/cm⁵
Valores normales de RVS: 800–1600 din·seg/cm⁵.
Utilidad clínica
✅ Una RVS alta sugiere vasoconstricción o aumento de la postcarga (como en shock cardiogénico o estados de bajo gasto).
✅ Una RVS baja indica vasodilatación sistémica (como en shock séptico).
IRVS
La IRVS en el monitoreo hemodinámico por Swan-Ganz es el Índice de Resistencia Vascular Sistémica. Este parámetro cuantifica la resistencia que ofrece el sistema vascular periférico al flujo sanguíneo, ajustado por la superficie corporal, y es fundamental para evaluar la poscarga del ventrículo izquierdo.
¿Qué representa la IRVS?
✅ Refleja la resistencia total que debe vencer el ventrículo izquierdo para eyectar la sangre hacia la circulación sistémica.
✅ Es clave para la valoración y el manejo de estados de shock, insuficiencia cardíaca y otras alteraciones hemodinámicas en pacientes críticos.
¿Cómo se calcula la IRVS?
La fórmula es:
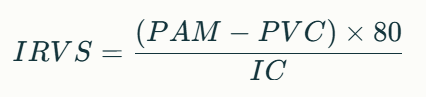
Donde:
✅ PAM: Presión Arterial Media (mmHg)
✅ PVC: Presión Venosa Central (mmHg)
✅ IC: Índice Cardíaco (L/min/m²)
✅ 80: Factor de conversión para expresar el resultado en din·seg·m²/cm⁵
Valores normales de IRVS: 1600–2400 din·seg·m²/cm⁵.
Utilidad clínica
✅ Una IRVS alta sugiere vasoconstricción o aumento de la poscarga (por ejemplo, en shock cardiogénico o hipovolémico).
✅ Una IRVS baja indica vasodilatación sistémica (como en shock distributivo/septico).
RVP
La RVP en el monitoreo hemodinámico por Swan-Ganz corresponde a la Resistencia Vascular Pulmonar. Es un parámetro que cuantifica la resistencia que encuentra la sangre al pasar a través de la circulación pulmonar, es decir, desde el ventrículo derecho hacia los pulmones.
¿Qué representa la RVP?
✅ Refleja la poscarga del ventrículo derecho, es decir, el esfuerzo que debe realizar para bombear la sangre hacia la arteria pulmonar.
✅ Es fundamental para diagnosticar y monitorizar enfermedades como la hipertensión pulmonar, embolia pulmonar, enfermedad pulmonar obstructiva crónica (EPOC) y otras patologías que afectan la circulación pulmonar.
¿Cómo se calcula la RVP?
La fórmula clásica es:
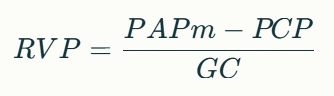
Donde:
✅ PAPm: Presión Arterial Pulmonar Media (mmHg)
✅ PCP: Presión de enclavamiento capilar pulmonar (mmHg)
✅ GC: Gasto Cardíaco (L/min)
Para expresar la RVP en dinas·seg/cm⁵, se multiplica el resultado por 80:
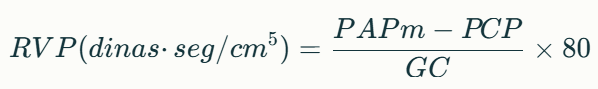
También puede expresarse en unidades Wood (1 unidad Wood = 80 dinas·seg/cm⁵).
Valores normales
✅ RVP normal: 1–3 unidades Wood (80–240 dinas·seg/cm⁵).
Utilidad clínica
✅ Una RVP elevada indica aumento de la resistencia en la circulación pulmonar, como ocurre en la hipertensión pulmonar o en obstrucciones vasculares.
✅ Una RVP baja puede observarse en estados de vasodilatación pulmonar.
IRVP
La IRVP en el monitoreo hemodinámico por Swan-Ganz es el Índice de Resistencia Vascular Pulmonar. Este parámetro cuantifica la resistencia que enfrenta la sangre al pasar por la circulación pulmonar, ajustado por la superficie corporal del paciente, y es fundamental para evaluar la poscarga del ventrículo derecho.
¿Qué representa la IRVP?
✅ Refleja la resistencia total del lecho vascular pulmonar, es decir, la dificultad que tiene el ventrículo derecho para eyectar sangre hacia los pulmones.
✅ Es clave para la valoración de enfermedades como la hipertensión pulmonar y para el seguimiento de pacientes críticos con alteraciones respiratorias o cardíacas.
¿Cómo se calcula la IRVP?
La fórmula es:
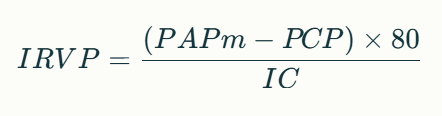
Donde:
✅ PAPm: Presión Arterial Pulmonar Media (mmHg)
✅ PCP: Presión Capilar Pulmonar (mmHg)
✅ IC: Índice Cardíaco (L/min/m²)
✅ 80: Factor de conversión para expresar el resultado en din·seg·m²/cm⁵
Valores normales de IRVP: 250–340 din·seg·m²/cm⁵.
Utilidad clínica
✅ Una IRVP elevada indica aumento de la resistencia en la circulación pulmonar, como ocurre en la hipertensión pulmonar o en obstrucciones vasculares.
✅ Una IRVP baja puede observarse en estados de vasodilatación pulmonar.
Ventrículo izquierdo
La presión del VI tiene una aceleración rápida durante la sístole inicial, seguida de un descenso rápido. La presión diastólica inicial es baja, mientras que la final aumenta lentamente hasta que la aurícula izquierda se contrae representando la verdadera precarga del ventrículo izquierdo. Con la ayuda del CAP se puede calcular el GC y, por ende, el índice cardiaco (IC) mediante termodilución y por el principio de Fick. La presencia de un IC disminuido es el indicador hemodinámico principal en el diagnóstico de CC. Puede ayudar a reconocer un mal funcionamiento de los dispositivos de SCM y evaluar la recuperación del miocardio con miras al destete. Junto con la resistencia vascular sistémica (RVS) el IC permite diferenciar los distintos tipos de fenotipos de CC (6). Con los valores del GC se puede calcular el poder cardíaco (PC) el cual es el marcador hemodinámico independiente más fuerte de mortalidad intrahospitalaria que el Shock trial registró dentro de la estratificación de riesgo en pacientes con infarto de miocardio, un valor < 0,6 Watts es indicador de disfunción severa del VI.
Por otro lado, la presión de llenado transmural de VI representa la precarga del VI, así como la diferencia entre la presión capilar pulmonar (PCP) y la presión pericárdica (PP), utilizando la PVC en lugar de la PP en el cálculo. La PCP varía con los cambios de presión transmural del VI y la PP, por lo que en un paciente con FC evidencia el efecto restrictivo pericárdico sobre la precarga del VI.
Existe también una medida de valoración biventricular llamada índice de trabajo sistólico(iTS). Este parámetro evalúa el trabajo (energía) ventricular y ha demostrado que su caída en VI es un predictor de mal pronóstico y necesidad de mayor soporte hemodinámico; además, el iTS de VD es un predictor de falla de VD en SCM y mortalidad en pacientes postransplante pulmonar.
ITSVI
La ITSVI en el monitoreo hemodinámico por Swan-Ganz corresponde al Índice de Trabajo Sistólico del Ventrículo Izquierdo. Es un parámetro que refleja el trabajo realizado por el ventrículo izquierdo para eyectar la sangre hacia la aorta en cada latido, ajustado por la superficie corporal del paciente.
¿Qué representa la ITSVI?
✅ ITSVI evalúa la función contráctil del ventrículo izquierdo, integrando tanto la presión generada (postcarga) como el volumen de sangre eyectado (volumen sistólico).
✅ Es útil para valorar la capacidad de bombeo del corazón y el estado hemodinámico general, especialmente en pacientes críticos o con shock.
¿Cómo se calcula la ITSVI?
La fórmula es:
ITSVI = (PAM−PCP) × IVS × 0.0136
Donde:
✅ PAM: Presión Arterial Media (mmHg)
✅ PCP: Presión Capilar Pulmonar (mmHg)
✅ IVS: Índice de Volumen Sistólico (ml/latido/m²)
✅ 0.0136: factor de conversión para expresar el resultado en gramos-metro por metro cuadrado por latido (g·m/m²/latido)
Valores normales de ITSVI: 44–64 g·m/m²/latido.
Utilidad clínica:
✅ Un ITSVI bajo indica disminución de la contractilidad o un aumento significativo de la postcarga, y puede ser señal de insuficiencia cardíaca o shock.
✅ Un ITSVI alto puede reflejar un aumento de la demanda cardíaca o estados hiperquinéticos.
Shunt intracardiaco (SI)
Una saturación de oxígeno de AP mayor a 75% puede indicar la presencia de un SI de izquierda a derecha, por lo que es recomendado realizar la medición de la vena cava superior e inferior, AD (media, alta y baja), VD y AP. El aumento de la saturación de oxígeno ≥ 7% puede ser indicativo de un shunt auricular de izquierda a derecha, mientras que ≥ 5% puede indicar un shunt a nivel del VD o de AP. Cuando se sospecha de un SI izquierda a derecha, el método directo de Fick es el medio preferido de medición del GC.
Cuadrantes de Forrester
La clasificación de Forrester es un sistema hemodinámico que utiliza los datos obtenidos mediante el catéter de Swan-Ganz para categorizar a los pacientes con insuficiencia cardíaca aguda o shock cardiogénico. Se basa en dos parámetros principales:
✅ Presión capilar pulmonar (PCP o wedge, reflejo de la congestión pulmonar)
✅ Índice cardíaco (IC, reflejo de la perfusión sistémica)
Estos parámetros permiten dividir a los pacientes en cuatro cuadrantes o perfiles hemodinámicos, que orientan el diagnóstico y el tratamiento.
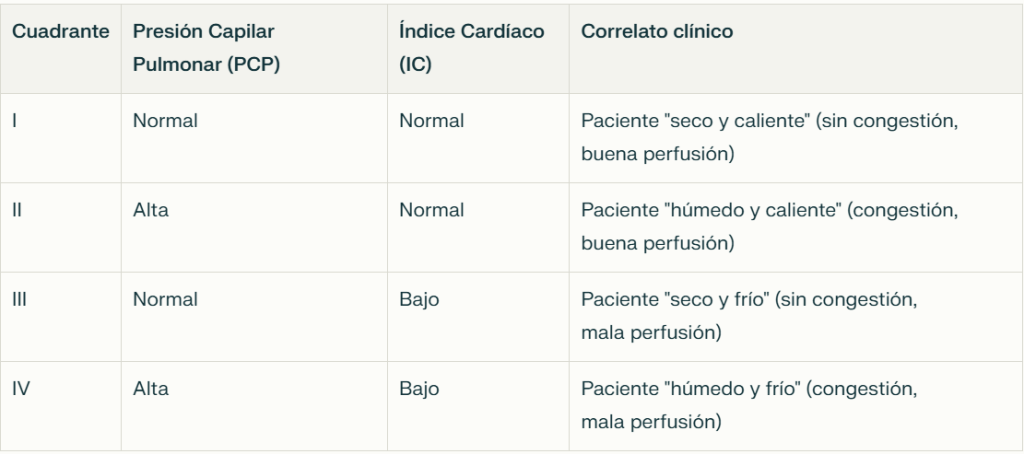
Interpretación de cada cuadrante
↪️ Cuadrante I («seco y caliente»):
✅PCP normal, IC normal.
✅El paciente no presenta congestión ni hipoperfusión. Es el estado hemodinámico ideal.
↪️ Cuadrante II («húmedo y caliente»):
✅PCP elevada, IC normal.
✅Hay congestión pulmonar pero la perfusión sistémica es adecuada. Es típico de insuficiencia cardíaca descompensada pero sin shock.
↪️ Cuadrante III («seco y frío»):
✅PCP bajo, IC bajo.
✅No hay congestión, pero existe hipoperfusión sistémica, como en el shock hipovolémico.
↪️ Cuadrante IV («húmedo y frío»):
✅PCP elevada, IC bajo.
✅Hay congestión pulmonar y mala perfusión, típico del shock cardiogénico grave y de peor pronóstico.
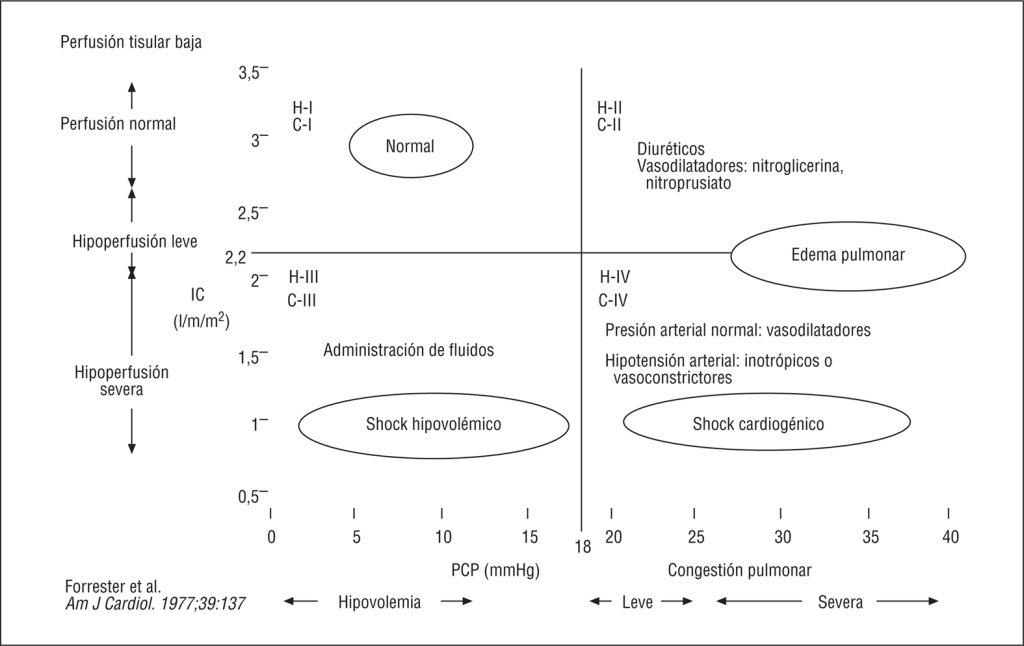
Utilidad clínica
La clasificación de Forrester ayuda a guiar el tratamiento:
✅ Si hay congestión (PCP alta), se consideran diuréticos o vasodilatadores.
✅ Si hay hipoperfusión (IC bajo), puede requerirse soporte inotrópico o vasopresor.
✅ El cuadrante IV (húmedo y frío) es el de mayor gravedad y peor pronóstico, requiriendo intervenciones agresivas.
Esta clasificación sigue siendo una herramienta fundamental en la monitorización y manejo de pacientes críticos con insuficiencia cardíaca aguda, especialmente cuando se utiliza el catéter de Swan-Ganz para obtener mediciones precisas.