La investigación muscular a principios del siglo XIX se centró en el entonces nuevo campo de la termodinámica, en particular la primera ley, que establece que la suma de las energías en un sistema aislado es constante. Esto significa que cuando un músculo se contrae, la energía química consumida por la maquinaria contráctil se libera en forma de trabajo y calor. El trabajo muscular se había cuantificado desde el siglo XVII, y el primer esfuerzo para medir la producción de calor por músculo aislado fue realizado por el físico y fisiólogo alemán Hermann von Helmholtz en 1848. Sin embargo, no fue hasta la década de 1920 que A. V. Hill pudo medir el calor muscular con suficiente precisión para obtener información sobre la química de la contracción muscular. Un primer esfuerzo para medir la producción de calor por el músculo cardíaco fue realizado en 1925 por L. N. Katz, a quien está dedicado este texto, pero su esfuerzo resultó infructuoso porque el corazón generaba demasiado poco calor para ser registrado por los instrumentos de la época. Investigaciones posteriores que utilizan una mejor instrumentación han demostrado diferencias importantes entre la energía del músculo cardíaco y el músculo esquelético, pero los estudios de Hill continúan proporcionando información valiosa sobre la maquinaria contráctil del corazón.
Términos
Contracciones isométricas e isotónicas
Los fisiólogos generalmente estudian los músculos cuando se contraen a una longitud constante (contracción isométrica) o a una carga constante (contracción isotónica). En una contracción isométrica, los extremos del músculo se fijan para que el músculo no pueda acortarse; A pesar de que la tensión desarrollada es máxima en estas condiciones, el trabajo (el producto de la distancia de fuerza) es cero porque la longitud del músculo no cambia. En una contracción isotónica, se permite que el músculo se acorte mientras soporta una carga constante. Si la carga es cero, el músculo se acorta a su máxima extensión, pero no se realiza ningún trabajo porque no se desarrolla ninguna fuerza. El trabajo es máximo cuando el músculo se acorta frente a una carga intermedia. La contracción de los miocitos cardíacos en el corazón que late no es isométrica ni isotónica porque la tensión de la pared primero aumenta y luego disminuye a medida que las cavidades se vacían.
Precarga y poscarga
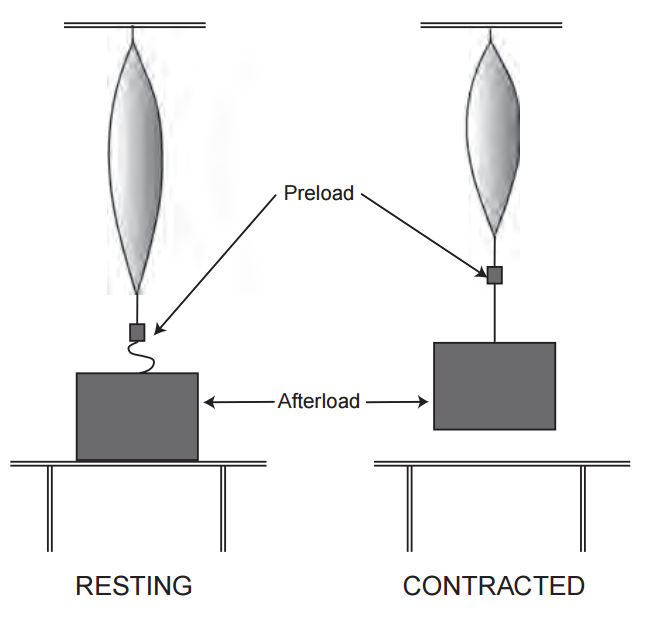
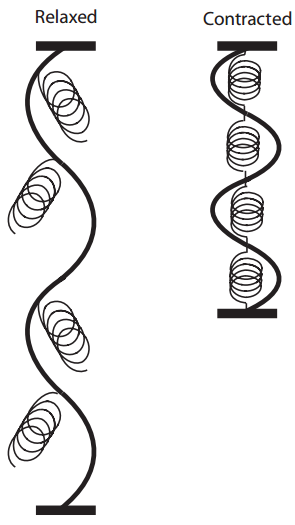
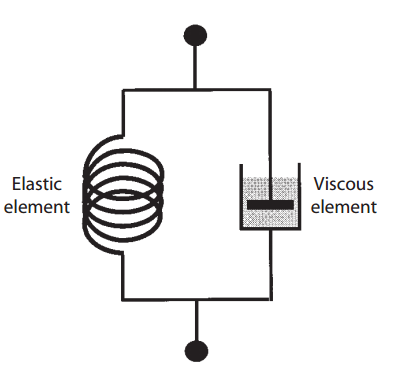
La diferencia entre una precarga y una poscarga depende del momento en que el músculo interactúa por primera vez con la carga. Una precarga estira un músculo esquelético relajado antes de que comience la contracción, mientras que el músculo no encuentra una poscarga hasta después de que haya comenzado la contracción. En un músculo lineal (Fig. 1), un peso soportado por el músculo en reposo es una precarga, mientras que un peso que descansa sobre un soporte hasta después de que haya comenzado la contracción es una poscarga.
El corazón palpitante funciona tanto con una precarga como con una poscarga. En el ventrículo izquierdo, la precarga está determinada por las presiones y volúmenes durante la diástole, mientras que la poscarga está determinada por las presiones y volúmenes después de que la presión ventricular izquierda supera la presión aórtica. La precarga y la poscarga son importantes desde el punto de vista clínico porque son determinantes importantes del trabajo del corazón e influyen en la energía del rendimiento ventricular.
Influencia de la poscarga en el trabajo
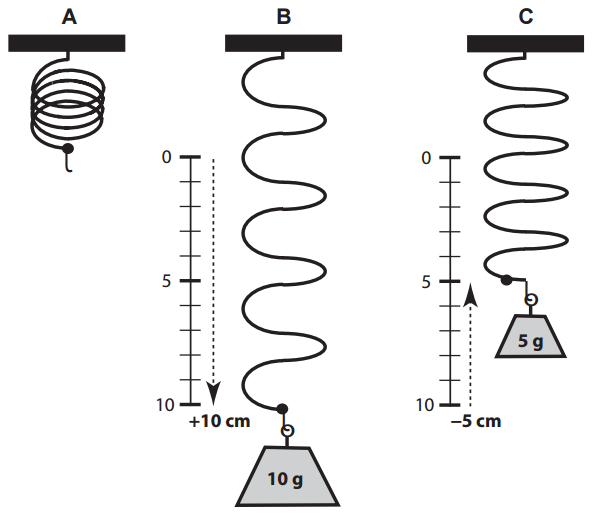
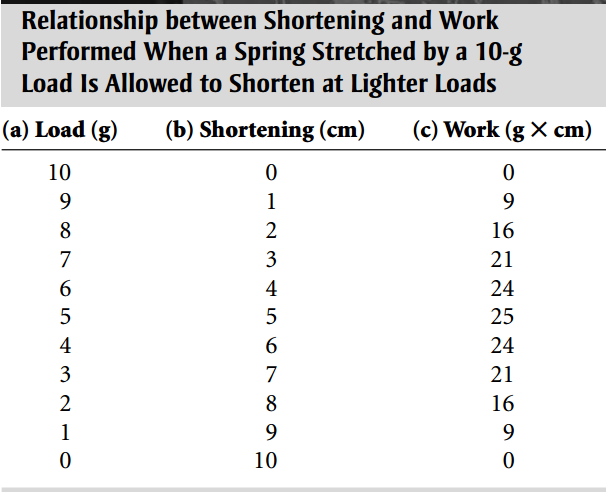
La relación entre la carga (P) y el trabajo se puede entender comparando un músculo contraído con un resorte que, cuando se carga con un peso de 10 g, ha aumentado su longitud en 10 cm (Fig. 2). Si el aumento de la longitud es linealmente proporcional al aumento de la carga (ley de Hooke), la longitud habrá aumentado 1 cm por cada gramo de carga añadida; Por el contrario, si una carga inicial de 10 g se disminuye en pasos de 1 g, el resorte se acortará 1 cm por cada gramo eliminado de la carga. Estas relaciones se muestran en la Tabla 1, donde la columna a describe la disminución gradual de la carga cuando se cuelga una serie de pesos más ligeros en el resorte después de haber sido estirado por el peso de 10 g. La columna b describe el grado de acortamiento en cada peso más ligero, mientras que la columna c enumera el trabajo que se habría realizado si el resorte estirado hubiera levantado cada uno de los pesos más ligeros, calculado multiplicando cada nueva carga (columna a) por la distancia que el resorte se habría acortado en cada nueva carga (10 – columna b). El trazado del trabajo en la columna c en función de la carga demuestra que no se realiza ningún trabajo cuando la carga es la misma que la carga máxima (P = 10 g), porque el resorte no puede acortarse con esta carga, ni cuando el resorte está completamente descargado (P = 0) porque a pesar de la gran extensión del acortamiento, No se genera ninguna fuerza. En cambio, el trabajo es máximo en las cargas intermedias (Fig. 3).
Las relaciones entre la carga de trabajo y la de un muelle también describen la influencia de la carga en el trabajo realizado por un músculo activado. Esta similitud llevó a los primeros fisiólogos a postular que la transición del reposo a la actividad ocurría cuando un músculo en reposo formaba nuevos enlaces en forma de resorte. Aunque ahora se sabe que es incorrecta, esta nueva teoría del cuerpo elástico se describe en este punto porque el reconocimiento del error fundamental proporcionó la base para nuestra comprensión moderna de la energía muscular.

Nueva teoría del cuerpo elástico de la contracción muscular
Las curvas de carga de trabajo, como la que se muestra en la Figura 3, se explicaron inicialmente postulando que la transición del reposo a la actividad en un músculo provoca la formación de nuevos enlaces elásticos dentro de la maquinaria contráctil (Fig. 4). Por lo tanto, se pensaba que la contracción se iniciaba cuando se utilizaba energía química para formar enlaces elásticos que aumentaban la capacidad del músculo para acortarse y generar tensión. Esta teoría explicaba por qué el estiramiento de un músculo en reposo (Fig. 4, izquierda) genera solo una pequeña cantidad de tensión (tensión en reposo) y la mayor rigidez del músculo activo (Fig. 4, derecha). Según esta teoría, la activación agrega una cantidad fija de energía que hace que el músculo se convierta en un resorte más rígido; es decir, un «nuevo cuerpo elástico».
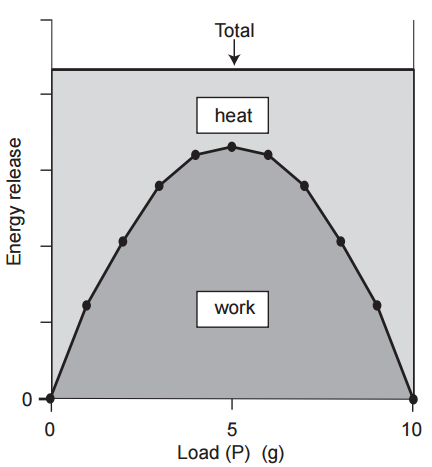
Una suposición clave de la nueva teoría del cuerpo elástico era que la excitación agrega una cantidad fija de energía al músculo para establecer los nuevos enlaces; Por esta razón, la energía total disponible para ser liberada por el músculo activo (trabajo + calor) debe ser independiente de la carga. Por lo tanto, esta teoría predijo que las curvas que relacionan la carga con la liberación total de energía se parecerían a la Figura 5. A la carga máxima, toda la energía añadida durante la transición del reposo a la actividad aparecería como calor porque no se realiza ningún trabajo. En una contracción sin carga, toda la energía añadida para establecer los nuevos enlaces cruzados en el músculo también aparecería como calor, de nuevo porque no se realiza ningún trabajo. A cargas intermedias, donde la liberación de energía como trabajo es máxima (ver Tabla 1 y Fig. 3), la liberación de calor debe ser mínima porque la nueva teoría del cuerpo elástico predice que la liberación total de energía es independiente de la carga (Fig. 5).
La nueva teoría del cuerpo elástico fue ampliamente aceptada hasta que Fenn (1923) demostró que la energía total liberada por un músculo en contracción no es constante, sino que depende de la carga.
Efecto Fenn
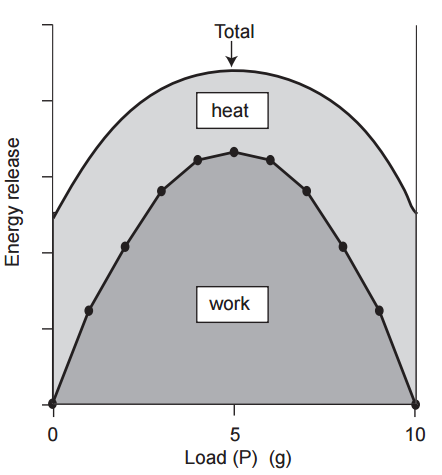
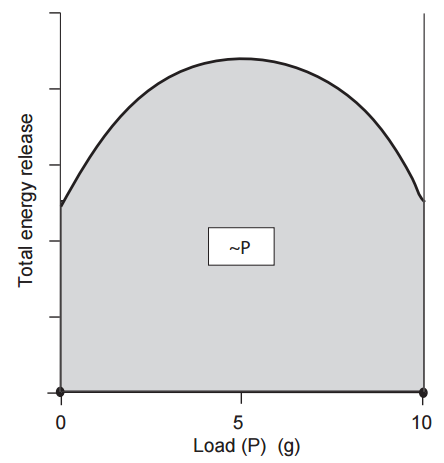
La contribución decisiva de Fenn a nuestra comprensión de la contracción muscular fue que la energía total liberada en forma de trabajo y calor aumenta cuando se realiza más trabajo (Fig. 6). Este hallazgo, llamado el «efecto Fenn», demostró que la energía disponible para ser liberada por un músculo en contracción no se determina en el momento de la activación, sino que depende de la carga porque cuando el músculo hace más trabajo, se libera más energía. Este hallazgo indicó que un músculo se asemeja a un motor de gasolina o eléctrico, donde el consumo de combustible aumenta cuando el motor está más cargado. El efecto Fenn se confirmó directamente a principios de la década de 1960 cuando se demostró que la utilización de fosfato de alta energía, como la liberación de energía como trabajo más calor, era máxima en cargas intermedias, donde se realizan los niveles más altos de trabajo (Fig. 7).
Es una curiosidad histórica que el efecto Fenn se hubiera documentado en el músculo cardíaco casi una década antes del informe de Fenn. En un artículo que había sido pasado por alto por la mayoría de los fisiólogos musculares de la época, pero que Fenn citó en su artículo de 1923, Evans y Matsuoka (1914-1915) informaron que el consumo de oxígeno cardíaco aumenta cuando el corazón hace más trabajo. Esta observación llevó a Starling, en su Conferencia Linacre describiendo la «Ley del Corazón» (1918), a equiparar el consumo adicional de oxígeno causado por un aumento en el trabajo cardíaco con el consumo de combustible adicional de una motocicleta cuando se conduce cuesta arriba.
Relación fuerza-velocidad
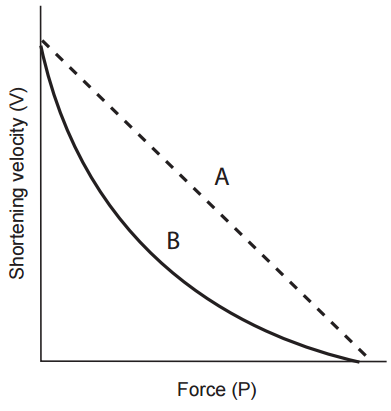
La relación fuerza-velocidad, que traza la influencia de la carga en la velocidad del acortamiento muscular, proporciona evidencia adicional de que la contracción del músculo no se comporta como un resorte estirado. La nueva teoría del cuerpo elástico, que consideraba el músculo formado por elementos elásticos y viscosos paralelos (Fig. 8), predijo que la velocidad de acortamiento aumentaría de manera lineal cuando se disminuyera la carga (curva A, Fig. 9). En 1935, sin embargo, Fenn y Marsh encontraron que esta relación era hiperbólica (curva B, Fig. 9). Aunque esta relación hiperbólica podría explicarse en el contexto de la nueva teoría del cuerpo elástico asumiendo características especiales para la elasticidad y la viscosidad muscular, A. V. Hill demostró en 1938 que la forma hiperbólica también se obtiene a partir de mediciones de trabajo y calor, y por lo tanto refleja las propiedades energéticas fundamentales de la maquinaria contráctil.
Liberación de calor por el musculo
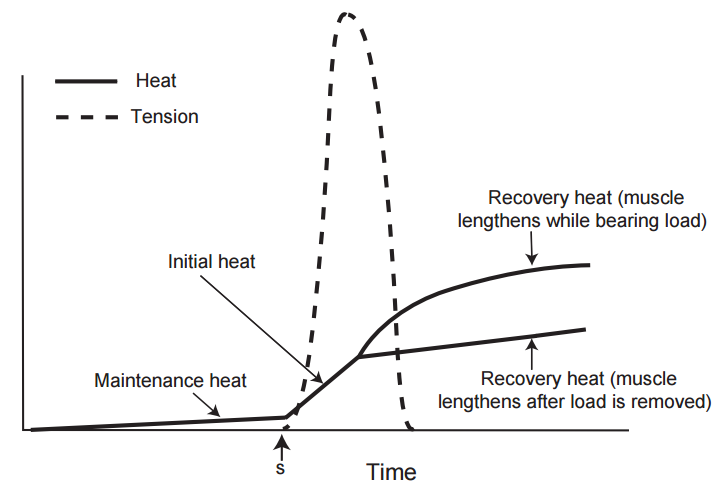
El músculo libera tres tipos de calor (Fig. 10, Tabla 2). El calor de mantenimiento (en reposo), la liberación lenta de calor por el músculo en reposo, no está relacionado con la contracción y, por lo tanto, no se considera más a fondo. Los otros dos tipos de calor, que juntos representan el calor relacionado con la actividad, se generan cuando el músculo se contrae; Estos son el calor inicial y el calor de recuperación. El calor inicial aparece durante la contracción, mientras que el calor de recuperación se libera después de que la contracción ha alcanzado su punto máximo.
Calor inicial
El primer componente del calor liberado después de la estimulación, que por razones históricas se denomina calor inicial, es el calor adicional (extra en el sentido de que excede el calor de mantenimiento) liberado durante la activación, el acortamiento y la generación de tensión (Fig. 10, Tabla 2). La siguiente descripción relaciona los procesos bioquímicos y biofísicos clave con los diferentes componentes del calor inicial. Sin embargo, esto es impreciso porque muchos procesos contribuyen a más de una fase de liberación de calor.
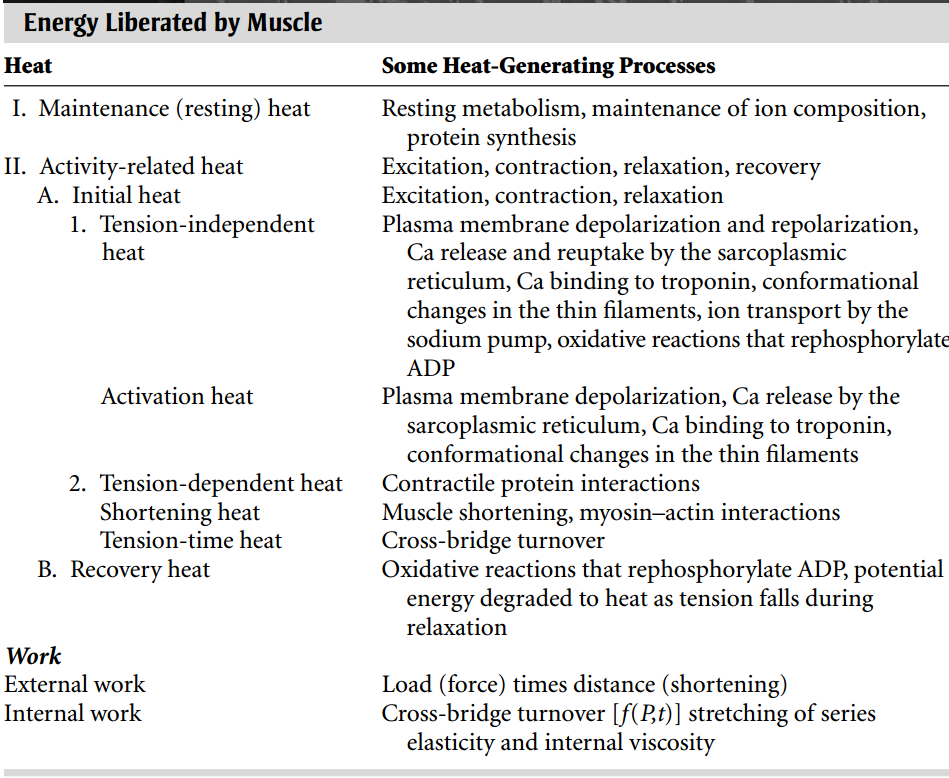
Calor de activación, calor independiente de la tensión y calor dependiente de la tensión
El calor inicial que se libera inmediatamente después de que se estimula un músculo a menudo se denomina calor de activación; la mayor parte de este calor está asociado con los flujos de iones de la membrana plasmática en el momento de la despolarización, la liberación de calcio del retículo sarcoplásmico y los cambios conformacionales entre las proteínas de los filamentos delgados que se inician cuando el calcio se une a la troponina C.
En un músculo en el que se inhiben las interacciones entre los filamentos gruesos y finos, de modo que no se puede realizar ningún trabajo externo, la estimulación sigue siendo seguida por la aparición de una pequeña cantidad de calor inicial. Este último, que representa el calor independiente de la tensión, incluye la parte del calor de activación no relacionada con las interacciones de las proteínas contráctiles, junto con el calor liberado durante los procesos que finalizan la activación, incluida la repolarización de la membrana plasmática, la recaptación de calcio activador por el retículo sarcoplásmico, el transporte de iones por la bomba de sodio que restaura los gradientes de reposo para el sodio y el potasio a través de la membrana plasmática. y la refosforilación de ADP por metabolismo oxidativo.
El calor dependiente de la tensión, que es la diferencia entre el calor inicial total y el calor independiente de la tensión, se debe principalmente a las interacciones entre los puentes cruzados de miosina en los filamentos gruesos y la actina en los filamentos delgados.
Recuperación de calor
El calor de recuperación, la mayor parte del cual se genera mediante procesos que restauran el estado del músculo contraído al que existía antes de la excitación, juega un papel importante en la determinación de la eficiencia muscular. En el músculo esquelético, gran parte de este calor se debe a la oxidación del lactato producido durante la actividad, mientras que parte del calor de recuperación producido por el músculo cardíaco está relacionado con la refosforilación de ADP por parte de las mitocondrias.
Una gran cantidad adicional de calor de recuperación aparece cuando se permite que un músculo se relaje mientras soporta un peso (Fig. 10). Este calor extra, que es proporcional a la carga, se genera por la disipación de la energía potencial almacenada por las elasticidades dentro del músculo contraído; por esta razón, el calor de recuperación se reduce si la carga se elimina del músculo antes de que comience a relajarse (Fig. 10). En el corazón, la disipación de la energía potencial almacenada por las elasticidades en las paredes del ventrículo contraído contribuye en gran medida al calor de recuperación y, por lo tanto, reduce la eficiencia cardíaca. Sin embargo, el calor de recuperación disminuye mediante el cierre de las válvulas aórtica y pulmonar, lo que reduce la tensión de la pared ventricular a medida que el corazón comienza a relajarse al aislar los ventrículos relajantes de la sangre bajo presión en la aorta y la arteria pulmonar. El calor de recuperación en el corazón también se reduce por la disminución de la tensión de la pared que normalmente ocurre durante la eyección.
Liberación de calor inicial durante la contracción isométrica
Dos componentes del calor inicial se liberan en una contracción isométrica (Fig. 11). El primero, que aparece inmediatamente después de que se estimula el músculo, es el calor de activación descrito anteriormente (A, Fig. 11). Se libera calor adicional cuando se mantiene la tensión isométrica [f(P,t) en la Fig. 11]; esto se denomina calor en tiempo de tensión, y se asocia con el trabajo interno (Wi).

Por lo tanto, la energía total liberada (ΔE) durante una contracción isométrica se describe mediante la siguiente ecuación:
ΔE = A + Wi
El trabajo interno se realiza durante una contracción isométrica porque, aunque los extremos del músculo están fijos y la longitud total del músculo no puede disminuir, las proteínas contráctiles estiran la elasticidad de la serie y provocan cambios de forma en el músculo. Además de la energía asociada con el trabajo interno que aparece como calor de tensión-tiempo, la energía potencial generada por el estiramiento de la elasticidad en serie durante la realización del trabajo interno se convierte en calor de recuperación al final de la contracción isométrica, cuando la tensión se disipa y la elasticidad se acorta.
Liberación de calor inicial durante la contracción isotónica
La energía de una contracción isotónica, en la que se permite que el músculo se acorte, es más compleja que la de una contracción isométrica porque el cambio de longitud libera dos formas adicionales de energía. El primero es el trabajo externo que se realiza cuando se permite que un músculo cargado se acorte. El segundo componente adicional del calor inicial está determinado por el grado de acortamiento muscular, por lo que se denomina calor de acortamiento.
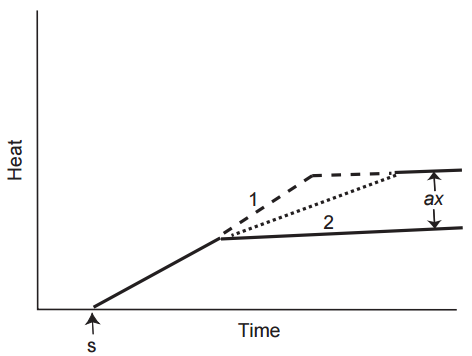
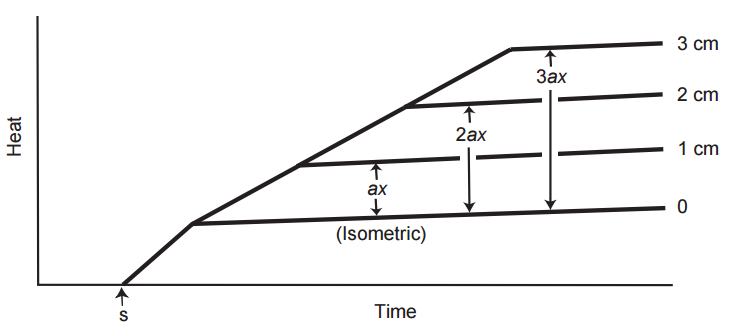
En 1938, Hill descubrió que el acortamiento de un músculo activado va acompañado de la liberación de una pequeña cantidad de calor adicional (hacha etiquetada en la Fig. 12). Este es el calor de acortamiento, que es independiente de la carga pero proporcional a la distancia que acorta el músculo (x). Si al músculo se le presentan diferentes cargas y se le permite acortar una distancia fija, la cantidad total de calor de acortamiento permanece igual, pero la velocidad a la que aparece este calor disminuye con el aumento de la carga (Fig. 12). Cuando se permite que el músculo acorte diferentes distancias con la misma carga, la cantidad de calor de acortamiento aumenta proporcionalmente con la extensión del acortamiento (Fig. 13).
Para analizar estos hallazgos, Hill introdujo el término a para cuantificar la cantidad de calor liberado por centímetro de manteca. Esta cantidad, que es constante para un músculo dado, tiene las dimensiones de una fuerza, de modo que a por x (la distancia que el músculo acorta) es la cantidad total de calor liberado durante el acortamiento:
Acortamiento del calor = ax
A diferencia de la cantidad de calor de acortamiento liberada en una contracción isotónica, que depende de la distancia acortada pero es independiente de la carga, la velocidad a la que se genera el calor de acortamiento es inversamente proporcional a la carga. Debido a que la velocidad a la que el músculo se acorta también es inversamente proporcional a la carga (Fig. 9), la tasa de liberación total de energía, como trabajo y calor, disminuye con cargas más pesadas.
La energía total liberada durante una contracción isotónica (E) incluye el trabajo externo (We), el trabajo interno (Wi), el calor de activación (A) y el calor de acortamiento (ax), de modo que:
ΔE = A + Wi + ax + We
A diferencia de una contracción isométrica, donde solo se realiza trabajo interno, la mayor parte del trabajo en una contracción isotónica es el trabajo externo gastado para levantar la carga (We).
Tensión-tiempo de calor
Las mediciones mejoradas de la liberación de calor durante la década de 1960 mostraron que tanto el calor de activación (A) como el calor de acortamiento (ax) aumentan con cargas más altas. Una interpretación simple de estos hallazgos fue proporcionada por Mommaerts (1969), quien separó el calor de activación en dos componentes: A y f(P,t). El primer componente, A, es el calor de activación descrito anteriormente (Tabla 2). El segundo término, f(P,t), representa un «calor tensión-tiempo» cuya magnitud es proporcional a la tensión en el músculo (P) y al tiempo (t) que se mantiene la tensión.
La principal fuente de calor en tiempo de tensión es el ciclo lento de los puentes cruzados de miosina unidos a actina en el músculo activado. Debido a que gran parte del calor liberado como f(P,t) está relacionado con el trabajo interno, este término puede reemplazar a Wi en la Ecuación 1. Por lo tanto, la energía liberada durante una contracción isométrica es:
ΔE = A + f(P,t)
Y la ecuación para una contracción isotónica, (Ecuación [3]), se convierte en:
ΔE = A + We + ax + f(P,t)
El calor en tiempo de tensión [f(P,t)] juega un papel importante en las consecuencias energéticas de los cambios en la actividad de la miosina ATPasa causados por alteraciones en esta molécula, como los cambios en las isoformas de la cadena pesada de la miosina. Por ejemplo, la sobrecarga hemodinámica crónica, como ocurre en la hipertensión y la estenosis aórtica, favorece la síntesis de una miosina baja en ATPasa que deprime la contractilidad miocárdica al ralentizar el ciclo de los puentes cruzados de miosina unidos a actina. Al mismo tiempo, sin embargo, este cambio aumenta la eficiencia al reducir el calor de tensión-tiempo [f(P,t)]. Este último representa un importante mecanismo adaptativo porque los corazones crónicamente sobrecargados generalmente están hambrientos de energía.
El calor tensión-tiempo, f(P,t), no se incluye en la siguiente discusión de la ecuación de Hill. Aunque esta simplificación introduce un error menor, aclara las relaciones sobresalientes entre la fuerza, la velocidad, la liberación de energía y la química de las proteínas contráctiles.
La ecuación de Hill
La ecuación de Hill, que describe la energía de la contracción muscular, relaciona la liberación de energía extra en forma de trabajo y calor con la química del proceso contráctil. Esta ecuación se basa en la energía de la contracción isotónica, donde un músculo levanta una carga (P) a una distancia (x). La cantidad de energía extra liberada durante el acortamiento aparece como trabajo externo (Px que es el mismo que We) y calor de acortamiento (ax), de modo que:
Energia extra = (Px) + (ax) = (P + a) x
El calor de activación, que aparece antes de que el músculo comience a acortarse (Fig. 11), no se incluye en la ecuación anterior porque, cuando se ignora f(P,t), no se ve influenciado por la cantidad de trabajo realizado.
La velocidad a la que se libera energía adicional durante el acortamiento se puede calcular diferenciando la cantidad (P + a) x con respecto al tiempo:
Tasa de liberación de energía extra = (P + a) dx/dt
Debido a que dx/dt = velocidad de acortamiento (v), la tasa de liberación de energía adicional es (P + a) v. Esto permite reescribir la ecuación anterior de la siguiente manera:
Tasa de liberación de energía extra = (P + a) v
Hill encontró experimentalmente que la tasa de liberación de energía adicional descrita en la ecuación anterior disminuye con el aumento de la carga, y es una función lineal directa de P0 – P, la diferencia entre la tensión isométrica máxima (P0) y la carga real (P) (Fig. 14). En una contracción isométrica, donde P = P0 y la distancia acortada (x) es cero, la tasa de liberación de energía adicional es cero porque no hay calor de acortamiento (eje) ni trabajo (Px). La tasa de liberación de energía adicional es máxima en una contracción isotónica sin carga, donde P = 0, porque aunque el trabajo (Px) es cero, tanto la distancia acortada (x) como la liberación de calor acortante (ax) son grandes. Esta es la razón por la que, a medida que la carga (P) se hace más pequeña, la tasa de liberación de energía adicional aumenta (Fig. 14).
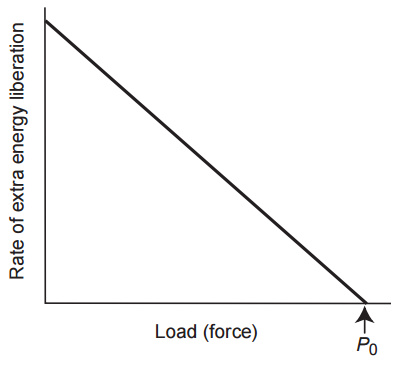
La proporcionalidad lineal directa entre la tasa de liberación de energía extra [(P + a) v] y la diferencia entre la tensión isométrica máxima y la carga real (P0 – P) mostrada en la Figura 14 se puede describir mediante la siguiente ecuación:
(P + a) v = b (P0 – P)
donde b es una constante de proporcionalidad. Reorganizando la ecuación anterior para poner todas las constantes (a, b, P0) a la derecha genera la ecuación de Hill:
(P + a) (v + b) = (P0 + a) b
Debido a que P y v, las únicas dos variables, se expresan como un producto a la izquierda, y todos los términos a la derecha son constantes, la ecuación anterior describe una hipérbola (x por y = constante). Por esta razón, un gráfico de la ecuación de Hill que traza la tasa de liberación de energía adicional [(P + a) v] como una función inversa de la carga (P0 P), produce una curva hiperbólica (Fig. 15).

Las curvas de fuerza-velocidad basadas en las mediciones de Hill del calor y el trabajo (Fig. 3-15) tienen la misma forma hiperbólica que las relaciones fuerza-velocidad obtenidas por Fenn y Marsh una década antes (Fig. 9). La similitud entre estas mediciones directas y las basadas en la ecuación de Hill demuestra que la relación hiperbólica entre la fuerza y la velocidad es una expresión de las propiedades fundamentales de la química muscular.
Importancia de la ecuación de Hill
El lector que se ha esforzado por leer los conceptos (y el álgebra) descritos anteriormente tiene derecho a preguntarse cómo estas características de la física muscular (carga, energía, producción de calor, velocidad, etc.) ayudan a comprender la fisiología del corazón. Llegados a este punto, se responde a esta pregunta en términos generales. La importancia de la ecuación fue elocuentemente expresada por Hill (1938), quien proporcionó una predicción notable con respecto a la química del músculo en funcionamiento:
«El control ejercido por la tensión P existente en el músculo en cualquier momento, sobre la tasa de su gasto de energía en ese momento, puede deberse a algunos de los siguientes mecanismos. Imaginemos que las transformaciones químicas asociadas con el estado de actividad en el músculo ocurren por combinación en, o por el efecto catalítico de, o tal vez por el paso a través de, ciertos puntos activos en la maquinaria molecular, el número de los cuales está determinado por la tensión existente en el músculo en ese momento. Podemos imaginar que cuando la fuerza en el músculo es alta, las afinidades de más de estos puntos están siendo satisfechas por las atracciones que ejercen unos sobre otros, y que menos de ellos están disponibles para participar en la transformación química. Cuando la tensión es baja, las afinidades de menos de estos puntos están siendo satisfechas por atracción mutua, y más de ellos están expuestos a la reacción química. La velocidad a la que ocurriría la transformación química y, por lo tanto, a la que se liberaría la energía, sería directamente proporcional al número de afinidades expuestas o grupos catalíticos, y por lo tanto sería una función lineal de la fuerza ejercida por el músculo, aumentando a medida que la fuerza disminuye.»
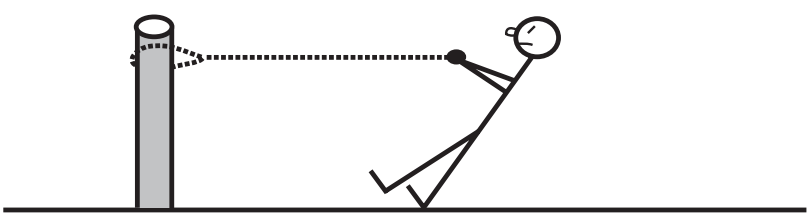
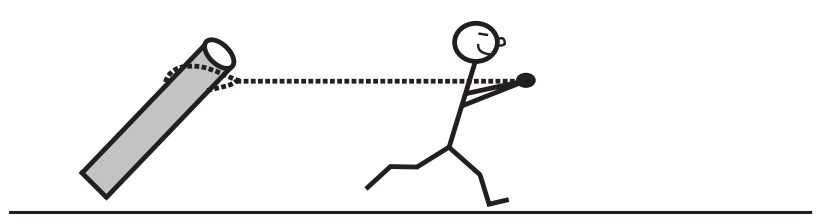
La declaración de Hill, escrita cuando prácticamente no se sabía nada de la bioquímica de las proteínas contráctiles y un año antes de que se descubriera que la miosina era una enzima ATPasa, explica la energética de la contracción muscular en términos de interacciones entre hipotéticos «puntos activos» dentro del músculo. Para explicar la relación inversa entre la carga y la tasa de liberación de energía adicional (Fig. 14), Hill postuló que los puntos activos pueden existir en cualquiera de los dos estados. En uno, los puntos activos están unidos y así mantienen la tensión, como cuando un hombre tira de una cuerda que está firmemente anclada a un poste (Fig. 16); en el otro, todos los puntos activos son libres de liberar energía química y, por lo tanto, circulan a su velocidad máxima, ya que cuando se tira del poste del suelo, el hombre puede correr a su velocidad máxima (Fig. 17).
La relación inversa entre la carga y la tasa de liberación de energía adicional (Fig. 14) refleja los efectos de la carga en la distribución de los puntos activos entre los estados adjunto y libre. En una contracción isométrica, donde la tensión es máxima (P = P0), todos los puntos activos se unen en el estado en el que desarrollan tensión (Fig. 18); En estas condiciones, la fuerza es máxima y la tasa de liberación de energía es cero. Aunque se debe gastar energía para alcanzar este estado, que explica el calor de activación (Fig. 11), no es necesario gastar energía adicional para mantener la tensión. En la contracción descargada, donde P = 0, el músculo se acorta a su velocidad máxima porque todos los puntos activos son libres de circular a su velocidad máxima (Fig. 19).


Eficiencia y calor-tiempo de tensión
La discusión anterior se simplifica porque asume que una vez que se ha desarrollado la tensión durante una contracción isométrica, todos los puntos activos permanecen unidos y no experimentan más movimiento. Sin embargo, esto no es correcto; en cambio, una rotación lenta de puntos activos durante una contracción isométrica genera el calor tensión-tiempo f(P,t) descrito en las ecuaciones [4] y [5]; en términos antropomórficos, esto es como si los «hombrecitos» de la Figura 18 ocasionalmente movieran sus pies.
Ahora sabemos, por supuesto, que los puntos activos en el músculo no son hombres pequeños, sino que son interacciones entre los puentes cruzados de miosina y la actina. Esto explica el calor tensión-tiempo f(P,t), que se produce cuando las interacciones entre los puentes cruzados en los filamentos gruesos y la actina en los filamentos finos circulan entre los estados unidos y separados. El ciclo ocurre a una velocidad proporcional a la tasa intrínseca de liberación de energía por las proteínas contráctiles, que se puede medir in vitro como actividad de la miosina ATPasa. La velocidad a la que el calor-tensión-tiempo desperdicia energía durante una contracción isométrica es mayor en los músculos con alta actividad de miosina ATPasa porque la tasa de recambio intrínseco de los puentes cruzados de miosina in vivo refleja las mismas propiedades que determinan la actividad de la miosina ATPasa in vitro.
Los músculos rápidos, que contienen una miosina ATPasa alta, se contraen más eficientemente cuando están ligeramente cargados que los músculos lentos, pero son menos eficientes para mantener la tensión. Los músculos lentos, aunque se acortan menos rápidamente, mantienen la tensión de manera más eficiente porque la velocidad de ciclo más lenta entre puentes desperdicia menos energía en forma de calor en el tiempo de tensión. Volviendo a la analogía de los hombrecitos, a un corredor más rápido le resulta más fácil levantar los pies del suelo, como el rápido desprendimiento de las interacciones entre el puente de miosina y la actina, por lo que es más eficiente cuando corre libremente. Por el contrario, un atleta más lento, cuyos pies permanecen en el suelo durante más tiempo, es más eficiente cuando tira de una cuerda atada. En pocas palabras, un atleta que usa zapatos de plomo corre más lento y menos eficiente, pero usa menos energía cuando se le pide que tire de una cuerda atada, en comparación con un corredor más rápido que usa los zapatos alados de Hermes.
P0 y Vmax: Las intersecciones de la curva fuerza-velocidad
La ecuación de Hill predice que la velocidad de acortamiento de un músculo descargado (Vmax) es independiente del número de puntos activos; esto es evidente por la analogía de los hombrecitos porque un corredor capaz de una velocidad máxima de 10 mph tirará de una cuerda descargada a la misma velocidad que tres (o cualquier número) de tales corredores unidos entre sí (Figs. 17 y 19). Esta es la razón por la que Vmax refleja la velocidad intrínseca del recambio de puente cruzado de miosina (que es proporcional a la actividad de la miosina ATPasa), y es independiente del número de interacciones entre los filamentos gruesos y delgados. De acuerdo con la ecuación de Hill, la otra intersección de la curva fuerza-velocidad, la fuerza máxima generada durante una contracción isométrica (P0), está determinada por el número de puntos activos en el músculo. De acuerdo con la analogía de los hombrecitos (Figs. 16 y 18), P0 depende del número de hombres que tiran de la cuerda y no de la velocidad a la que puede correr cada uno cuando la carga es cero. Por lo tanto, P0 es independiente de la tasa máxima de gasto energético, reflejando en cambio el número de interacciones activas entre los puentes cruzados de miosina y la actina, que en el corazón está determinada en gran medida por la cantidad de calcio activador unido a la troponina C.
Los elegantes análisis de la energía del músculo sartorio de rana tetanizado descritos anteriormente no se pueden llevar a cabo en el corazón, donde el estado activo es de inicio lento y cambia a lo largo del ciclo cardíaco. La opinión una vez prevaleciente de que Vmax es un índice válido de contractilidad ha tenido que ser abandonada porque los cambios en el suministro de calcio a las proteínas contráctiles, el principal mecanismo que regula la contractilidad miocárdica, determinan el número de interacciones entre los puentes cruzados de miosina y la actina, en lugar de su tasa de recambio, por lo que se esperaría que modificara principalmente P0 y tuviera poco o ningún efecto sobre Vmax. Por otro lado, la identificación de un número creciente de cambios moleculares que cambian el desarrollo de la tensión y acortan la velocidad en los corazones indecisos ha aumentado la importancia clínica de estos conceptos en las enfermedades humanas.