Resumen
El shock distributivo y el síndrome de distrés respiratorio agudo (SDRA) son síndromes de profunda complejidad fisiopatológica, cada uno asociado independientemente con alta morbilidad y mortalidad. Cuando coexisten, crean un estado de insuficiencia cardiopulmonar sinérgica donde los enfoques de manejo convencionales y protocolizados suelen ser insuficientes. Esta revisión sintetiza los conocimientos actuales sobre los mecanismos de interacción cardiopulmonar en el shock distributivo con SDRA, destacando el papel central del acoplamiento ventrículo derecho-arteria pulmonar y el doble impacto de la alteración de la mecánica pulmonar y la desregulación vascular. Examinamos las distintas implicaciones hemodinámicas de los fenotipos pulmonares y extrapulmonares del SDRA, incluyendo sus efectos divergentes sobre la presión transpulmonar, el retorno venoso y la poscarga ventricular derecha, y enfatizamos la relevancia clínica de los fenotipos mixtos. Las modalidades avanzadas de monitorización (manometría esofágica, ecocardiografía y, en casos selectos, cateterismo de la arteria pulmonar) se presentan como herramientas esenciales para la fenotipificación dinámica y la titulación individualizada de las estrategias ventilatorias y hemodinámicas. Basándonos en estos principios, describimos enfoques basados en el fenotipo para la ventilación, la terapia de fluidos y vasoactiva, e intervenciones complementarias como la posición prona y el soporte extracorpóreo. Finalmente, analizamos las lagunas de conocimiento y las futuras direcciones, subrayando la necesidad de tecnologías integrativas y ensayos con estratificación por fenotipo para perfeccionar el manejo de precisión. La integración matizada de la fisiología cardiopulmonar en la toma de decisiones a pie de cama representa un cambio de paradigma hacia la atención individualizada y guiada por la fisiología para esta población de alto riesgo.
Introducción
El shock distributivo, comúnmente de origen séptico, y el síndrome de dificultad respiratoria aguda (SDRA) son síndromes formidables que, por sí solos, conllevan una morbilidad y mortalidad considerables en la unidad de cuidados intensivos (UCI). Cuando coexisten, crean un estado de extremo riesgo fisiológico donde las agresiones no son meramente aditivas, sino profundamente sinérgicas y mecanicistas. Los datos actuales siguen reportando altas tasas de mortalidad para esta afección combinada, que a menudo superan el 40-50% en cohortes multicéntricas, especialmente cuando se complica con vasoplejía refractaria o cor pulmonale agudo. El manejo de estos pacientes ejemplifica los matices de la fisiología aplicada a los cuidados críticos, exigiendo que el clínico actúe como un fisiólogo en tiempo real junto a la cama. Históricamente, las estrategias de manejo han evolucionado desde un enfoque en la normalización de las variables fisiológicas individuales hasta una filosofía más integral de protección de los órganos. Los primeros protocolos de terapia dirigida a objetivos para la sepsis buscaban optimizar objetivos hemodinámicos específicos. De manera similar, el emblemático ensayo ARMA estableció la ventilación con bajo volumen corriente como el estándar de atención para el SDRA, centrando la atención en la mitigación de la lesión pulmonar inducida por el ventilador. Sin embargo, un enfoque único ha demostrado ser inadecuado para la fisiopatología compleja y altamente variable del shock con SDRA. El uso rutinario de herramientas invasivas como el catéter de arteria pulmonar (AP), por ejemplo, no demostró un beneficio en la supervivencia en poblaciones amplias, lo que condujo a una disminución en su uso, pero también destacó la necesidad de una aplicación más específica en casos selectos y complejos donde se deben responder preguntas fisiológicas específicas.
Esta evolución ha dado lugar a la era actual, que enfatiza la medicina personalizada basada en una profunda comprensión mecanicista. La piedra angular de este enfoque es reconocer que la ventilación con presión positiva, si bien salva vidas, es una potente intervención hemodinámica. Sus efectos cíclicos y tónicos sobre la presión intratorácica influyen dinámicamente en el retorno venoso, las condiciones de carga biventricular y la interdependencia ventricular latido a latido. En consecuencia, ajustes aparentemente menores en la configuración del respirador o en las infusiones de fármacos vasoactivos pueden precipitar consecuencias hemodinámicas desproporcionadas, a menudo catastróficas, que con frecuencia culminan en insuficiencia ventricular derecha (VD) aguda. Comprender estas complejas interacciones es esencial para evitar daños iatrogénicos y adaptar el tratamiento a la fisiología única de cada paciente.
Esta revisión reexamina los mecanismos fundamentales de las interacciones cardiopulmonares en el shock distributivo combinado y el SDRA, destacando el papel fundamental del fenotipado hemodinámico para optimizar las estrategias terapéuticas que preservan simultáneamente la función pulmonar y el rendimiento del VD.
La fisiopatología entrelazada
La coexistencia del shock distributivo y el SDRA crea un círculo vicioso de daño orgánico. La inflamación sistémica de la sepsis provoca daño endotelial, degradación del glucocáliz y trombosis microvascular, procesos que se amplifican en la delicada circulación pulmonar. Esta patología compartida se ve sometida a las complejas y a menudo opuestas fuerzas mecánicas de la ventilación con presión positiva, que pueden mantener o destruir la estabilidad cardiovascular según la mecánica subyacente.
Mecánica pulmonar alterada y el concepto de poder lesivo
La mecánica alveolar en el SDRA se define por una profunda heterogeneidad. El pulmón se transforma en un mosaico de regiones dependientes colapsadas y llenas de líquido, y regiones no dependientes relativamente preservadas y aireadas. Esto da lugar al concepto de «pulmón bebé», donde el pulmón funcional y ventilado es mucho más pequeño que el pulmón anatómico. Las unidades dependientes sufren atelectasia cíclica (reclutamiento y desreclutamiento con cada respiración), lo que genera esfuerzo cortante e inflamación (atelectrauma), mientras que las unidades no dependientes son susceptibles a la sobredistensión (volutrauma), especialmente al aumentar la presión positiva al final de la espiración (PEEP). Esta heterogeneidad es la base de dos conceptos cruciales en el manejo moderno de los ventiladores: la presión de conducción (ΔP) y la potencia mecánica (PM).
La presión de conducción, definida como la presión meseta menos la PEEP, representa la deformación cíclica aplicada al parénquima pulmonar. Un análisis post hoc clave reveló que la ΔP, y no el volumen corriente ni la PEEP por sí solos, fue la variable más fuertemente asociada con la supervivencia en el SDRA. Fisiológicamente, es el predictor más potente de insuficiencia ventricular derecha (VD) relacionada con el ventilador, ya que el cambio cíclico en la presión transpulmonar (PTP = Paw − Ppl) determina el grado de compresión alveolocapilar durante la inspiración, un factor importante en la poscarga pulsátil que enfrenta el ventrículo derecho.
El concepto de MP integra múltiples componentes lesivos (es decir, volumen corriente, frecuencia respiratoria, ΔP y flujo inspiratorio) en una única variable que representa la energía transferida del ventilador al sistema respiratorio por minuto. Una MP elevada se ha relacionado tanto con la lesión pulmonar como con la disfunción ventricular derecha. Esto pone de relieve que una estrategia aparentemente «protectora» con un volumen corriente bajo puede ser perjudicial si la frecuencia respiratoria es excesivamente alta. El reto actual es normalizar la MP al tamaño del pulmón artificial aireado, ya que la misma potencia suministrada a un pulmón funcional más pequeño es, sin duda, más perjudicial.
La vasculatura sistémica y pulmonar desregulada
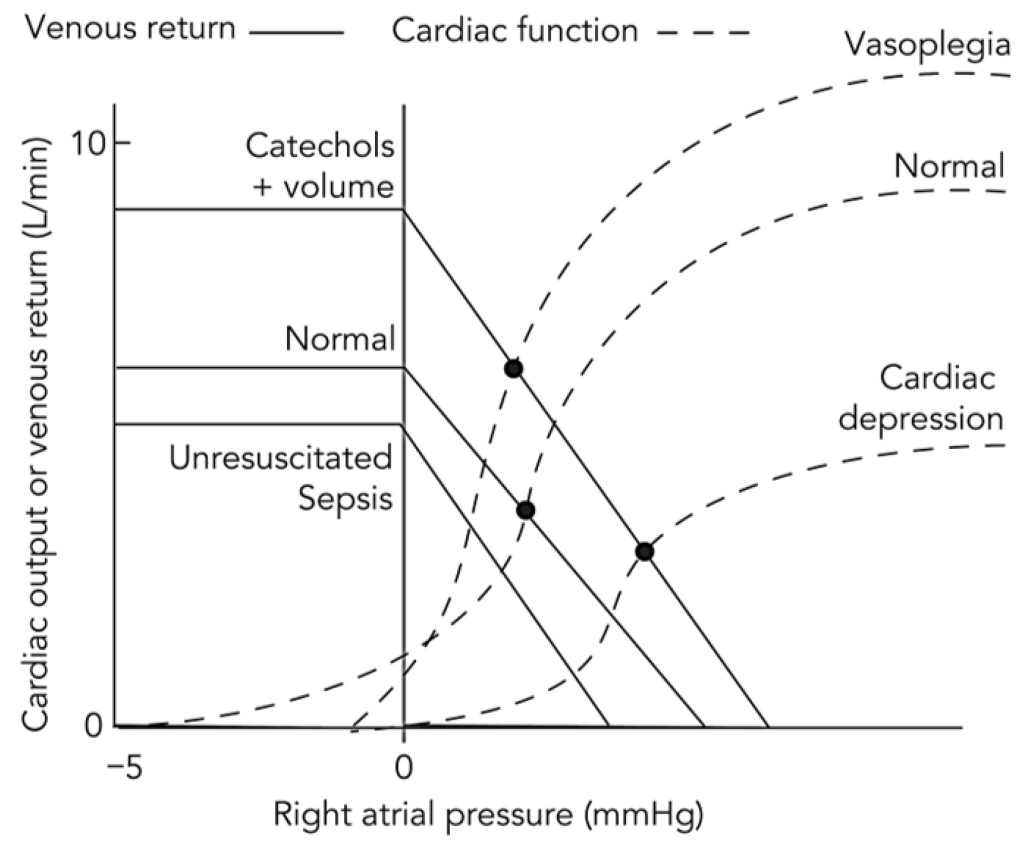
El tono vascular, tanto en el circuito sistémico como en el pulmonar, se desregula profundamente durante el shock distributivo. La liberación de mediadores vasodilatadores, como el óxido nítrico y las prostaglandinas, provoca una marcada vasodilatación sistémica, que reduce la resistencia vascular sistémica (RVS) y aumenta considerablemente la capacitancia venosa. Esto resulta en un estado de hipovolemia relativa. En el marco del modelo de equilibrio circulatorio de Guyton, esta vasodilatación generalizada, junto con la fuga capilar, disminuye la presión media de llenado sistémico (PMSF), que representa la presión ascendente que impulsa el retorno venoso (Figura 1). Conceptualmente, la PMSF es la presión teórica en todo el sistema circulatorio si el corazón se detuviera, lo que refleja la retracción elástica de la vasculatura que actúa sobre el volumen sanguíneo contenido. El retorno venoso al corazón depende del gradiente de presión entre esta PMSF ascendente y la presión auricular derecha (PRA) descendente. A medida que la PMSF disminuye, este gradiente (PMSF − PRA) disminuye, lo que hace que el paciente sea profundamente dependiente de la precarga.
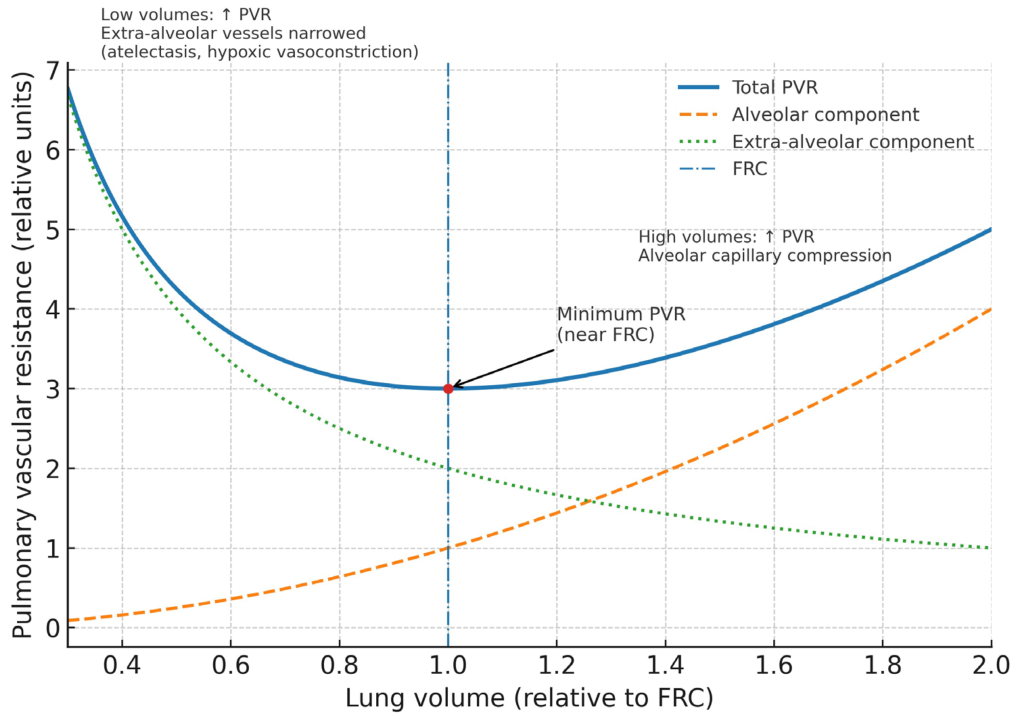
En marcado contraste, la circulación pulmonar se convierte en un circuito de alta resistencia e impedancia, y la relación entre el volumen pulmonar y la resistencia vascular pulmonar (RVP) se describe mediante una curva en forma de U. La resistencia vascular pulmonar se minimiza cerca de la capacidad residual funcional normal. A volúmenes pulmonares bajos, la atelectasia y la tortuosidad vascular aumentan la resistencia en los vasos extraalveolares, una situación exacerbada por la vasoconstricción pulmonar hipóxica, mientras que a volúmenes pulmonares altos, los alvéolos distendidos estiran y comprimen los delicados capilares intraalveolares, lo que aumenta notablemente la RVP (Figura 2). Esta compresión mecánica se ve agravada por la patología vascular intrínseca: la lesión endotelial generalizada, la formación de microtrombos y un entorno inflamatorio desregulado mitigan la respuesta fisiológica de vasoconstricción pulmonar hipóxica en las regiones pulmonares más consolidadas. Esto tiene el efecto desastroso de aumentar la perfusión a unidades pulmonares no ventiladas que producen shunts, lo que empeora la hipoxemia sistémica mientras otros segmentos vasculares sufren una vasoconstricción profunda, aumentando así aún más la RVP general.
Fenotipos del SDRA: la piedra angular del manejo hemodinámico
Un avance fundamental en el manejo de la hemodinámica del SDRA es la descomposición del síndrome en fenotipos distintos según la localización primaria del trastorno mecánico. La distinción clásica entre SDRA pulmonar (ARDSp) y SDRA extrapulmonar (ARDSexp) no es meramente etiológica; tiene implicaciones profundas, predecibles y a menudo opuestas para las interacciones cardiopulmonares bajo ventilación con presión positiva. El comportamiento mecánico del sistema respiratorio se rige por la relación entre la compliancia pulmonar (CL) y la pared torácica (CCW). El cambio en la presión pleural (Ppl) durante una respiración mecánica pasiva no está determinado por la compliancia total del sistema respiratorio, sino casi exclusivamente por la CCW, según la ecuación fundamental: ΔPpl = ΔVolumen/CCW. Esta simple pero profunda relación dicta el destino hemodinámico del paciente.
SDRA pulmonar
Este fenotipo, derivado de lesiones directas como neumonía o aspiración, se caracteriza por una densa consolidación alveolar y una marcada reducción de la LC, mientras que el CCW suele conservarse y mantenerse relativamente alto. En consecuencia, la mayor parte de la presión aplicada en la vía aérea se transmite a través del parénquima pulmonar rígido, lo que genera una PTP peligrosamente elevada. Aunque la presión alveolar aumenta considerablemente en este contexto, la baja distensibilidad parenquimatosa típica del «pulmón rígido» limita el grado de transmisión de esta presión al espacio pleural. En consecuencia, el retorno venoso tiende a permanecer relativamente conservado a pesar del grave aumento de la PTP, una distinción que subraya la disociación entre el estrés alveolar y la transmisión de la presión intratorácica en este fenotipo. Esta PTP notablemente elevada comprime la microvasculatura pulmonar, lo que provoca un aumento brusco de la poscarga del ventrículo derecho.
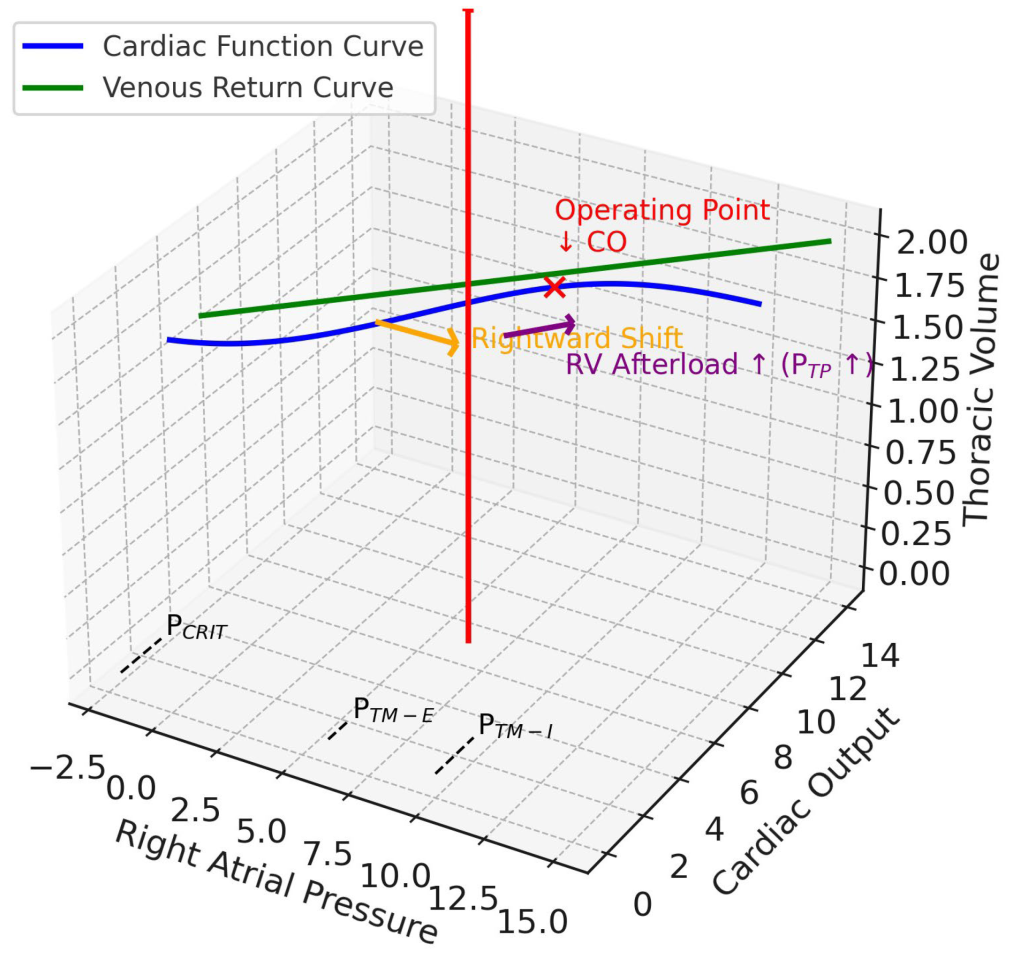
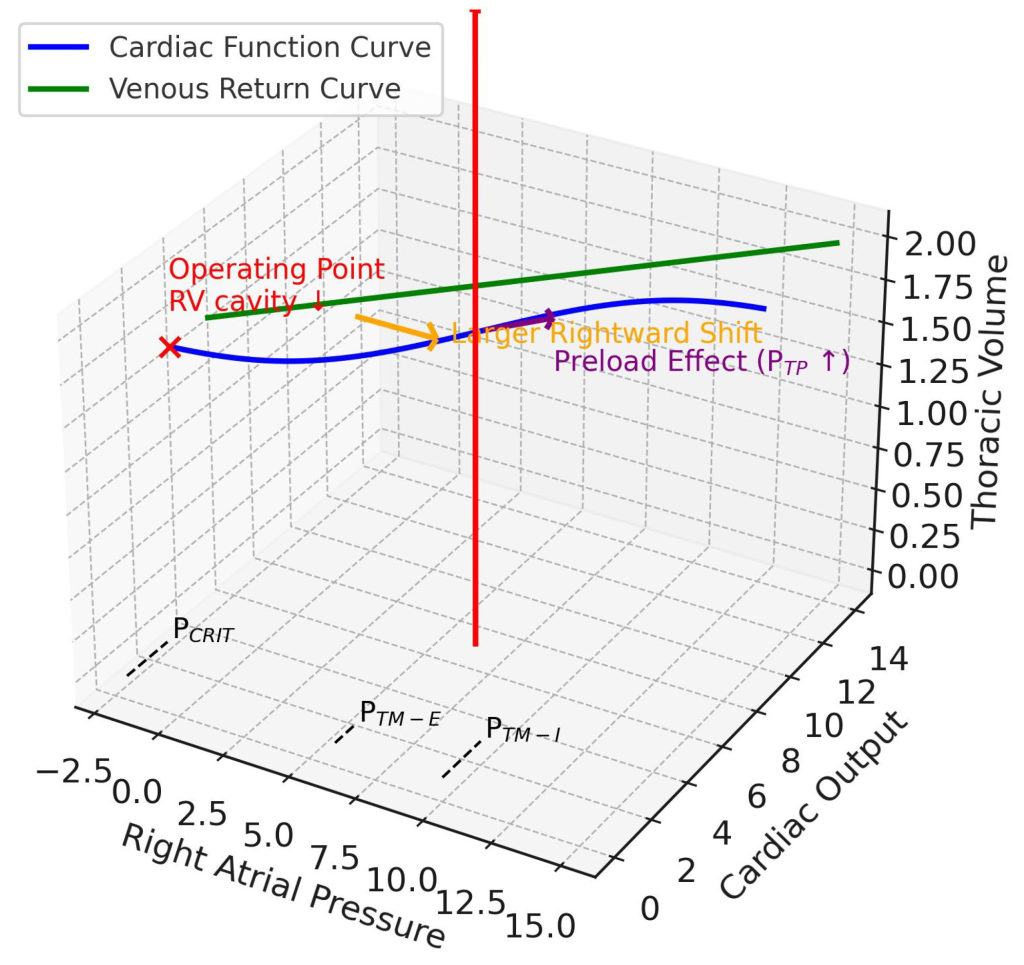
En este fenotipo de «pulmón rígido», el paciente es muy susceptible a la insuficiencia del ventrículo derecho con predominio de la poscarga. Es importante destacar que es el aumento resultante del volumen pulmonar, más que la elevación de la PTP per se, lo que explica muchas de las alteraciones observadas en la RVP. Esta distinción es crucial, ya que tanto la sobredistensión alveolar como el reclutamiento alteran la geometría de los vasos pulmonares, aumentando así la poscarga del VD y predisponiendo a la insuficiencia circulatoria. Dado que el cambio en la Ppl es mínimo, los efectos directos de la ventilación con presión positiva sobre el retorno venoso y la poscarga del ventrículo izquierdo (VI) son menos pronunciados. Hemodinámicamente, como se ilustra en el diagrama conceptual de Campbell-Guyton, esto se manifiesta como un marcado aplanamiento de la pendiente de la curva de función cardíaca (que refleja un aumento de la poscarga) con solo un ligero desplazamiento hacia la derecha (que indica un cambio mínimo en la precarga), lo que finalmente produce un nuevo punto de equilibrio de bajo flujo (Figura 3). Este mecanismo explica el cuadro clínico de un paciente con neumonía grave que desarrolla cor pulmonale agudo y colapso hemodinámico en respuesta a un aumento de la PEEP o el volumen corriente.
SDRA extrapulmonar
Impulsado por la inflamación sistémica de origen como la pancreatitis o la sepsis abdominal, este fenotipo se caracteriza por edema intersticial y, fundamentalmente, una reducción primaria del CCW debido a factores como la hipertensión intraabdominal, la anasarca o la obesidad. En la presente revisión, el término «SDRA extrapulmonar» se utiliza en su sentido fisiomecánico, no puramente etiológico. Si bien tradicionalmente se define como el SDRA derivado de una lesión no pulmonar (p. ej., pancreatitis, traumatismo o sepsis de origen no pulmonar), aquí denota un fenotipo mecánico en el que la reducción del CCW y la elevación de la PPL —a menudo debidas a la hipertensión intraabdominal, la anasarca o la obesidad— rigen las interacciones cardiopulmonares. Esta distinción mecanicista destaca las consecuencias hemodinámicas de la transmisión de presión desde el abdomen y la caja torácica sobre el retorno venoso y la carga del ventrículo derecho.
En este escenario de «pared torácica rígida», una respiración mecánica genera un gran aumento de la PPL porque el CCW es bajo. Esto tiene una cascada de efectos hemodinámicos. En primer lugar, la Ppl elevada se transmite directamente a las grandes venas intratorácicas y a la aurícula derecha, lo que dificulta drásticamente el gradiente de presión para el retorno venoso y causa un compromiso circulatorio con precarga dominante. Sin embargo, debido a que la Ppl aumenta sustancialmente, la PTP para cualquier presión en la vía aérea es mucho menor (pero aún mayor que en condiciones normales), lo que mitiga el efecto compresivo sobre la vasculatura pulmonar y, por lo tanto, el aumento de la poscarga del ventrículo derecho. Simultáneamente, la alta presión intratorácica envuelve el ventrículo izquierdo, disminuyendo su presión transmural y reduciendo eficazmente la poscarga del ventrículo izquierdo, lo que puede ser beneficioso en pacientes con insuficiencia cardíaca preexistente o miocardiopatía séptica. La representación guytoniana muestra un desplazamiento significativo hacia la derecha de la curva de función cardíaca (reducción de la precarga), pero un aplanamiento mucho menos pronunciado de su pendiente (aumento menos severo de la poscarga), lo que conduce a un nuevo equilibrio complejo (Figura 4).
Fenotipo mixto/alternativo de SDRA
En la práctica clínica, una proporción significativa de pacientes presenta características de ambos fenotipos, en particular tras una doble agresión (p. ej., pancreatitis complicada por una neumonía asociada a la ventilación mecánica) o durante estancias prolongadas en la UCI. Estos pacientes presentan un profundo dilema terapéutico. Experimentan una doble carga mecánica: una pared torácica rígida que impide el retorno venoso (reduciendo la precarga) y pulmones rígidos que aumentan la poscarga del ventrículo derecho (VD). Cualquier intento de reclutar el pulmón consolidado con una PEEP o ΔP más elevadas corre el riesgo de aumentar aún más la poscarga del VD debido a la Ptp elevada, a la vez que empeora la reducción de la precarga como resultado del inevitable aumento de la Ppl. Este fenotipo destaca las limitaciones críticas de las mediciones globales, como la presión meseta, y enfatiza la necesidad de una monitorización avanzada para diferenciar la mecánica respiratoria de la dinámica cardiovascular, permitiendo a los médicos gestionar estas tensiones fisiológicas competitivas (Tabla 1).
| Característica | SDRA pulmonar (ARDSp) | SDRA extrapulmonar (ARDSexp) | SDRA mixto / alternativo |
|---|---|---|---|
| Causas comunes | Neumonía, aspiración, contusión pulmonar | Infección abdominal, pancreatitis, transfusión, trauma | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Sitio primario de lesión | Epitelio alveolar | Endotelio vascular | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Imagen | Consolidación densa en lóbulos dependientes | Atelectasias difusas / edema intersticial | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Compliance pulmonar | Marcadamente reducida | Frecuentemente relativamente preservada | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Compliance de la pared torácica | Generalmente cercana a la normalidad | Reducida (obesidad, ascitis, abdomen tenso) | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Presión pleural | Normal o moderadamente aumentada | Frecuentemente marcadamente aumentada | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Presión transpulmonar | Alta para una presión plateau (Pplat) determinada | Menor para una presión plateau (Pplat) determinada | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Reclutabilidad pulmonar | Generalmente menor | Frecuentemente mayor | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Poscarga del ventrículo derecho | Aumentada (↑PTP, ↑RVP) | Menor o sin cambios (↓PTP) | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Retorno venoso | Preservado o reducido si falla el ventrículo derecho | Reducido por ↑ presión pleural (limitado por precarga) | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Enfoque del manejo | Limitar PTP/ΔP; posición prona; evitar PEEP excesiva | Controlar presión abdominal; PEEP guiada por PTP; restaurar retorno venoso | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
Abreviaturas: SDRA: síndrome de distrés respiratorio agudo; Pplat: presión plateau; VD: ventrículo derecho; PTP: presión transpulmonar; RVP: resistencia vascular pulmonar; ΔP: presión de conducción; PEEP: presión positiva al final de la espiración.
El ventrículo derecho: de la fisiología a la insuficiencia
El ventrículo derecho, una cámara de paredes delgadas y sensible al volumen, adaptada a un circuito pulmonar de baja impedancia, es el nexo central de las interacciones cardiopulmonares en el shock distributivo con SDRA. Su singular geometría semilunar y su delgada pared libre lo hacen vulnerable a aumentos agudos de la poscarga.
Acoplamiento ventrículo-arterial
Una comprensión sofisticada de la función del ventrículo derecho requiere ir más allá de los términos descriptivos simples hacia un marco biofísico riguroso conocido como acoplamiento ventricular-arterial. Este concepto evalúa la eficiencia con la que se transfiere energía del ventrículo al sistema arterial y se define por la relación entre la elastancia telesistólica (Ees) y la elastancia arterial efectiva (Ea).
La elastancia telesistólica representa la medida más precisa, independiente de la carga, de la contractilidad miocárdica intrínseca o inotropía. Se define por la pendiente de la relación presión-volumen telesistólica (RPTS), una línea que conecta los puntos telesistólicos de múltiples bucles presión-volumen generados bajo diferentes condiciones de carga. Una pendiente más pronunciada refleja una mayor fuerza contráctil. Conceptualmente, la Ees puede concebirse como la rigidez ventricular o fuerza contráctil al final de la sístole, independientemente de la precarga y la poscarga (Figura 5).
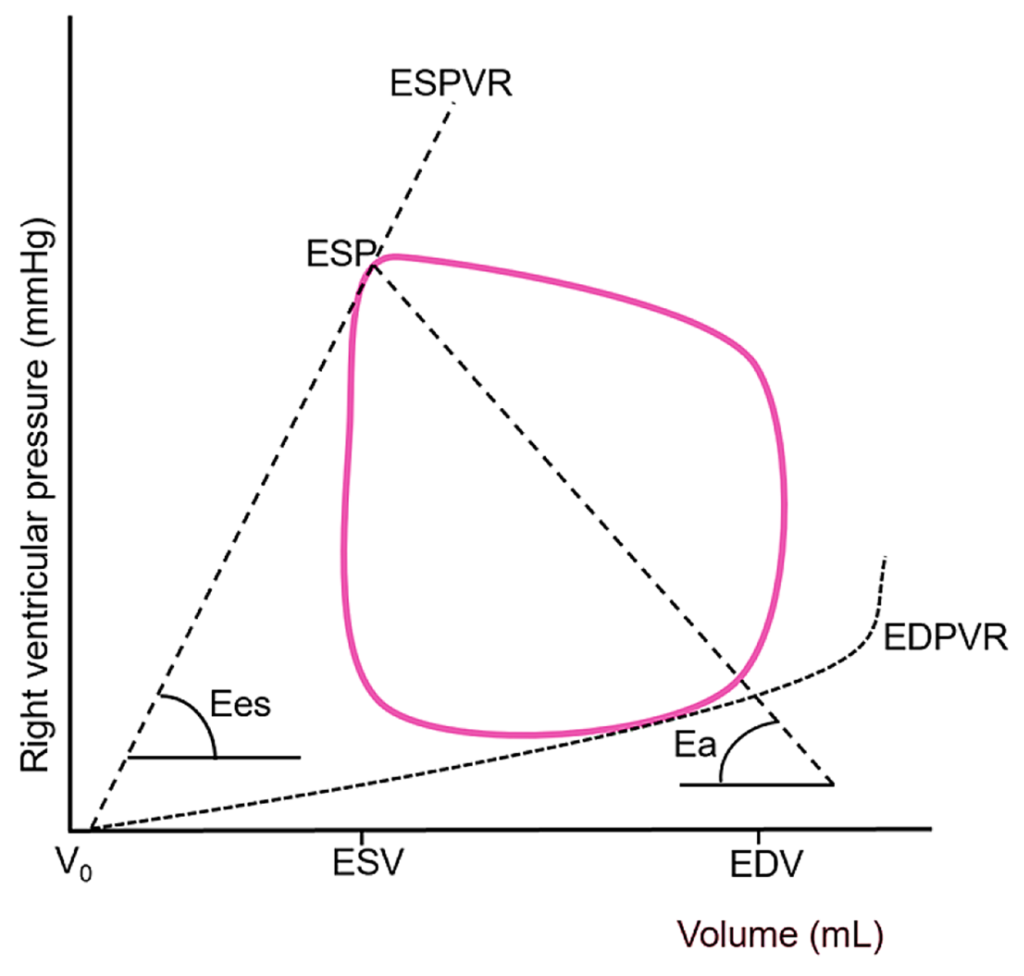
Un ventrículo sano se comporta como un resorte resiliente, capaz de generar una tensión (presión) considerable incluso con una deformación mínima (cambio de volumen). Sin embargo, en el shock séptico, la elastancia arterial efectiva (ESE) del ventrículo derecho suele reducirse notablemente debido a los mecanismos multifactoriales de la miocardiopatía inducida por sepsis, que incluyen la depresión miocárdica mediada por citocinas, la disfunción mitocondrial y la alteración de la señalización β-adrenérgica. Esta reducción resulta en una ESPVR más plana, lo que afecta significativamente la capacidad del ventrículo derecho para adaptarse al aumento de la poscarga.
La elastancia arterial efectiva (ESP/SV) es una medida integral de la poscarga total impuesta al ventrículo, calculada como el cociente entre la presión telesistólica y el volumen sistólico (ESP/SV). Abarca todos los factores que se oponen a la eyección ventricular y consta de un componente estable (resistivo) y otro pulsátil (reactivo). El componente estable es la presión arterial pulmonar (PVR), que, como se ha comentado, está notablemente elevada en el SDRA debido a una combinación de compresión mecánica, microtrombos, edema endotelial y vasoconstricción. El componente pulsátil, a menudo subestimado, también es crucial para el ventrículo derecho e incluye la compliancia de la arteria pulmonar (CPA) y la reflexión de la onda.
En condiciones normales, la circulación pulmonar presenta una alta compliancia. Sin embargo, en el SDRA, se vuelve rígida, por lo que un volumen sistólico determinado produce una presión de pulso mucho mayor, lo que aumenta la carga de trabajo pulsátil del ventrículo derecho. Además, en este sistema rígido y de alta resistencia, las ondas de presión generadas durante la sístole se reflejan desde la periferia antes, llegando al final de la sístole y oponiéndose directamente a la eyección anterior, lo que aumenta aún más la poscarga. Por lo tanto, la Ea proporciona una evaluación más completa de la poscarga ventricular que la PVR por sí sola.
Desacoplamiento ventrículo-arterial
La transferencia óptima de energía del ventrículo derecho a la circulación pulmonar ocurre cuando la relación Ees/Ea es de aproximadamente 1,5-2,0. Una relación inferior a 1,0 indica un desacoplamiento VD-AP, un estado de profunda ineficiencia bioenergética en el que el ventrículo ya no puede expulsar sangre eficazmente contra su carga, lo que provoca una rápida disminución del trabajo sistólico y, finalmente, una insuficiencia. El paciente con shock séptico y SDRA presenta un modelo fisiológico clásico de desacoplamiento inminente: la sepsis suprime activamente la Ees del VD, mientras que el SDRA y la ventilación mecánica aumentan drásticamente la Ea de la AP.
La transición de un estado acoplado a uno desacoplado suele ser precipitada, regida por un bucle vicioso de retroalimentación autoamplificadora. El ventrículo derecho se adapta inicialmente mediante el mecanismo de Frank-Starling y la adaptación homeométrica (efecto Anrep), pero estos son finitos y se ven comprometidos por la sepsis. Una vez que el ventrículo derecho se dilata más allá de un punto crítico, la Ley de Laplace dicta que la tensión de su pared aumenta exponencialmente. Este elevado estrés parietal tiene consecuencias catastróficas: altera directamente la contractilidad al sobreestirar los sarcómeros, aumenta drásticamente la demanda miocárdica de oxígeno y, simultáneamente, reduce el aporte miocárdico de oxígeno al comprimir la arteria coronaria derecha durante la diástole, todo ello en el contexto de una hipotensión sistémica. El ventrículo derecho desacoplado consume un exceso de oxígeno para un trabajo mínimo efectivo, lo que conduce a la isquemia, la insuficiencia energética y el colapso bioenergético. Esto se manifiesta clínicamente como una disminución del gasto cardíaco, un aumento de la presión venosa central (PVC) y una hipoperfusión sistémica progresiva refractaria al tratamiento convencional.
Interdependencia ventricular y restricción pericárdica
El destino hemodinámico del ventrículo izquierdo está inextricablemente ligado al ventrículo derecho a través de la interdependencia ventricular diastólica y sistólica, amplificada por el pericardio relativamente no complaciente. A medida que el ventrículo derecho, sobrecargado de presión y volumen, se dilata, el tabique interventricular compartido se aplana y se curva hacia la izquierda. Este desplazamiento septal altera directamente el llenado diastólico del VI al disminuir su compliancia efectiva, lo que lleva a una caída en el volumen telediastólico y el volumen sistólico del VI, independientemente del retorno venoso sistémico. Además, la interacción ventricular sistólica, mediante la cual la contracción del VI normalmente contribuye hasta en un 40% a la generación de presión del VD, también se ve comprometida. Esta interdependencia es un mecanismo crítico por el cual una patología pulmonar primaria y derecha se traduce directamente en insuficiencia circulatoria sistémica.
Monitoreo avanzado: de los datos al conocimiento fisiológico
Una gestión eficaz depende de ir más allá de las presiones de llenado estáticas y adoptar una monitorización avanzada para caracterizar el fenotipo subyacente y rastrear la función del ventrículo derecho en tiempo real.
Catéter de la arteria pulmonar
Aunque no se utiliza de forma rutinaria, el PAC puede ser invaluable en los casos más complejos de shock refractario o sospecha de insuficiencia del ventrículo derecho, donde es necesario responder a preguntas fisiológicas específicas. Es la única herramienta que permite la medición directa de la onda de PAP y el cálculo de la RVP, el gradiente transpulmonar (GTP) y el gradiente pulmonar diastólico (GPD). Un GPD > 7 mmHg, por ejemplo, es altamente indicativo de un componente precapilar (vasorreactivo/obstructivo) de hipertensión pulmonar, que podría ser susceptible a terapia dirigida con vasodilatadores pulmonares inhalados. La monitorización continua de la saturación venosa mixta de oxígeno (SvO₂) proporciona una evaluación en tiempo real de la adecuación global del aporte de oxígeno al consumo; una disminución de la SvO₂ suele ser el signo más temprano y sensible de descompensación inminente del ventrículo derecho e insuficiencia circulatoria.
Cabe destacar que, dado que la monitorización de Peso no está disponible en muchas UCI, el PAC ofrece una alternativa pragmática y ampliamente accesible para la fenotipificación hemodinámica avanzada. Mediante el seguimiento continuo de la PRA, la PAP media (mPAP), la presión capilar pulmonar enclavada (PCP), el gasto cardíaco y la SvO₂, el clínico puede diferenciar si la insuficiencia circulatoria está dominada por una limitación de la precarga, una poscarga excesiva del VD o una depresión miocárdica biventricular. Índices derivados como la PVR, la Cpa y la DPG añaden resolución mecanicista al cuantificar los componentes estable, pulsátil y microvascular de la poscarga del VD.
Para una interpretación práctica a pie de cama, los patrones hemodinámicos específicos derivados de la CAP pueden aclarar el mecanismo fisiológico dominante. Por ejemplo, una mPAP ascendente acompañada de una PCP normal y una SvO₂ descendente suele indicar un aumento de la poscarga del VD, que se observa con mayor frecuencia en la espnea obstructiva del sueño (ARDSp) o cuando una PTP excesiva causa sobredistensión alveolar. Por el contrario, la elevación simultánea de la PRA y la PCP junto con un gasto cardíaco reducido es más consistente con la depresión miocárdica biventricular o con niveles excesivos de PEEP que alteran el retorno venoso. Por el contrario, cuando tanto la ARP como la PCWP son bajas, mientras que el gasto cardíaco es alto y la RVS está disminuida, el cuadro hemodinámico está dominado por la vasoplejía, característica de la fisiología del shock distributivo. Estos marcos interpretativos permiten a los médicos ajustar la configuración del ventilador y de los vasoactivos según la fisiopatología subyacente, en lugar de objetivos numéricos fijos.
En este contexto, los datos derivados del CAP orientan la intervención dirigida, ya sea para reducir la ΔP y la PEEP para aliviar la poscarga del VD, iniciar inotrópicos como la dobutamina o la milrinona para aumentar la contractilidad, añadir vasodilatadores pulmonares selectivos para mejorar el acoplamiento o ajustar la dosis de vasopresores para restablecer la presión de perfusión coronaria. Las tendencias continuas del gasto cardíaco derivadas de la SvO2 y la termodilución suelen indicar un desacoplamiento VD-AP en evolución antes de que se evidencien los cambios ecocardiográficos, lo que ofrece una valiosa alerta temprana de un colapso hemodinámico inminente.
La integración práctica de los datos del CAP en el manejo a pie de cama se resume en la Tabla 2.
| Parámetro | Significado fisiológico | Patrón / Umbral | Fisiopatología probable | Intervención guiada |
|---|---|---|---|---|
| PRA (PVC) | Retorno venoso (precarga del VD) | ↑ PRA + ↓ GC | Fallo del ventrículo derecho o PEEP excesiva | Reducir ΔP/PEEP; considerar vasodilatador |
| mPAP | Poscarga del VD | ↑ mPAP + PCWP normal | Sobredistensión alveolar, RVP elevada | Disminuir PTP; posición prona; vasodilatador pulmonar |
| PCWP | Presión de llenado del VI | ↑ PCWP + ↑ PRA | Depresión biventricular, exceso de líquidos | Restringir fluidos; añadir inotrópico |
| GC / IC | Flujo global | ↓ IC < 2.2 L min-1 m-2 | Disfunción del VD o del VI | Optimizar precarga; considerar inotrópico |
| RVP | Poscarga sostenida | >240 dyn·s·cm-5 (≈3 unidades Wood) | Compresión vascular, hipoxia, microtrombosis | Optimizar oxigenación; terapia vasodilatadora |
| Cpa | Poscarga pulsátil | ↓ <2 mL mmHg-1 | Vasculatura pulmonar rígida | Reducir ΔP; posición prona; inodilatador |
| SvO2 | Balance global de oxígeno | ↓ <60% | Desequilibrio DO2/VO2; desacoplamiento precoz del VD | Optimizar GC, Hb, FiO2 |
| DPG | Obstrucción microvascular | >7 mmHg | Vasculopatía pulmonar | Considerar vasodilatadores selectivos |
Abreviaturas: PRA: presión auricular derecha; PVC: presión venosa central; VD: ventrículo derecho; VI: ventrículo izquierdo; GC: gasto cardíaco; IC: índice cardíaco; PEEP: presión positiva al final de la espiración; ΔP: presión de conducción; mPAP: presión arterial pulmonar media; PCWP: presión de enclavamiento capilar pulmonar; RVP: resistencia vascular pulmonar; PTP: presión transpulmonar; Cpa: compliance de la arteria pulmonar; SvO2: saturación venosa mixta de oxígeno; DO2: entrega de oxígeno; VO2: consumo de oxígeno; Hb: hemoglobina; FiO2: fracción inspirada de oxígeno; DPG: gradiente diastólico pulmonar.
Ecocardiografía de cuidados críticos
La ecocardiografía es vital para el tratamiento moderno de estos pacientes. Proporciona una evaluación directa y no invasiva del tamaño y la función del ventrículo derecho (VD/VI), la excursión sistólica del plano del anillo tricúspide (TAPSE), la velocidad de la onda S del VD, el cambio de área fraccional (FAC), la evidencia de sobrecarga de presión (aplanamiento septal, ventrículo izquierdo en forma de D) y puede utilizarse para estimar la presión arterial pulmonar (PAP). Su función más importante es guiar las intervenciones dinámicas. Por ejemplo, una prueba de provocación con líquidos debería realizarse idealmente bajo guía ecocardiográfica directa, evaluando una respuesta positiva (p. ej., un aumento >15 % en la integral de velocidad-tiempo del tracto de salida del ventrículo izquierdo (IVTVI) y, al mismo tiempo, asegurando que no haya efectos perjudiciales en el ventrículo derecho (es decir, que no empeore la dilatación del VD). Esto ayuda a distinguir a los pacientes que responden a los líquidos de aquellos que simplemente los toleran.
Manometría esofágica
Esta es la única herramienta clínica que permite la partición de la mecánica del sistema respiratorio a pie de cama, proporcionando un sustituto de la Ppl. Sigue siendo indispensable para calcular la PTP real y la presión transmural auricular derecha (PRATM = PRA − Ppl), que es la presión de llenado efectiva del ventrículo derecho. Esto permite una titulación más precisa de la PEEP para prevenir tanto el colapso alveolar (manteniendo una PTP al final de la espiración ligeramente positiva) como la sobredistensión (limitando la PTP al final de la inspiración < 25 cmH₂O). Además, en pacientes que no están profundamente sedados, la presión esofágica (Peso) puede cuantificar el esfuerzo respiratorio del paciente, lo cual es crucial para diagnosticar y tratar la lesión pulmonar autoinfligida del paciente. Aunque se considera el estándar de referencia para separar la mecánica pulmonar y de la pared torácica, la manometría esofágica requiere experiencia específica y no está fácilmente disponible en todas las UCI. Su aplicación exitosa exige capacitación, equipo e interpretación adecuados dentro de un marco de monitoreo guiado por la fisiología.
Tecnologías de monitoreo emergentes
Cabe mencionar otras tres herramientas por su potencial para refinar la gestión del ventilador. El índice de estrés, derivado de la forma de la onda de presión-tiempo durante la ventilación con flujo constante, puede ser un signo específico de sobredistensión (índice de estrés > 1) frente al reclutamiento tidal (índice de estrés < 1) a la cabecera del paciente. La tomografía de impedancia eléctrica es una herramienta de monitorización no invasiva y sin radiación que proporciona imágenes en tiempo real, respiración a respiración, de la distribución regional de la ventilación. Esto permite ajustar la PEEP para lograr una insuflación pulmonar lo más homogénea posible, minimizando simultáneamente la atelectasia y la sobredistensión.
La elastancia arterial dinámica (Eadyn) se ha convertido en otro indicador funcional para evaluar la respuesta vasopresora. Calculada como la relación entre la variación de la presión de pulso y la variación del volumen sistólico [Eadyn = VVS/VPP], Eadyn proporciona un índice en tiempo real de la carga arterial. En esencia, cuantifica la relación dinámica entre el corazón y el sistema arterial, prediciendo cómo responderá la presión arterial media (PAM) a los cambios en el gasto cardíaco. Esto es particularmente valioso en el shock distributivo, donde la hipotensión puede ser causada tanto por hipovolemia como por vasodilatación. Un Eadyn bajo (p. ej., <0,8) sugiere una alta compliancia arterial (vasodilatación). En este escenario, incluso si el paciente responde a los líquidos (VPP/VVS alto), es poco probable que aumentar el volumen sistólico con líquidos eleve significativamente la presión arterial. Esto indica una necesidad primaria de vasopresores para restaurar el tono arterial. Un Eadyn alto (p. ej., >1,0) implica que el tono arterial está preservado. Por lo tanto, un aumento del volumen sistólico después de una prueba de líquidos probablemente se traducirá en un aumento significativo de la PAM. Sin embargo, el Eadyn solo es fiable en pacientes que están completamente sedados, ventilados pasivamente con un volumen corriente estable y en un ritmo sinusal regular.
Principios de gestión basados en el fenotipo
Fenotipos hemodinámicos en el shock distributivo con SDRA
Cuatro patrones recurrentes en la cabecera del paciente enmarcan el manejo hemodinámico del shock distributivo con SDRA:
(1) Vasoplejía predominante con función biventricular preservada: La presión arterial media es baja, con un gasto cardíaco elevado y una extracción de oxígeno deficiente. El mecanismo principal es la vasodilatación sistémica con un acoplamiento ventrículo-arterial preservado. El tratamiento se centra en la noradrenalina como primera línea y la vasopresina en estados de resistencia a las catecolaminas para restablecer el volumen estresado sin aumentar la RVP. La ventilación debe evitar una PTP excesiva para prevenir la carga secundaria del VD.
(2) Disfunción de predominio ventricular derecho con espandemia de reflujo agudo (ARDSp): La PTP y la RVP elevadas provocan dilatación del VD, desplazamiento septal e hipotensión sistémica. La fisiopatología principal es la insuficiencia del VD con predominio de poscarga causada por sobredistensión alveolar y compresión vascular. El tratamiento se centra en la descarga del VD mediante la reducción de la ΔP, la titulación cuidadosa de la PEEP y la colocación temprana en decúbito prono, lo que redistribuye el estrés transpulmonar, recluta las regiones dorsales y disminuye la Ea, mejorando así el acoplamiento VD-AP. Se pueden añadir vasodilatadores pulmonares inhalados (óxido nítrico o epoprostenol) e inodilatadores (dobutamina o milrinona) si persisten estados de bajo flujo a pesar de la poscarga optimizada. Se prefiere la vasopresina a los α-agonistas para optimizar la PAM y mantener la perfusión pulmonar/coronaria sin aumentar la PAP.
(3) Depresión miocárdica biventricular (superposición distributiva-cardiogénica): Este fenotipo mixto presenta disfunción sistólica global, a menudo inducida por sepsis, con disminución de la Ees del ventrículo derecho y deterioro de la eyección del ventrículo izquierdo. El tratamiento equilibra vasopresores e inotrópicos, a la vez que minimiza la poscarga del ventrículo derecho. Se debe evitar la hipercapnia y la acidosis, que aumentan la RVP y empeoran el acoplamiento. La posición prona y la vasodilatación pulmonar selectiva pueden aumentar simultáneamente la oxigenación y reducir la tensión de la pared del ventrículo derecho.
(4) Fenotipos mixtos o evolutivos: Muchos pacientes experimentan una transición entre estados con precarga y poscarga dominante debido a cambios en la mecánica pulmonar, la presión abdominal o el patrón infeccioso. La posición prona puede descargar el ventrículo derecho y, si la distensibilidad abdominal es limitada, reducir transitoriamente el retorno venoso; por lo tanto, se requiere la monitorización continua de los marcadores de precarga y el tamaño del ventrículo derecho. El manejo requiere un ajuste dinámico en lugar de protocolos fijos, alternando entre estrategias que optimizan el retorno venoso (disminuir la PEEP, aliviar la presión intraabdominal) y aquellas que reducen la poscarga del ventrículo derecho (limitar la ΔP, usar vasodilatadores en decúbito prono o inhalados) según la fisiología predominante.
Cabe destacar que la posición prona no solo sirve como complemento para la oxigenación, sino también como una intervención hemodinámica dirigida que mejora el acoplamiento VD-AP, mitiga la interdependencia ventricular adversa y promueve una distribución más homogénea de la PTP. La Tabla 3 resume las estrategias vasoactivas correspondientes adaptadas a cada fenotipo hemodinámico.
| Fenotipo | Problema principal | Tratamiento de primera línea | Terapias adjuntas | Precauciones |
|---|---|---|---|---|
| Predominio de vasoplejía | RVS baja, gasto cardíaco adecuado | Norepinefrina | Vasopresina | Evitar aumento excesivo de ΔP que incremente la RVP |
| Sobrecarga del ventrículo derecho (SDRA pulmonar) | PTP / RVP elevadas → fallo del VD | Reducir ΔP; optimizar PEEP; posición prona | Inotrópico/inodilatador (dobutamina o milrinona); vasodilatador inhalado | Evitar vasoconstrictores puros que aumenten la presión arterial pulmonar |
| Limitación por precarga (alta Ppl/IAP; SDRA extrapulmonar) | Retorno venoso impedido | Reducir PEEP; aliviar presión intraabdominal | Fluidos cautelosos; venoconstricción | Cuidado con sobrecarga de líquidos y deterioro de la oxigenación |
| SDRA mixto / alternante (SDRA pulmonar ↔ extrapulmonar) | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante | Combinación individualizada de estrategias pulmonares y extrapulmonares | Ajustar dinámicamente ventilación y fármacos vasoactivos según el fenotipo dominante | Vigilar sobrecarga del VD y limitación de precarga |
| Depresión biventricular | Baja contractilidad de ambos ventrículos | Norepinefrina + inotrópico/inodilatador | Considerar vasodilatación pulmonar | Vigilar hipotensión con inodilatadores |
Abreviaturas: RVS: resistencia vascular sistémica; ΔP: presión de conducción; RVP: resistencia vascular pulmonar; SDRA: síndrome de distrés respiratorio agudo; PTP: presión transpulmonar; VD: ventrículo derecho; PEEP: presión positiva al final de la espiración; PAP: presión arterial pulmonar; Ppl: presión pleural; IAP: presión intraabdominal.
Estrategias ventilatorias: dirigidas al fenotipo
La ventilación con presión positiva modula el retorno venoso y las condiciones de carga ventricular latido a latido. El aumento de la presión intratorácica durante la inspiración aumenta la PRA, reduciendo el gradiente de retorno venoso; simultáneamente, disminuye la poscarga del VI al disminuir la presión sistólica transmural. La presión positiva al final de la espiración añade un aumento constante de la presión intratorácica que puede ser beneficioso o perjudicial según el fenotipo. En la espnea del sueño con sobrecarga del VD, una PTP elevada magnifica la RVP y puede precipitar un cor pulmonale agudo; en la espnea del sueño con PPL elevada e infrallenado del VD, una PEEP moderada puede estabilizar la circulación reclutando el pulmón, sin aumentar significativamente la PTP, siempre que se controle la presión abdominal y la presión intratorácica total no sea excesiva. Por lo tanto, el ventilador debe ajustarse como terapia de intercambio gaseoso y como intervención hemodinámica.
El manejo del ventilador debe perseguir el doble objetivo de proteger los pulmones y el VD. La ventilación con bajo volumen corriente (4-6 mL kg−1 de peso corporal previsto) y la presión meseta limitante siguen siendo fundamentales, pero el fenotipo y el estado del ventrículo derecho determinan el «techo» seguro para ΔP. La PEEP óptima es la que maximiza el reclutamiento alveolar sin causar sobredistensión significativa o compromiso hemodinámico. En el SDRA focal (a menudo ARDSp), es poco probable que una PEEP alta reclute el pulmón consolidado y sobredistenderá preferentemente las regiones más sanas, empeorando la RVP y el shunt. En el SDRA difuso, reclutable (a menudo ARDSexp), la PEEP incremental puede abrir secuencialmente las unidades pulmonares colapsadas, disminuyendo la RVP general. Se debe realizar una «prueba de PEEP» o una maniobra de reclutamiento a desreclutamiento con monitorización hemodinámica concurrente. La titulación guiada por la presión esofágica para lograr una PTP positiva al final de la espiración (p. ej., 0-2 cmH2O) mientras se limita la PTP al final de la inspiración (<25 cmH2O) es el enfoque fisiológicamente más sólido. Cabe destacar que una presión parcial arterial de oxígeno (PaO₂) elevada no equivale a una mejor oxigenación tisular si la intervención utilizada para lograrla (p. ej., PEEP excesiva) reduce el gasto cardíaco. Las guías actuales respaldan el objetivo de una PaO₂ de 55-80 mmHg o una SpO₂ de 88-95 %. Si bien ensayos como LOCO₂ e ICU-ROX han mostrado resultados dispares sobre los beneficios de la oxigenación conservadora, sugieren que un objetivo único es insuficiente. La ventilación con protección pulmonar a menudo requiere hipercapnia permisiva. Si bien generalmente se tolera, la hipercapnia grave (p. ej., pH < 7,15-7,20) puede provocar acidosis respiratoria, que es un potente vasoconstrictor pulmonar, aumenta la Ea de la PA, empeora la función del ventrículo derecho y tiene efectos inotrópicos negativos directos sobre el miocardio.
Los principios de manejo del SDRA de fenotipo mixto requieren un ajuste dinámico en lugar de protocolos fijos. La configuración del ventilador debe individualizarse combinando los objetivos de ΔP, la monitorización de la PTP y las evaluaciones del reclutamiento regional. La titulación positiva de la presión al final de la espiración debe tener en cuenta tanto el riesgo de sobredistensión como la posible reapertura alveolar, posiblemente mediante la relación reclutamiento-inflación o la tomografía de impedancia eléctrica, si está disponible. La frecuencia de monitorización debe ser mayor que en el SDRA de fenotipo único, ya que los cambios entre el comportamiento pulmonar y el extrapulmonar pueden ocurrir en cuestión de horas (Tabla 4).
| Objetivo / Restricción | Fundamento | SDRA pulmonar (sobrecarga del VD) | SDRA extrapulmonar (limitado por precarga) | SDRA mixto / alternativo |
|---|---|---|---|---|
| VT 4–6 mL kg-1 PBW | Prevenir sobredistensión | Objetivo 4–5 mL kg-1 si hay estrés del VD | 5–6 mL kg-1 guiado por PTP | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Pplat ≤ 30 cmH2O | Protección pulmonar | Mantener más baja si PTP elevada | Interpretar con presión esofágica (Peso); puede tolerarse mayor Pplat si PTP es baja | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Minimización de ΔP | Marcador sustituto de strain pulmonar | Reducir mediante ajuste VT/PEEP | Reducir con PEEP guiada por reclutabilidad | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Estrategia de PEEP | Equilibrio entre reclutamiento y carga del VD | Preferir PEEP moderada; evitar sobredistensión | Usar objetivos de PTP; tratar primero la presión intraabdominal | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Hipercapnia permisiva | Evitar aumento de RVP | Mantener pH ≥ 7.25 (usar buffer si es necesario) | Similar, pero evitar hipercapnia severa si aumenta la PAP | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Posición prona | Mejora de oxigenación y descarga del VD | Precoz y prolongada | Considerar especialmente si hay atelectasias dorsales prominentes | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Vasodilatadores inhalados | Rescate del VD / reducción de RVP | Considerar NO o epoprostenol como terapia puente | Considerar en desajuste V/Q transitorio durante reposicionamiento | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
| Indicadores para destete | Evitar desreclutamiento | Disminuir PEEP tras recuperación del VD | Reevaluar presión esofágica / presión intraabdominal; asegurar retorno venoso estable | Características de ambos fenotipos; mecánica variable según el patrón de lesión predominante |
Abreviaturas: SDRA: síndrome de distrés respiratorio agudo; VD: ventrículo derecho; VT: volumen tidal; PBW: peso corporal predicho; PTP: presión transpulmonar; Pplat: presión plateau; Peso: presión esofágica; ΔP: presión de conducción; PEEP: presión positiva al final de la espiración; IAP: presión intraabdominal; RVP: resistencia vascular pulmonar; PAP: presión arterial pulmonar; NO: óxido nítrico inhalado.
Líquidos, vasopresores y el lado venoso de la circulación
En estados distributivos, la capacitancia venosa se expande y la PMSF disminuye. Una carga moderada de líquidos puede ser necesaria al inicio, pero en presencia de SDRA, el margen para el exceso de líquidos es estrecho porque el edema intersticial empeora la oxigenación y aumenta la RVP. Además, un balance hídrico acumulativo positivo después de 24-48 h se asocia fuertemente con peores resultados. Por lo tanto, la estrategia de fluidos debe ser conservadora una vez restablecida la perfusión, utilizando evaluaciones dinámicas (elevación pasiva de piernas con ecografía, ultrasonido de exceso venoso, índices basados en el flujo) en lugar de presiones estáticas. El manejo puede conceptualizarse utilizando un enfoque estructurado como el modelo «Reanimación, Optimización, Estabilización, Evacuación» (ROSE).
Las medidas dinámicas estándar como la VPP y la VVS a menudo son poco fiables en el SDRA debido a los bajos volúmenes corrientes, el bajo CL y, críticamente, la insuficiencia del ventrículo derecho. Una «prueba de volumen corriente» puede mejorar transitoriamente su fiabilidad, pero la maniobra de elevación pasiva de piernas combinada con la monitorización del gasto cardíaco en tiempo real sigue siendo el predictor más sólido de la respuesta a los líquidos. La PVC, aunque muy criticada como medida de volumen, sigue siendo un parámetro clínicamente importante, ya que proporciona una indicación continua del equilibrio entre la precarga y la capacidad del corazón para manejarla; un aumento rápido de la PVC con una aportación de líquidos para una ganancia mínima del gasto cardíaco indica que el corazón se encuentra en la parte plana de su curva de Frank-Starling.
La elección y titulación de los agentes vasoactivos e inotrópicos debe considerar sus efectos tanto en la circulación sistémica como en la pulmonar. Al aumentar la presión sistémica, los vasopresores pueden mejorar la perfusión coronaria al ventrículo derecho estresado y pueden mejorar la correspondencia ventilación/perfusión (V/Q). La noradrenalina es el vasopresor de primera elección. Sus potentes efectos α1-adrenérgicos aumentan la RVS y la PAM, mientras que sus modestos efectos β1 favorecen la contractilidad cardíaca. Sin embargo, la noradrenalina puede aumentar la RVP y la poscarga del ventrículo derecho. La vasopresina, añadida a la noradrenalina en el shock refractario, actúa sobre los receptores V1 para causar vasoconstricción sistémica, a la vez que preserva o incluso dilata la circulación pulmonar, lo que la convierte en una opción fisiológicamente atractiva en pacientes con insuficiencia ventricular derecha. La fenilefrina, un agonista α1 puro, generalmente debe evitarse, ya que puede aumentar significativamente tanto la RVP como la RVS, empeorando la poscarga ventricular derecha sin mejorar el gasto cardíaco.
La dobutamina es el inótropo de elección para la disfunción miocárdica séptica. Actúa principalmente sobre los receptores β1 para aumentar la contractilidad miocárdica (EE) y el volumen sistólico. Sin embargo, al aumentar el gasto cardíaco, puede empeorar el desajuste V/Q al anular la vasoconstricción pulmonar hipóxica y aumentar la fracción de shunt, lo que podría afectar la oxigenación arterial. La milrinona, un inhibidor de la fosfodiesterasa-3, ofrece la ventaja teórica de ser un “inodilatador” (que proporciona tanto inotropía como vasodilatación pulmonar), pero su larga vida media y su potencial para producir hipotensión sistémica profunda hacen que sea difícil titular la dosis en caso de shock séptico.
Terapias complementarias y de rescate
Cuando el tratamiento convencional falla, se requieren terapias de rescate dirigidas a las alteraciones fisiológicas centrales. La pronación, indicada para el SDRA de moderado a grave [PaO₂/fracción de oxígeno inspirado (FiO₂) < 150], mejora drásticamente la supervivencia. Se asocia con múltiples efectos fisiológicos favorables: recluta las regiones pulmonares dorsales; hace que la presión arterial pulmonar (PAP) sea más homogénea; mejora la correspondencia V/Q; y, fundamentalmente, descarga el ventrículo derecho al reducir la PA Ea y modificar la orientación gravitacional del corazón dentro del mediastino para aliviar la restricción pericárdica.
La oxigenación por membrana extracorpórea (ECMO) veno-venosa (VV) puede ser una terapia vital para la hipoxemia refractaria. Un beneficio clave es su capacidad para facilitar la ventilación «ultraprotectora» o de «reposo» (p. ej., ΔP cercana a cero). Esto proporciona el máximo descanso al pulmón lesionado, reduce el biotrauma y descarga profundamente el ventrículo derecho al minimizar las presiones en las vías respiratorias, lo que la convierte posiblemente en la terapia más potente para el cor pulmonale agudo provocado por ventilación lesiva. La ECMO venoarterial (VA) es una terapia fundamentalmente diferente, reservada para el colapso circulatorio refractario debido a una insuficiencia irreversible del ventrículo derecho o biventricular. La extracción extracorpórea de dióxido de carbono (CO₂) (ECCO₂R) utiliza flujos sanguíneos más bajos que la ECMO y es una opción para pacientes con acidosis hipercápnica intratable que limita la aplicación de una estrategia de protección pulmonar. Al controlar el CO₂, la ECCO₂R permite reducciones adicionales del volumen corriente y la ΔP, protegiendo así el pulmón y el ventrículo derecho.
Consideraciones especiales
Obesidad e hipertensión intraabdominal
En la obesidad, la elastancia de la pared torácica aumenta y la presión de la vía aérea se transmite con mayor facilidad al espacio pleural; la estimación de la PTP se vuelve especialmente valiosa para lograr el reclutamiento alveolar sin perjudicar el retorno venoso. En la SDRA con hipertensión intraabdominal, el retorno venoso se ve obstaculizado por el aumento de las presiones venosas abdominales y el desplazamiento cefálico diafragmático, que aumenta la Ppl. La manometría esofágica revela una distensión insuficiente a pesar de las presiones meseta aparentemente altas. El manejo incluye evitar la PEEP excesiva, optimizar el dominio abdominal (drenaje nasogástrico, bloqueo neuromuscular para el tono de la pared abdominal, drenaje percutáneo o laparotomía descompresiva cuando esté indicado) y priorizar las estrategias que restablezcan el retorno venoso (posicionamiento, administración prudente de líquidos o venoconstrictores) a la vez que se previene la sobredistensión.
Sedación, analgesia y sincronía ventilatoria
El manejo preciso de la sedación y la analgesia constituye una piedra angular, no una consideración secundaria, de las estrategias de protección pulmonar y ventricular derecha. La disincronía paciente-ventilador, en particular cuando se presentan esfuerzos inspiratorios espontáneos vigorosos, puede socavar fundamentalmente los beneficios de la ventilación protectora. Estos esfuerzos, impulsados por el paciente, pueden generar PPL negativos pronunciados y PTP ocultos, lo que desencadena una lesión pulmonar autoinfligida por el paciente (P-SILI). La fisiopatología de la P-SILI está mediada por pendelluft (es decir, el gas intrapulmonar se desplaza de regiones pulmonares no dependientes a dependientes durante la inspiración), la sobredistensión regional y el reclutamiento-desreclutamiento alveolar repetitivo, todo lo cual exacerba el estrés mecánico, amplifica las cascadas inflamatorias y empeora el edema pulmonar.
Por lo tanto, lograr la sincronía paciente-ventilador es fundamental. Las técnicas avanzadas de monitorización, en particular la manometría esofágica, son invaluables para detectar esfuerzos respiratorios lesivos, ya que permiten estimar el PTP y el trabajo respiratorio. La práctica médica actual favorece las estrategias que priorizan la analgesia, que priorizan el control óptimo del dolor para atenuar los estímulos nocivos y mitigar el impulso respiratorio, junto con una sedación adecuada y ajustada a la profundidad mínima necesaria para la comodidad del paciente y la sincronización del ventilador.
En casos de SDRA temprano y grave, donde la disincronía persiste a pesar de la analgesia y la sedación optimizadas, puede estar indicado un ciclo breve de bloqueo neuromuscular intermitente o continuo para preservar una ventilación protectora auténtica de los pulmones y el ventrículo derecho. Al suprimir el esfuerzo respiratorio espontáneo, el bloqueo neuromuscular asegura la administración precisa del volumen corriente bajo prescrito y la ΔP, minimizando así la MP y facilitando intervenciones complementarias como el decúbito prono y la hipercapnia permisiva controlada. Cabe destacar que esta sedación profunda es inherentemente temporal. La profundidad de la sedación debe reevaluarse diariamente, con el objetivo de pasar a una sedación más ligera según lo permitan la estabilidad hemodinámica y el intercambio gaseoso. Este enfoque facilita la participación en las pruebas de despertar y respiración espontánea (PRE), esenciales para evaluar la preparación para el destete y promover la movilización temprana.
Destete y recuperación
A medida que se resuelven los factores subyacentes del shock distributivo y el SDRA, y se estabilizan la oxigenación y la hemodinámica del paciente, los objetivos terapéuticos se orientan hacia la liberación de la ventilación mecánica. Esta fase presenta sus propios desafíos fisiológicos, ya que la transición de la ventilación con presión positiva a la ventilación con presión negativa puede revelar una disfunción cardíaca subyacente y precipitar el desreclutamiento o la descompensación del VD. Por lo tanto, el proceso debe ser sistemático y centrado en el paciente. Las evaluaciones diarias de la preparación para el destete son cruciales y deben incluir evidencia objetiva de mejoría clínica, como la mejora de la hemodinámica con mínimo o ningún soporte vasopresor, la disminución de los requerimientos de FiO2 y PEEP, la presencia de un reflejo tusígeno adecuado y una adecuada activación neurológica. Cuando un paciente cumple estos criterios, se debe realizar una prueba de respiración espontánea (PBE).
Los parámetros de la PBE deben seleccionarse cuidadosamente para aproximarse a la carga fisiológica que el paciente experimentará después de la extubación, que generalmente implica niveles bajos (o muy bajos) de presión de soporte con PEEP mínima. El fracaso de una PBE puede manifestarse como dificultad respiratoria, pero una proporción significativa de los fracasos son de origen cardiovascular. El cambio a respiración con presión negativa aumenta el retorno venoso y la poscarga ventricular izquierda, lo que puede precipitar un edema pulmonar inducido por el destete en pacientes con disfunción diastólica o sistólica subyacente.
En pacientes con antecedentes de sobrecarga significativa del VD durante la fase aguda de su enfermedad, el proceso de destete requiere especial precaución. Puede ser necesario un enfoque gradual, con una reducción progresiva del soporte ventilatorio en lugar de una liberación espontánea brusca. La monitorización hemodinámica estrecha, que puede incluir una ecocardiografía focalizada durante la prueba de destete, puede ayudar a identificar signos tempranos de descompensación del VD, lo que permite a los médicos adaptar la estrategia de destete para prevenir la insuficiencia recurrente y promover una liberación exitosa.
Mejora de la calidad y direcciones futuras
Las mejoras en los resultados de síndromes complejos, como el shock séptico con SDRA, dependen de la coordinación del equipo, modelos mentales compartidos y retroalimentación oportuna. Implementar rondas estructuradas que aborden explícitamente la protección pulmonar y del ventrículo derecho (VD), por ejemplo, preguntando «¿Cuál es la ΔP hoy? ¿Cuál es la PTP estimada por Peso? ¿Qué nos dicen el eco y el intercambio de gases sobre el acoplamiento VD-AP?», ayuda a afianzar la toma de decisiones en objetivos fisiológicos compartidos. El entrenamiento basado en simulación en logística de pronación, rescate hemodinámico y canulación de ECMO reduce los errores de procedimiento y genera confianza en todas las disciplinas. Los paneles de control en tiempo real que integran datos del respirador, métricas ecográficas y dosis vasoactivas pueden detectar el deterioro de forma temprana y proporcionar un punto de referencia común para equipos multidisciplinarios. Integrar estas herramientas en el flujo de trabajo diario fomenta la anticipación en lugar de la reacción, lo que permite a los médicos intervenir antes de que se produzca una insuficiencia cardiovascular irreversible o una ventilación perjudicial (Tabla 5). Los paneles de control también sirven como un puente educativo, reforzando la toma de decisiones basada en la fisiología para los médicos en formación y al mismo tiempo garantizando la alineación entre los servicios de cuidados críticos, cardiología y perfusión (Tabla 6 y Tabla 7).
| Pregunta clínica | Mejor herramienta | Herramienta secundaria | Limitaciones / errores frecuentes | Consideraciones en SDRA mixto / alternante |
|---|---|---|---|---|
| ¿La PTP es excesiva? | Presión esofágica | Tendencias de ΔP | Artefactos de Peso; esfuerzo del paciente | Puede variar por región pulmonar; combinar con imagen y pruebas de reclutamiento |
| ¿El retorno venoso está limitado por Ppl? | Ecocardiografía (tamaño VCI/VD); presión esofágica | Ecografía de congestión venosa | La PVC puede ser engañosa cuando la Ppl es alta | El fenotipo mixto puede presentar limitación variable de precarga |
| ¿Existe desacoplamiento VD-AP? | Ecocardiografía (tamaño del VD / TAPSE / PASP) | Catéter de arteria pulmonar (RVP, SvO2) | Ignorar la interdependencia VI-VD | Puede cambiar durante la evolución clínica; reevaluar con frecuencia |
| ¿Es el paciente respondedor a fluidos? | Elevación pasiva de piernas (PLR) con VTI por ecocardiografía | PPV, SVV (ajustados por RVP) | Falsos positivos cuando la RVP es elevada | El patrón mixto puede responder de forma diferente según la fisiología dominante |
| ¿Limitación de flujo vs. limitación de DO2? | SvO2 / ScvO2 y lactato | NIRS | Poco fiable en anemia severa o fallo microcirculatorio | Monitorizar estrechamente la hemodinámica macro y microcirculatoria |
Abreviaturas: PTP: presión transpulmonar; ΔP: presión de conducción; Ppl: presión pleural; VCI: vena cava inferior; VD: ventrículo derecho; Peso: presión esofágica; PVC: presión venosa central; VD-AP: acoplamiento ventrículo derecho-arteria pulmonar; TAPSE: excursión sistólica del plano del anillo tricuspídeo; PASP: presión sistólica de la arteria pulmonar; AP: arteria pulmonar; RVP: resistencia vascular pulmonar; SvO2: saturación venosa mixta de oxígeno; VI-VD: interdependencia ventrículo izquierdo-derecho; PLR: elevación pasiva de piernas; VTI: integral velocidad-tiempo; PPV: variación de presión de pulso; SVV: variación del volumen sistólico; DO2: entrega de oxígeno; ScvO2: saturación venosa central de oxígeno; NIRS: espectroscopía de infrarrojo cercano.
A pesar de los avances, persisten varias lagunas de conocimiento. En primer lugar, carecemos de herramientas pragmáticas a pie de cama que permitan un seguimiento continuo del acoplamiento VD-AP y la PTP. En segundo lugar, aunque la distinción etiológica entre ARDSp y ARDSexp ofreció un valor pronóstico limitado en ensayos clínicos a gran escala y, por lo tanto, se excluyó de la Definición de Berlín, sigue siendo un marco conceptual valioso para comprender sus mecanismos subyacentes divergentes. Sin embargo, los ensayos clínicos rara vez estratifican por fenotipo de SDRA o estado del VD, lo que diluye las posibles señales de beneficio de las intervenciones dirigidas. En tercer lugar, la integración de la presión abdominal en la titulación del respirador y el manejo hemodinámico sigue siendo infrautilizada fuera de los centros especializados.
Los ensayos futuros deberían estratificar prospectivamente por fenotipo de SDRA, estado del VD (normal vs. no acoplado) y mecánica de la pared torácica (PPL normal vs. alta). Los criterios de valoración deben reflejar no solo la oxigenación, sino también la hemodinámica (indicadores indirectos del acoplamiento VD-AP, necesidad de soporte ventricular derecho de rescate) y los resultados centrados en el paciente. Las prioridades tecnológicas incluyen la medición mínimamente invasiva de la presión arterial pulmonar (PPL), la monitorización continua de la deformación del ventrículo derecho (VD) y algoritmos de apoyo a la toma de decisiones que ajustan la PEEP/ΔP para preservar el acoplamiento y evitar la sobredistensión. Los avances en sensores portátiles y tecnologías basadas en catéteres podrían, con el tiempo, permitir la evaluación continua, a pie de cama, de la mecánica de la pared torácica y el rendimiento del VD de forma práctica y escalable. La integración de estas señales fisiológicas en plataformas basadas en aprendizaje automático podría facilitar estrategias de ventilación adaptativa que respondan en tiempo real a los cambios en la precarga, la poscarga y la mecánica pulmonar.
Más allá de la UCI, los registros multicéntricos que armonizan los datos fisiológicos y de resultados serán fundamentales para validar los enfoques de protección del fenotipo y acelerar su aplicación práctica. En última instancia, la mejora sostenida de la calidad en este ámbito dependerá no solo de la innovación tecnológica, sino también del desarrollo de la experiencia multidisciplinaria, protocolos estandarizados y sistemas de retroalimentación robustos que refuercen el cambio a largo plazo.
Mensajes para llevar a casa para la práctica clínica
Priorizar la caracterización fenotípica precisa: La identificación precisa del fenotipo del SDRA constituye la base para un manejo ventilatorio y hemodinámico individualizado. Antes de modificar la configuración del ventilador, determine si la limitación dominante proviene del parénquima pulmonar (ARDSp) o de la pared torácica/compartimento extrapulmonar (ARDSexp). En el ARDSp, la protección del VD mediante la minimización de la ΔP es fundamental. En el ARDSexp, el compromiso hemodinámico a menudo se debe a la Ppl y la reducción del retorno venoso; por lo tanto, el manejo debe centrarse en aliviar la hipertensión intraabdominal y aplicar la PEEP con prudencia.
Utilizar la presión transpulmonar para guiar la ventilación: La presión transpulmonar, en lugar de la presión meseta, debe dirigir la ventilación con protección pulmonar para lograr un reclutamiento alveolar óptimo, evitando la sobredistensión y la sobrecarga del VD.
La presión impulsora es el determinante crítico: Entre las variables ventilatorias, la ΔP muestra la asociación más fuerte con la mortalidad y la disfunción del VD. Cuando la ΔP supera los 15 cmH₂O, el imperativo clínico es reducirla —aceptando hipoxemia o hipercapnia permisivas si es necesario— para proteger la función pulmonar y del ventrículo derecho.
Reconocer el papel central del ventrículo derecho: El ventrículo derecho es el nexo fisiológico que vincula la mecánica pulmonar, la oxigenación y la perfusión sistémica. Si se desarrolla hipotensión tras un aumento de la PEEP, se debe sospechar insuficiencia aguda del ventrículo derecho antes de considerar vasoplejía. Incluso una evaluación ecocardiográfica a pie de cama del paciente, centrada en el tamaño y la función del ventrículo derecho, puede proporcionar información diagnóstica crucial.
Utilizar la posición prona temprana para la protección del ventrículo derecho: En la espnea obstructiva del sueño (ARDSp) con evidencia de sobrecarga del ventrículo derecho, la posición prona debe instaurarse tempranamente. Además de mejorar la oxigenación, la posición prona sirve como una maniobra eficaz de descarga del ventrículo derecho, reduciendo la impedancia vascular pulmonar y mejorando la interdependencia ventricular.
Integrar la monitorización fisiológica multimodal: Si bien la manometría esofágica y la ecocardiografía siguen siendo las herramientas más robustas a pie de cama para la titulación individualizada de la ventilación y la hemodinámica, en casos complejos puede justificarse una estrategia de evaluación multimodal que incorpore indicadores dinámicos/estáticos (p. ej., tendencias de la PVC, índices de respuesta a los fluidos) y, cuando corresponda, modalidades invasivas como la PAC.
Adoptar una estrategia hemodinámica con base fisiológica: Una vez establecida la perfusión tisular adecuada, se debe adoptar una estrategia conservadora de manejo de fluidos para minimizar la congestión del ventrículo derecho y el edema pulmonar. En el contexto de vasoplejía o hipotensión persistente, especialmente cuando se evidencia sensibilidad a la poscarga del ventrículo derecho o resistencia vascular pulmonar elevada, el uso preferente de vasopresina sobre catecolaminas puede ser fisiológicamente ventajoso. Este enfoque ejemplifica un marco de fisiología de precisión, que enfatiza la modulación individualizada de la precarga, la poscarga y el tono vascular en lugar de la administración refleja de fluidos o la escalada adrenérgica.
Reevaluar continuamente el fenotipo fisiológico: La coexistencia de shock distributivo y SDRA representa un estado de excepcional complejidad fisiopatológica. Un fenotipo inicialmente extrapulmonar (ARDSexp), por ejemplo, secundario a pancreatitis, puede evolucionar a una forma mixta o de predominio pulmonar (ARDSp) tras una neumonía secundaria. Por lo tanto, la reevaluación fisiológica continua es fundamental para garantizar que las intervenciones ventilatorias y hemodinámicas se adapten adecuadamente al estado fisiopatológico dinámico del paciente.
Conclusiones
El manejo de pacientes con shock distributivo y SDRA es la quintaesencia de la fisiología aplicada a los cuidados críticos, lo que exige un cambio de paradigma: desde protocolos universales hacia un enfoque individualizado y matizado, basado en un profundo conocimiento de las interacciones cardiopulmonares. Para ello, es fundamental definir con precisión el fenotipo cardiopulmonar dinámico del paciente. Esta revisión ha articulado un marco centrado en la distinción crucial entre ARDSp y ARDSexp, demostrando cómo la localización primaria del trastorno respiratorio determina consecuencias hemodinámicas fundamentalmente diferentes en respuesta a la ventilación con presión positiva. Establecer dicho marco es esencial para avanzar en el manejo personalizado, a la vez que orienta la investigación para dilucidar los mecanismos fisiopatológicos y descubrir dianas terapéuticas en pacientes críticos.