Introducción
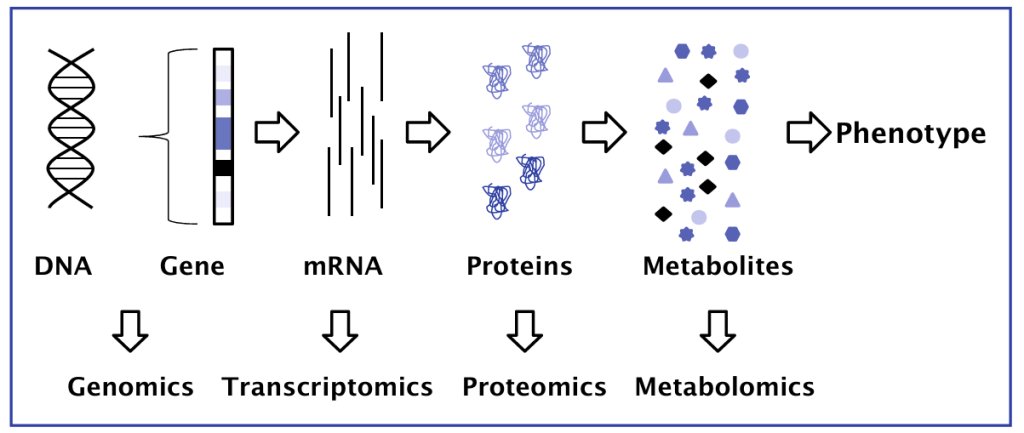
Los avances en biología molecular y celular durante las últimas dos décadas, incluyendo muy notablemente la secuenciación del genoma humano, han determinado sin duda una mejor comprensión de la fisiopatología de las enfermedades, y una identificación más precisa de las poblaciones en riesgo para ciertas condiciones. Sin embargo, muchas preguntas permanecen sin respuesta utilizando solo el enfoque genómico, incluyendo cuáles son los productos génicos y las respuestas celulares a ciertas agresiones, dada una determinada anomalía genética. El estudio del metaboloma ofrece una oportunidad única para responder algunas de estas preguntas. El metaboloma representa una combinación de todos los metabolitos y productos intermedios del metabolismo en un organismo biológico. El estudio del metaboloma, más adelante en la línea desde la estructura y función génica, refleja más estrechamente las actividades de la célula a nivel funcional y magnifica los eventos que ocurren a nivel del genoma, transcriptoma y proteoma (Fig. 1).
El desarrollo de técnicas de separación cromatográfica a principios de la década de 1970 marcó el origen del campo de identificación de metabolitos. La técnica de resonancia magnética nuclear (RMN) de 1H se utilizó por primera vez para estudios metabólicos en 1977, cuando se detectó una gama de compuestos, como lactato, creatina y alanina, en una suspensión de glóbulos rojos. Durante la década de 1980, el análisis de la plétora de metabolitos detectados en espectros de RMN de 1H impulsó el desarrollo de nuevas técnicas para clasificar muestras según su estado biológico. Así, nació el concepto de metabolómica, cuando los datos complejos de muestras biológicas se interpretaron mediante estadística multivariante. La metabolómica es el estudio científico de la respuesta metabólica de los sistemas vivos a estímulos fisiopatológicos o modificaciones genéticas. La transcriptómica, la proteómica y la metabolómica comprenden lo que se denomina biología de sistemas.
El potencial del análisis metabolómico en la enfermedad crítica se basa en su capacidad para detectar cambios en fenotipos que pueden ser útiles para el diagnóstico temprano, el pronóstico o la predicción de la respuesta a la terapia. En el presente capítulo, primero describimos los principios del análisis metabolómico, incluyendo diferentes plataformas analíticas y herramientas de interpretación de datos, y luego nos centramos en la aplicación de las ciencias metabolómicas en la medicina de cuidados críticos.
Técnicas Analíticas
Los conjuntos de datos metabolómicos se generan actualmente principalmente mediante espectroscopía de RMN (ERMN), principalmente 1H – ERMN, y espectrometría de masas (EM). Otros métodos estructurales o analíticos, como la espectroscopía infrarroja por transformada de Fourier (FTIR) o la cromatografía líquida de alta resolución (HPLC), tienen la desventaja de proporcionar un bajo nivel de identificación molecular detallada.
Espectroscopía de RMN
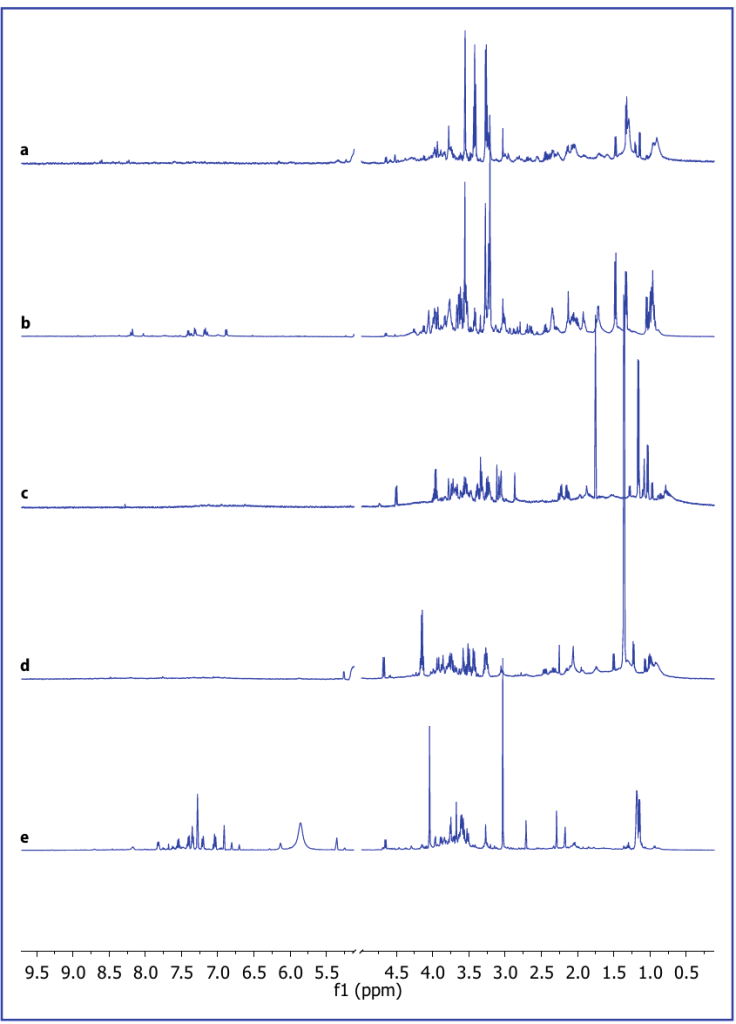
La ERMN es una técnica no destructiva que proporciona información detallada sobre la estructura molecular, así como información sobre concentraciones absolutas o relativas. La RMN es un fenómeno en el que los núcleos magnéticos en un campo magnético absorben y reemiten radiación electromagnética. La ERMN se basa en el hecho de que isótopos similares no resuenan a la misma frecuencia porque los núcleos están rodeados por una nube de electrones diamagnéticos que generan un campo magnético local. Dependiendo del entorno químico local, diferentes protones en una molécula resuenan a frecuencias ligeramente diferentes. La detección y cuantificación molecular resultante se adquiere como un conjunto de datos espectrales (Fig. 2). El eje horizontal es la frecuencia de RMN (o desplazamiento químico en partes por millón (ppm), relativo a un químico de referencia a 0 ppm (en lugar de en unidades absolutas de Hertz), y el eje vertical es la intensidad de la señal (en unidades arbitrarias). Basándose en su estructura química única, los grupos bioquímicos (CH3,CH2,OH, etc.) de cada molécula originan diferentes picos en el espectro que aparecen a una frecuencia conocida. La ERMN que utiliza rotación de ángulo mágico de alta resolución (HR-MAS) permite la adquisición de espectros de RMN de alta resolución en muestras de tejido intacto con una preparación de muestra mínima. La principal limitación de la ERMN es que esta técnica es mucho menos sensible que la EM. El desarrollo reciente de sondas criogénicas ha proporcionado una mejora en la resolución al reducir el ruido térmico en la electrónica del espectrómetro. La ERMN, mediante HR-MAS, es la única técnica disponible para estudiar tejidos intactos.
La ERMN bidimensional puede ser muy útil para dilucidar la conectividad entre señales, resultando en una identificación de metabolitos no sesgada. Los experimentos que utilizan espectroscopía de correlación (COSY) y espectroscopía de correlación total (TOCSY) proporcionan conectividad de acoplamiento espín-espín 1H – 1H, informando sobre qué señales de protones están cercanas en términos de enlace químico. Otros experimentos de RMN de correlación heteronuclear pueden ser importantes para ayudar a asignar picos de RMN. La interacción entre los núcleos 13C y 1H es muy útil para fines de identificación.
Espectrometría de Masas
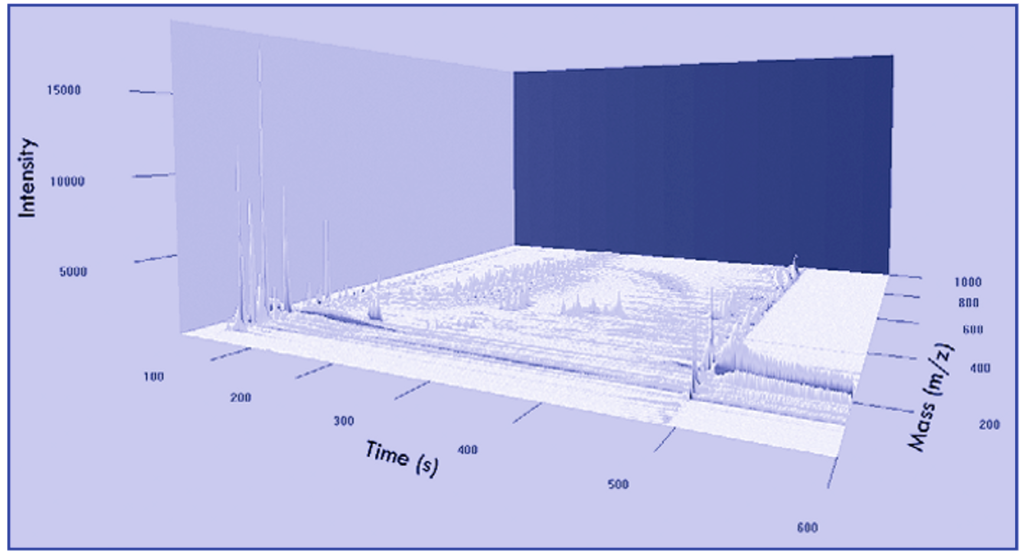
La espectrometría de masas EM es una técnica analítica destructiva que mide la relación masa-carga de partículas cargadas. Aunque los requisitos de preparación de muestras de esta técnica son generalmente más intensivos, la EM es considerablemente más sensible que la ERMN, permitiendo así el análisis metabolómico de muestras de baja concentración, como el líquido de condensado de aire exhalado. En general, esta técnica se ha acoplado a otros métodos de pre-separación como la cromatografía de gases (CG), la electroforesis capilar (EC), la movilidad iónica o la espectroscopía FTIR. El tándem más común en la metabolómica basada en EM es la cromatografía líquida (CL)-EM, que incluye HPLC y CL de ultra alta presión (UHPLC). La CL-EM proporciona datos metabólicos tridimensionales (Fig. 3), donde en cada punto de muestreo en el cromatograma (tiempo de retención) hay un espectro de masas completo (masa vs. intensidad).
Análisis de Datos Espectrales
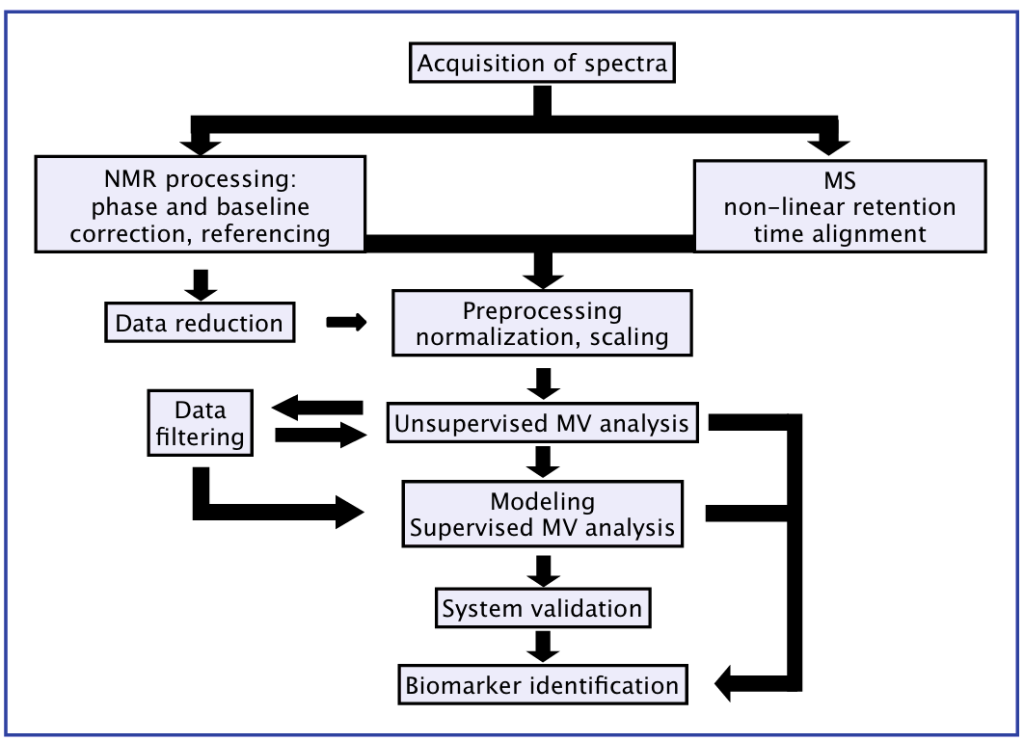
Análisis de Datos Espectrales Independientemente de la plataforma analítica utilizada, los datos espectrales pueden considerarse como un conjunto complejo multidimensional de coordenadas metabólicas. La interpretación de los datos metabólicos es complicada y requiere la aplicación de herramientas quimiométricas no supervisadas y supervisadas (Fig. 4). Antes del análisis estadístico, los datos espectrales deben ser preprocesados. El preprocesamiento de datos es un paso necesario entre la adquisición de los espectros brutos y el análisis multivariante de un conjunto de datos metabolómicos. Para los estudios metabolómicos, los métodos de preprocesamiento están diseñados para reducir las varianzas y las posibles influencias que podrían interferir con el análisis de datos (como posibles variaciones en las concentraciones de la muestra o diluciones variables de la muestra), distorsiones de fase y líneas de base irregulares en el espectro de RMN y desalineación del tiempo de retención en los datos de CL-EM.
Los métodos estadísticos multivariantes o de reconocimiento de patrones proporcionan un medio para recopilar información relevante sobre diferencias o similitudes entre las vías metabólicas. Estos métodos incluyen métodos de proyección multivariante, en los que el análisis de componentes principales (PCA) y el análisis discriminante de mínimos cuadrados parciales (PLS-DA) son las técnicas más utilizadas.
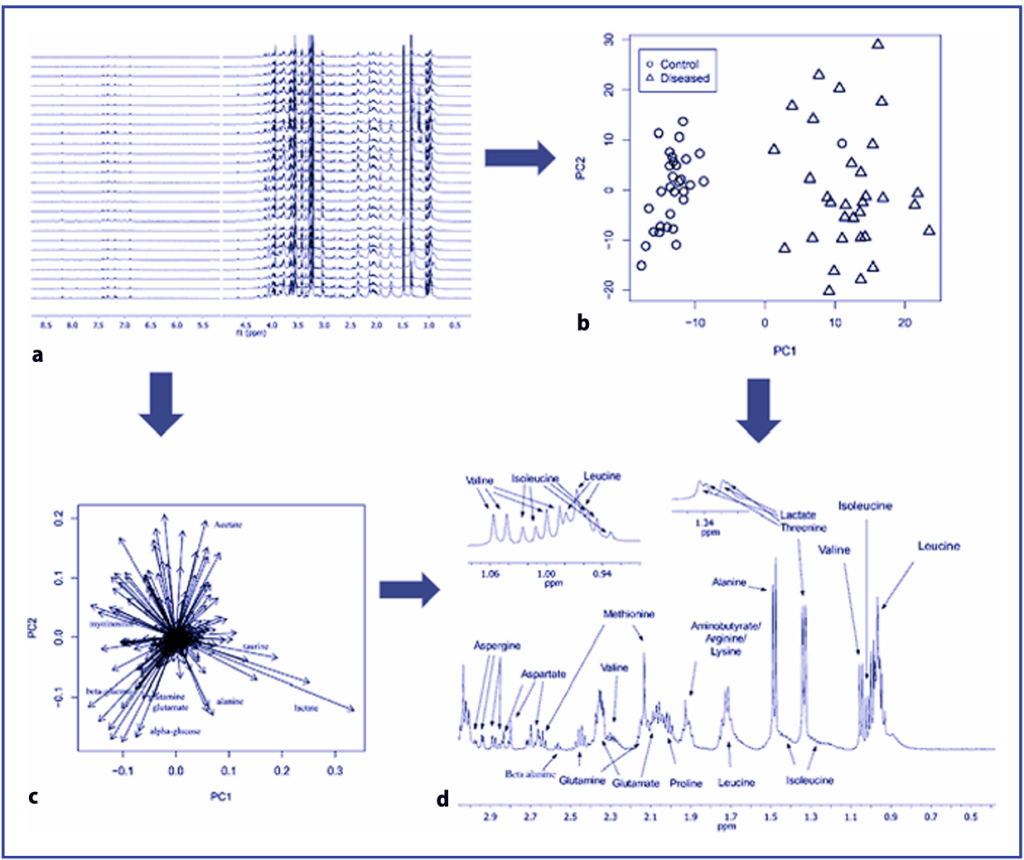
El PCA es una de las técnicas exploratorias más comunes en el análisis multivariante. Su uso más importante es representar datos multivariantes en un espacio de baja dimensionalidad (Fig. 5a). El primer componente principal está definido por el perfil espectral (carga) en los datos que describe la mayor parte de la variación. El segundo componente principal, ortogonal al primero, es el segundo mejor perfil que describe la variación, y así sucesivamente. Los componentes principales se componen de los llamados puntuaciones y cargas. Las cargas contienen información sobre las variables (desplazamientos químicos) en el conjunto de datos y las puntuaciones contienen información sobre las clases de muestras. Los gráficos de puntuaciones (Fig. 5b) se utilizan para distinguir el perfil de metabolitos de los sujetos control de los enfermos, o para evaluar la tasa de progresión de la enfermedad. Los gráficos de cargas (Fig. 5c) resaltan las variables más significativas. En otras palabras, los desplazamientos químicos (señales metabólicas) con los valores de carga más altos en la dirección correcta serían seleccionados como potenciales biomarcadores (Fig. 5d).
El PLS-DA es un método de regresión lineal supervisado mediante el cual las variables latentes construidas con las variables multivariantes correspondientes a las observaciones (descriptores espectrales) se asocian con la pertenencia a la clase de cada muestra. El objetivo del PLS-DA es encontrar en las regiones espectrales aquellos componentes que describan significativamente variaciones relevantes en los espectros y tengan la máxima covarianza con el vector de información de la clase. El PLS-DA también puede expresarse mediante matrices de puntuaciones y cargas, y la interpretación de los resultados es similar a la del PCA.
Análisis Metabolómico y Enfermedad Crítica
El análisis mediante ERMN 1H de biofluidos proporciona una herramienta para la comprensión de los procesos bioquímicos asociados con la enfermedad de cuidados críticos. La ERMN 1H, mediante HRMAS, es una excelente opción para estudiar fluidos no procesados. Se pueden citar varios estudios metabolómicos de ERMN 1H de diferentes tejidos como ejemplos para el diagnóstico en modelos animales agudos y en enfermedades humanas.
La enfermedad crítica se caracteriza por una alteración severa de la homeostasis metabólica y las vías de transducción de señales. La metabolómica puede definir fenotipos específicos de síndromes agudos que potencialmente pueden ayudar a comprender la fisiopatología, realizar un diagnóstico temprano, identificar pacientes en riesgo, determinar la gravedad y el pronóstico de la enfermedad y predecir la respuesta a la terapia. De esta manera, la metabolómica en la enfermedad crítica puede cambiar el concepto de biomarcadores. Por ejemplo, la metabolómica puede definir un biomarcador metabolómico específico asociado con la progresión al síndrome de dificultad respiratoria aguda (SDRA) en pacientes en riesgo, o con infecciones en pacientes con quemaduras graves.
Sepsis
Xu et al. construyeron un modelo pronóstico basado en el análisis de suero mediante metabolómica basada en HPLC-EM en ratas sometidas a ligadura y punción cecal (CLP). El análisis por HPLC-EM discriminó entre las ratas que sobrevivieron y las que no después de CLP y procedimiento simulado con una precisión del 94%. Se relacionaron seis metabolitos con el resultado, incluyendo ácido linoleico, ácido linolénico, ácido oleico, ácido esteárico, ácido docosahexaenoico y ácido docosapentaenoico. En un estudio posterior realizado por el mismo grupo con una técnica diferente, se analizaron muestras de suero de ratas sépticas utilizando 1H – ERMN. Seis metabolitos característicos involucrados en el metabolismo energético (lactato, alanina, acetato, acetoacetato, hidroxibutirato y formiato) cambiaron en las ratas sépticas, de manera más marcada en las no supervivientes. Un modelo predictivo pronóstico construido con estos metabolitos mostró una precisión del . En otro estudio, el análisis por CL-EM de muestras de plasma de ratas con lesiones térmicas y sépticas reveló nueve metabolitos característicos (hipoxantina, sulfato de indoxilo, ácido glucurónico, ácido glucónico, prolina, uracilo, nitrotirosina, ácido úrico y ácido trihidroxicoloánico) que discriminaban a los animales sépticos de los no sépticos. Estos biomarcadores están relacionados principalmente con el estrés oxidativo y el daño tisular.
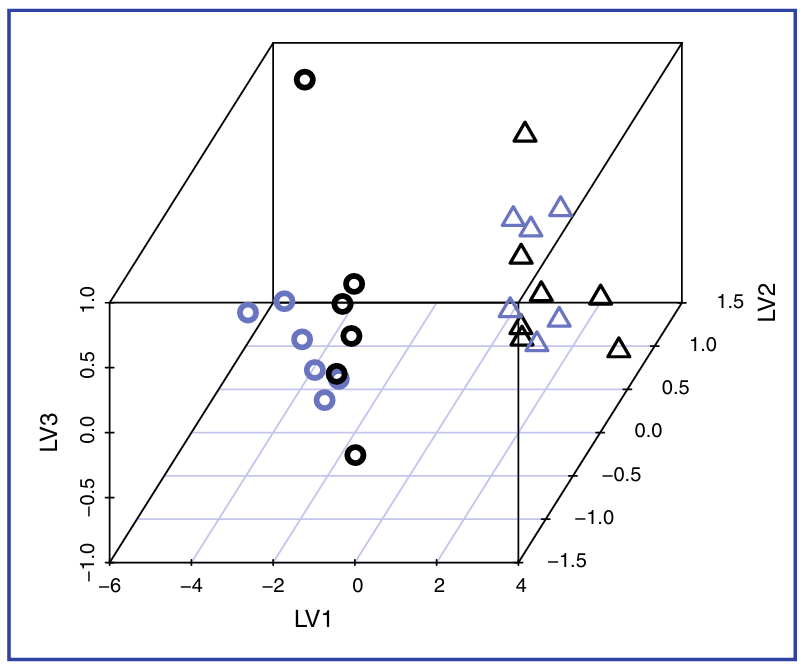
Recientemente hemos informado que la ERMN 1H de tejido pulmonar, líquido de lavado broncoalveolar (BAL) y muestras de suero mostraron concentraciones diferentes de metabolitos característicos en ratas sometidas a CLP en comparación con las ratas control: Las concentraciones de alanina, creatina, fosfoetanolamina y mioinositol aumentaron en el tejido pulmonar; la creatina aumentó y el mioinositol disminuyó en el líquido de BAL; y la alanina, creatina, fosfoetanolamina, acetoacetato y dos ácidos grasos no identificados aumentaron mientras que el formiato disminuyó en el suero. Construimos un modelo que fue 100% predictivo del diagnóstico de sepsis, utilizando todas las muestras combinadas o solo las muestras de suero (Fig. 6). Uno de los hallazgos novedosos de nuestro estudio fue el comportamiento diferente de los metabolitos en las diversas muestras analizadas.
Lesión Pulmonar Aguda (LPA) y SDRA
Actualmente, el diagnóstico de LPA y SDRA se basa en la presencia de criterios inespecíficos, como parámetros fisiológicos y radiológicos. Por lo tanto, existe la necesidad de biomarcadores para estas condiciones. Aunque se han propuesto varias proteínas séricas y perfiles genómicos como biomarcadores diagnósticos, carecen de suficiente sensibilidad y especificidad.
Serkova et al. utilizaron el análisis por ERMN 1H de muestras de tejido pulmonar de ratas que recibieron una administración intra-traqueal de interleucina (IL)-1β y factor de necrosis tumoral (TNF)-α. En este modelo de LPA inducida por inflamación, los fosfatos de alta energía (ATP, ADP, balance energético y cambio energético) y la relación lactato-glucosa fueron biomarcadores de la condición. Además, hubo una fuerte asociación temporal entre la metabolómica basada en ERMN y los índices histológicos de lesión pulmonar.
Más recientemente, Stringer et al. estudiaron muestras de suero de pacientes con LPA inducida por sepsis utilizando ERMN 1H. Encontraron diferencias significativas en la concentración de glutatión total, mioinositol, adenosina, fosfatidilserina y esfingomielina entre pacientes con LPA inducida por sepsis y sujetos sanos. Además, los niveles de mioinositol y glutatión total se asociaron con cambios en parámetros fisiológicos, como puntuaciones fisiológicas agudas y días sin ventilador.
Recientemente hemos utilizado un enfoque metabolómico basado en ERMN 1H para el diagnóstico de la lesión pulmonar inducida por ventilador (VILI) en ratas. Seis metabolitos (lactato, glucosa, acetato, creatina, glicina e hidroxibutirato) cambiaron significativamente en el tejido pulmonar y el líquido de BAL de ratas con VILI. Basándose en estos resultados, se puede plantear la hipótesis de que la ERMN podría ser útil para el diagnóstico de biotrauma en pacientes que reciben ventilación mecánica.
Lesión Renal Aguda (LRA)
Los biomarcadores tradicionales de LRA incluyen la concentración de nitrógeno ureico en sangre (BUN) y la concentración sérica de creatinina, que se sabe que carecen de sensibilidad para la disminución temprana de la función renal. Se están estudiando nuevos biomarcadores como la lipocalina asociada a gelatinasa de neutrófilos (NGAL) y la IL-18 con resultados alentadores.
Hasta ahora no hay estudios sobre el papel de la metabolómica para el diagnóstico o pronóstico de pacientes críticamente enfermos con LRA. En un modelo murino de insuficiencia renal aguda inducida por cisplatino, la ERMN 1H mostró cambios significativos en la concentración urinaria de glucosa, alanina, lactato, leucina, metionina, 2-oxoglutarato, piruvato y valina. Además, los ratones tratados con cisplatino exhibieron un aumento dependiente del tiempo en los niveles de ácidos grasos no esterificados y triglicéridos en suero, orina y tejido renal. Los autores propusieron que este perfil metabolómico relacionado con la LRA podría utilizarse como un nuevo biomarcador de lesión renal. Futuros estudios deberán dilucidar el papel de la metabolómica para la detección temprana y el pronóstico de la LRA.
Trauma
Se ha utilizado un enfoque metabolómico en dos estudios en pacientes con trauma. Una concentración plasmática más alta de lactato evaluada por ERMN 1H discriminó a los pacientes con trauma que desarrollaron síndrome de disfunción orgánica múltiple de aquellos que no lo hicieron. En otro estudio, una disminución de la concentración plasmática de tres lípidos fue un predictor importante del resultado en pacientes con trauma, mientras que las concentraciones plasmáticas de glucosa y glutamato fueron predictores intermedios.
Conclusión
Conclusión Se necesitan biomarcadores sensibles y específicos para el diagnóstico temprano y el pronóstico de enfermedades críticas, como sepsis, LPA/SDRA, LRA y trauma. Un enfoque metabólico que utilice ERMN 1H puede identificar fenotipos metabólicos específicos para ciertas condiciones o resultados, que pueden ser útiles como biomarcadores de enfermedad. Además, el análisis de las vías metabólicas específicas y de transducción de señales involucradas puede arrojar luz sobre la fisiopatología de estas condiciones.


