La fibrilación auricular (FA) asociada a factores de estrés se define como una FA de nueva aparición que se produce en el contexto de un factor de estrés fisiológico agudo y reversible (p. ej., cirugía cardíaca, infección aguda). Aunque históricamente se ha considerado transitoria y potencialmente benigna, cada vez hay más evidencia que demuestra que la FA asociada a factores de estrés tiene importancia pronóstica, con tasas a largo plazo de recurrencia de la FA y eventos adversos relacionados con la FA (p. ej., ictus, insuficiencia cardíaca) que se aproximan a las de la FA que ocurre sin un factor de estrés. Sin embargo, los aspectos clave del manejo de la FA asociada a factores de estrés (p. ej., prevención, vigilancia, tratamiento) siguen siendo muy variables. En esta revisión de vanguardia, ofrecemos una síntesis clínica de la epidemiología, los mecanismos, los resultados y el manejo de la FA asociada a factores de estrés, considerando todos los factores desencadenantes caracterizados. En este contexto, describimos un marco fisiopatológico en el que la FA asociada a factores de estrés representa un espectro que abarca las contribuciones relativas variables de los efectos directos del factor de estrés, el sustrato mediado por el factor de estrés y la predisposición subyacente (es decir, factores de riesgo de FA modificables y no modificables). Los episodios de FA asociada a factores de estrés que ocurren en el contexto de una fuerte predisposición subyacente a la FA (a veces denominada «FA provocada») tienen un mayor riesgo de recurrencia, mientras que los episodios que ocurren en respuesta a un factor de estrés fisiológico profundo con una predisposición subyacente mínima o nula (a veces denominada «FA reversible») tienen un menor riesgo de recurrencia. Tomando como ejemplo la FA asociada a factores de estrés poscirugía cardíaca, resumimos los avances recientes que traducen una mayor comprensión fisiopatológica (p. ej., el papel de la inflamación local) en nuevas intervenciones clínicas capaces de reducir la incidencia de la FA asociada a factores de estrés (p. ej., pericardiotomía posterior). Resumimos la evidencia disponible para el manejo clínico de la FA asociada a factores estresantes y ofrecemos un marco conceptual para fundamentar la atención. Finalmente, concluimos describiendo las prioridades clave para futuras investigaciones diseñadas para facilitar el manejo preciso de la FA asociada a factores estresantes, incluyendo la identificación de medidas preventivas más efectivas, el desarrollo de modelos para estratificar el riesgo de FA recurrente y eventos adversos relacionados con la FA tras un episodio de FA asociada a factores estresantes, y la integración de resultados centrados en el paciente.
¿Qué es la fibrilación auricular asociada a factores de estrés?
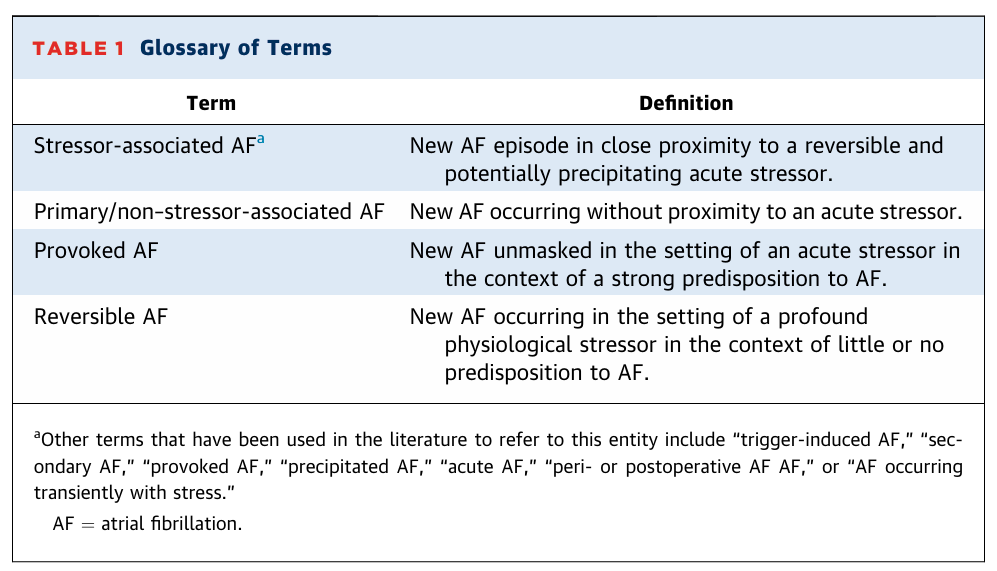
La carga global de fibrilación auricular (FA) está aumentando y afecta actualmente a casi 60 millones de personas en todo el mundo. En casi un tercio de los casos, la FA se diagnostica inicialmente en el contexto de un factor estresante fisiológico agudo, como una cirugía o una infección, y se ha denominado de forma variable como «FA desencadenada», «FA precipitada», «FA secundaria», «FA aguda», «FA provocada», «FA perioperatoria o posoperatoria» o «FA transitoria con estrés» (Tabla 1). En este estudio, adoptamos el término FA asociada a factores estresantes para describir un nuevo episodio de FA que ocurre en estrecha proximidad a un factor reversible y potencialmente desencadenante. Seleccionamos este término en lugar de otras alternativas para reconocer la incertidumbre inherente sobre si la FA detectada en el contexto de un factor estresante es realmente secundaria a este o preexistente y detectada incidentalmente debido a una hospitalización. La FA asociada a factores estresantes contrasta con la FA no asociada a factores estresantes o «FA primaria», que se refiere a una FA de nueva aparición que ocurre sin proximidad a un factor desencadenante agudo. Como analizaremos en detalle, e independientemente del término utilizado, es importante reconocer que la FA que se presenta en el contexto de un factor estresante es en sí misma una entidad heterogénea, con contribuciones causales, generalmente poco claras y potencialmente variables, del factor estresante subyacente a la aparición de la FA (Ilustración Central). Las directrices actuales reconocen un amplio espectro de posibles factores estresantes, incluyendo factores estresantes quirúrgicos, como la cirugía cardíaca y no cardíaca, así como factores estresantes no quirúrgicos (médicos), que abarcan afecciones cardíacas (p. ej., infarto de miocardio [IM], miocarditis) y no cardíacas (p. ej., infección aguda), situaciones de emergencia (p. ej., traumatismo), consumo excesivo de alcohol, consumo de drogas (p. ej., metanfetamina, cocaína) y trastornos endocrinos (p. ej., tiroideos, suprarrenales).
Aunque en su momento se consideró benigna y autolimitada, un análisis fundamental del Estudio Cardíaco de Framingham demostró que las tasas de FA recurrente y de eventos adversos relacionados con la FA, como ictus, insuficiencia cardíaca y muerte, tras la FA asociada a factores de estrés, se aproximan a las de la FA primaria. Estudios posteriores han reforzado las importantes implicaciones pronósticas de la FA asociada a factores de estrés, demostrando que las personas que desarrollan FA asociada a factores de estrés se enfrentan a un mayor riesgo de resultados adversos en comparación con las personas expuestas al mismo evento desencadenante, pero que no desarrollan FA. Esta revisión proporcionará una visión general de la epidemiología, los factores de riesgo y los principios contemporáneos de gestión preventiva y terapéutica de la FA asociada a factores de estrés, centrándose en factores de estrés quirúrgicos y médicos comunes, como infecciones agudas, sepsis, infarto de miocardio y afecciones tóxicas como el hipertiroidismo y el consumo agudo de alcohol. Si bien la revisión enfatiza estos factores estresantes mejor caracterizados, reconocemos la relevancia clínica de otros factores desencadenantes menos estudiados, como el consumo de estimulantes, los traumatismos, la embolia pulmonar y otros trastornos endocrinos, que no se analizan en detalle aquí debido a la escasez de datos, pero que ameritan mayor investigación. A lo largo de este artículo, analizaremos las lagunas de conocimiento existentes y destacaremos futuras vías para un enfoque preciso del manejo de la FA asociada a factores estresantes.
Métodos de revisión narrativa
Realizamos una revisión narrativa para sintetizar el conocimiento actual sobre la FA asociada a factores estresantes en diversos contextos clínicos. Las fuentes iniciales se identificaron a partir de las guías contemporáneas de manejo de la FA y las declaraciones de consenso emitidas por las principales sociedades cardiovasculares, como la Asociación Americana del Corazón, la Sociedad Europea de Cardiología y la Sociedad Cardiovascular Canadiense. Se identificó literatura adicional mediante: 1) revisión manual de listas de referencias; 2) búsquedas específicas en PubMed y Google Académico utilizando combinaciones de palabras clave y términos MeSH (Medical Subject Headings) (“fibrilación auricular”, “nueva aparición”, “precipitado”, “postoperatorio”, “cirugía cardíaca”, “cirugía no cardíaca”, “sepsis” e “infarto de miocardio”, “anticoagulación”); y 3) la aportación de expertos de los autores del estudio. Priorizamos estudios prospectivos, análisis de cohortes grandes y revisiones sistemáticas o metaanálisis que aportaran información clínica o mecanicista importante. Dada la heterogeneidad terminológica utilizada en la literatura existente, se prestó especial atención a la definición temporal y etiológica de la FA. El objetivo de esta revisión es depurar los temas relevantes para la práctica clínica, destacar las áreas de incertidumbre restantes y contextualizar las consideraciones de vigilancia y manejo para los profesionales clínicos que se enfrentan a la FA asociada a factores estresantes. Esta revisión no implicó una investigación original con sujetos humanos, por lo que no se obtuvo la aprobación ética ni la supervisión del Comité de Ética de la Investigación (CRI).
Incidencia de fa asociada a factores de estrés
De forma análoga a la población post-ictus, la incidencia de FA asociada a factores de estrés depende de la frecuencia, duración e intensidad de la monitorización. De acuerdo con lo esperado, la incidencia de FA asociada a factores de estrés es sustancialmente mayor con la monitorización continua rutinaria que con la monitorización intermitente clínicamente controlada, tanto en poblaciones quirúrgicas como no quirúrgicas. Por ejemplo, en un metaanálisis de estudios prospectivos que evaluaron la FA asociada a factores de estrés tras cirugía no cardíaca (27 estudios; n = 5.829.758), los estudios que utilizaron monitorización continua informaron una tasa de FA asociada a factores de estrés siete veces mayor que los que no la utilizaron (13,9 % frente a 1,9 %). De igual manera, los estudios que utilizan monitorizaciones continuas extendidas (p. ej., monitores de parche, registradores de bucle implantables) han informado incidencias notablemente mayores de FA asociada a factores de estrés (Tabla 2). En conjunto, estos hallazgos sugieren que la determinación de la FA mediante monitorización intermitente, a corto plazo o basada en criterios clínicos (p. ej., electrocardiograma [ECG] de 12 derivaciones activado por síntomas, monitores Holter) puede subestimar considerablemente la incidencia real de la FA asociada a factores de estrés, y las tasas de incidencia notificadas deben interpretarse con cautela dada esta limitación. Es plausible que, en algunos casos, la FA asociada a factores de estrés pueda representar en realidad una FA paroxística no diagnosticada previamente, detectada incidentalmente mediante la monitorización clínica intensificada típica del entorno hospitalario. Esta clasificación errónea puede inflar la incidencia observada de FA asociada a factores de estrés y sesgar las tasas de eventos hacia las notificadas habitualmente para la FA primaria. La FA posoperatoria es una complicación frecuente de la cirugía cardíaca, con una incidencia global de aproximadamente el 30 % (Tabla 2). La incidencia varía según el tipo de intervención quirúrgica: se presenta en aproximadamente el 20 % de los pacientes sometidos a cirugía de revascularización coronaria aislada (CABG), aumenta al 40 % tras el reemplazo o la reparación valvular y alcanza hasta el 50 % en casos que involucran procedimientos combinados de CABG y valvulopatías. Por el contrario, la incidencia de FA asociada a factores de estrés es menor tras la cirugía torácica no cardíaca (5 %-30 %) y es la más baja tras la cirugía no cardíaca ni torácica (0,4 %-15 %).
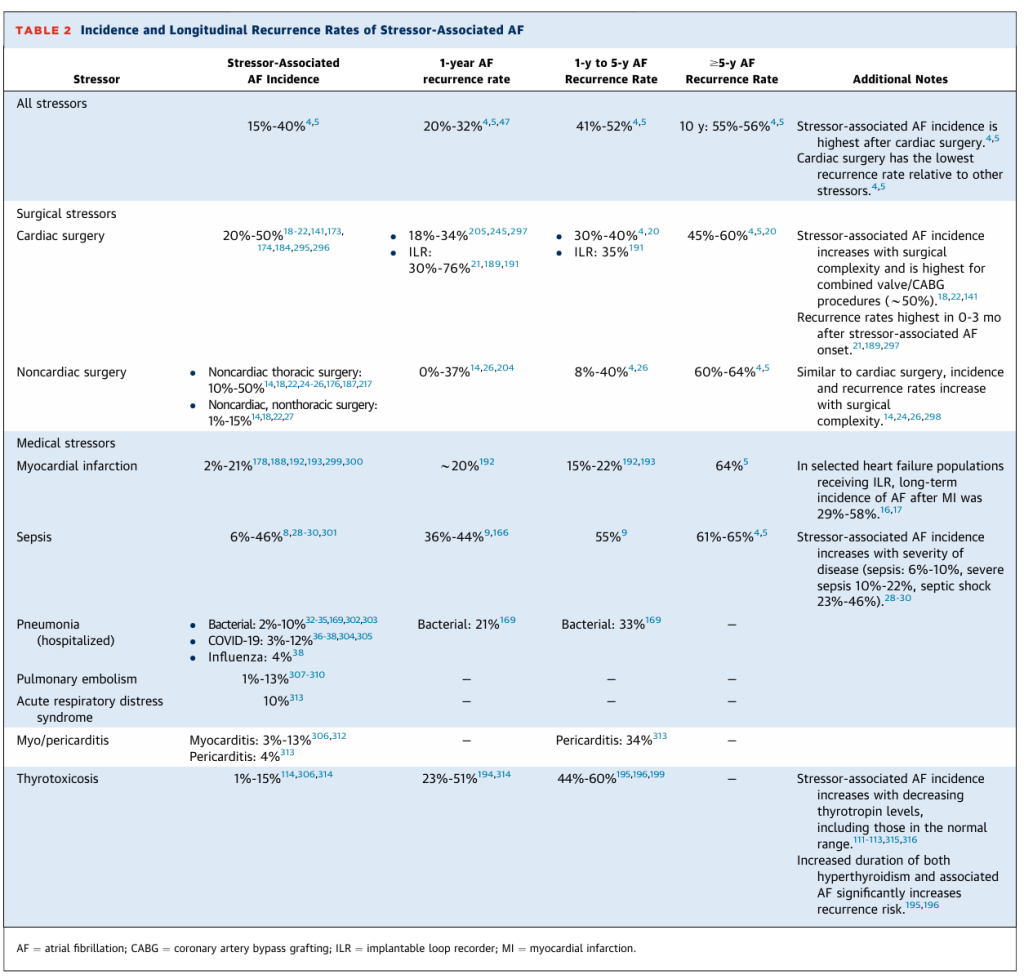
La sepsis se asocia con tasas de incidencia de FA asociada a factores de estrés de entre el 6% y el 40% (Tabla 2). Además del impacto de las diferentes prácticas de monitorización del ritmo cardíaco, las diferencias en la incidencia de FA notificada en la población con sepsis probablemente también reflejen la variación en los métodos de determinación de la sepsis (p. ej., códigos de facturación frente a definiciones clínicas) y la gravedad de la enfermedad subyacente. En uno de los estudios prospectivos más amplios de pacientes con sepsis ingresados en una unidad de cuidados intensivos (n = 1782), la incidencia de FA asociada a factores de estrés aumentó considerablemente con el empeoramiento de los parámetros hemodinámicos y la función orgánica, del 10% al 40% en sepsis frente a shock séptico, respectivamente. En comparación con la sepsis, las tasas de FA asociada a factores de estrés tras la neumonía bacteriana y vírica son menores, entre el 5% y el 10%, como se demuestra en estudios que utilizan datos radiográficos, de cultivos y pruebas de antígenos séricos y urinarios. Cabe destacar que un estudio que comparó directamente la COVID-19 con la gripe observó tasas casi idénticas entre ambos grupos.
La incidencia de FA asociada a factores de estrés tras un infarto de miocardio se estima en torno al 6%-11% (Tabla 2). Sin embargo, los resultados de los ensayos ARREST (Monitorización Continua del Ritmo en Pacientes Tras un Infarto Agudo de Miocardio y Fracción de Eyección del Ventriculo Izquierdo Preservada), CARISMA (Arritmias Cardíacas y Estratificación del Riesgo Tras un Infarto Agudo de Miocardio) y SMART-MI (Monitores Cardíacos Implantables en Pacientes de Alto Riesgo con Disfunción Cardíaca Autonómica), que utilizaron registradores de bucle implantables para la detección de FA a largo plazo en poblaciones post-IM muy seleccionadas, informaron tasas sustancialmente más altas (28%-58%).
Fisiopatología al pronóstico
Relación dinámica entre estresante y sustrato
La fisiopatología de la FA asociada a factores estresantes no se comprende completamente y probablemente varíe según el factor estresante. Sin embargo, la evidencia sugiere que es probable que un tema unificador incluya cambios fisiológicos agudos que inducen actividad ectópica (inicio) en el contexto de un sustrato auricular lo suficientemente vulnerable como para mantener los circuitos de reentrada característicos de la FA (mantenimiento). Si bien los factores de riesgo no modificables (p. ej., predisposición genética, edad) constituyen la base del riesgo de FA, otros factores de riesgo modificables (p. ej., hipertensión, obesidad) aceleran las anomalías estructurales y funcionales que predisponen a la FA, como la dilatación y la fibrosis auriculares (Figura 1). Cuando se presentan factores estresantes agudos, no solo actúan para inducir actividad ectópica, sino que también pueden contribuir a cambios proarrítmicos persistentes durante el período de exposición (es decir, actúan como un «perpetuador» de la FA). Por ejemplo, como se analiza con mayor detalle más adelante, el infarto de miocardio (IM) puede inducir tanto efectos estresantes directos, como la actividad ectópica, como contribuir al sustrato inducido por el estresor, como la dilatación auricular secundaria al aumento de la presión arterial por disfunción ventricular izquierda. Por lo tanto, en un paciente con hipertensión e IM, los factores de riesgo modificables y el sustrato mediado por el estresor contribuyen sinérgicamente a la remodelación patológica de las aurículas, lo que a su vez aumenta el riesgo futuro de FA.
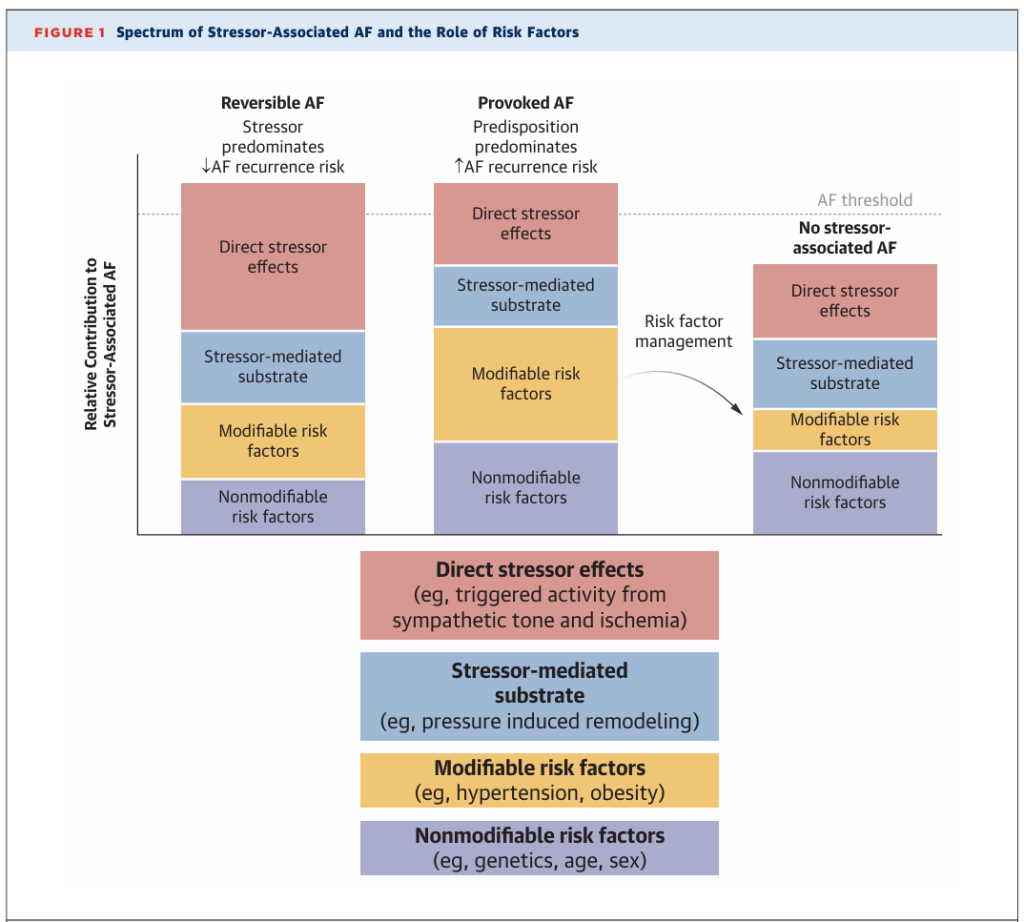
En este contexto, resulta evidente que la FA asociada a factores estresantes, incluso dentro de los límites del mismo factor estresante, probablemente representa un espectro que abarca contribuciones relativas variables de los efectos directos del factor estresante, el sustrato mediado por el factor estresante y la predisposición subyacente. Los dos extremos del espectro de la FA asociada a factores estresantes se han dicotomizado previamente en FA «provocada» y «reversible» (Tabla 1). La FA «provocada» se refiere a la FA desenmascarada en el contexto de un factor estresante agudo en el contexto de un sustrato auricular crónicamente susceptible con una fuerte predisposición a la FA. Además, en algunos casos, la FA «provocada» probablemente representa una FA primaria detectada fortuitamente gracias a la monitorización del ritmo inherente a la hospitalización. Por el contrario, la FA «reversible» se refiere a la FA que se produce en respuesta a un factor estresante fisiológico profundo que se produce en el contexto de una predisposición subyacente mínima o nula a la FA. Intuitivamente, tras la resolución del factor estresante, las personas con FA «provocada» tienen un riesgo sustancialmente mayor de recurrencia de la FA en comparación con las personas con FA «reversible».
Inflamación local y sistémica.
La activación sistémica del sistema inmunitario innato por señales inflamatorias asociadas a patógenos o estériles es un precursor establecido de la FA no asociada a factores de estrés. La activación del inflamasoma NLRP3 induce la sobreexpresión de citocinas proinflamatorias, como la proteína C reactiva (PCR) y la interleucina (IL)-6. Estas citocinas, a su vez, alteran la expresión de los canales iónicos de membrana, así como de los canales iónicos intracelulares conocidos como conexinas, lo que resulta en la promoción de la actividad auricular desencadenada, como se evidencia en modelos animales de sepsis e infarto de miocardio (IM). La asociación clínica de marcadores inflamatorios con la FA asociada a factores de estrés se ha descrito en infecciones agudas, sepsis e IM.
A diferencia de la FA asociada a factores de estrés médico, los estudios que investigan la asociación entre marcadores inflamatorios sistémicos (p. ej., recuento de leucocitos, PCR e IL-6) y la FA posoperatoria han arrojado resultados contradictorios. Si bien la concentración de leucocitos y los niveles máximos se han correlacionado con el momento de inicio de la FA, marcadores de inflamación más específicos, como los niveles pre y posoperatorios de PCR e IL-6, se han asociado de forma inconsistente con la FA posoperatoria. Cabe destacar que un metaanálisis indicó que la reducción de la inflamación con colchicina se asocia con una reducción de la FA poscirugía cardíaca. Sin embargo, las directrices actuales no recomiendan la profilaxis con colchicina debido a las reacciones adversas y la interrupción frecuente del tratamiento.
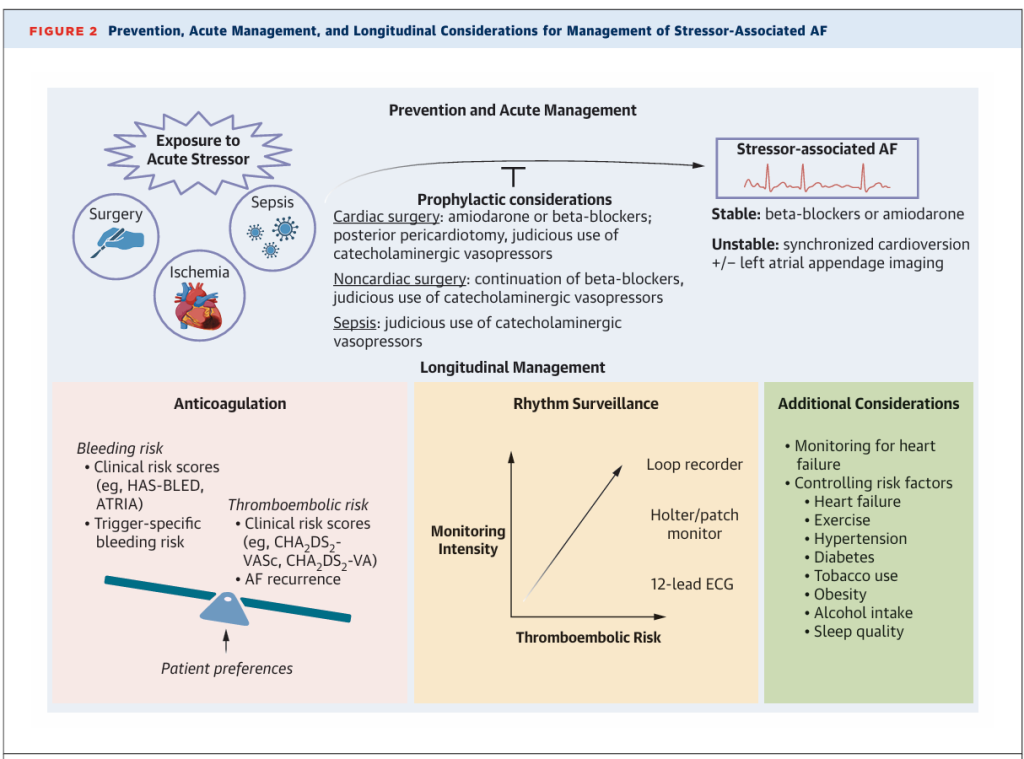
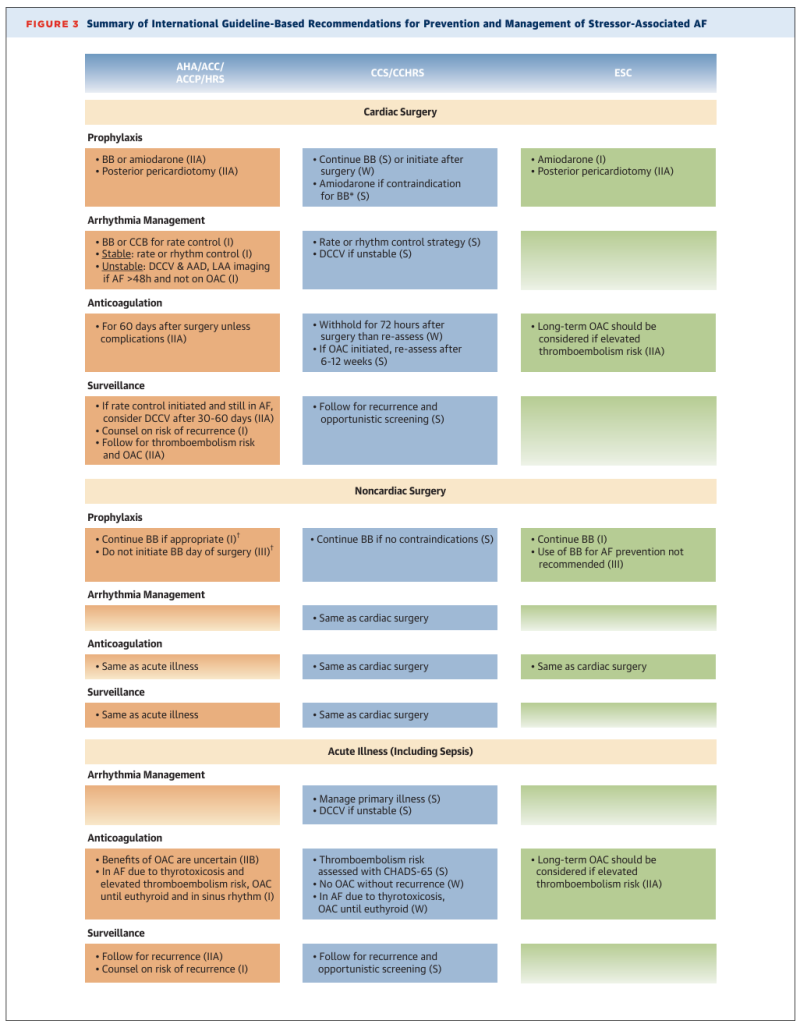
Aunque la contribución de la inflamación sistémica a la FA asociada a factores de estrés tras la cirugía cardíaca sigue sin estar del todo definida, se ha observado sistemáticamente que la inflamación local auricular y pericárdica secundaria a la acumulación de sangre mediastínica en el espacio pericárdico produce anomalías de la conducción comparables a las observadas en estados inflamatorios sistémicos. Estas observaciones sentaron las bases teóricas de un ensayo aleatorizado de pericardiotomía posterior para la prevención de la FA posoperatoria, en el que 420 pacientes sometidos a cirugía cardíaca fueron asignados a pericardiotomía posterior o a la atención habitual. El ensayo halló que la pericardiotomía redujo a la mitad el riesgo tanto de derrame pericárdico como de FA asociada a factores de estrés, lo que condujo a la inclusión de la profilaxis con pericardiotomía posterior en las directrices internacionales (Tabla 3, Figuras 2 y 3).
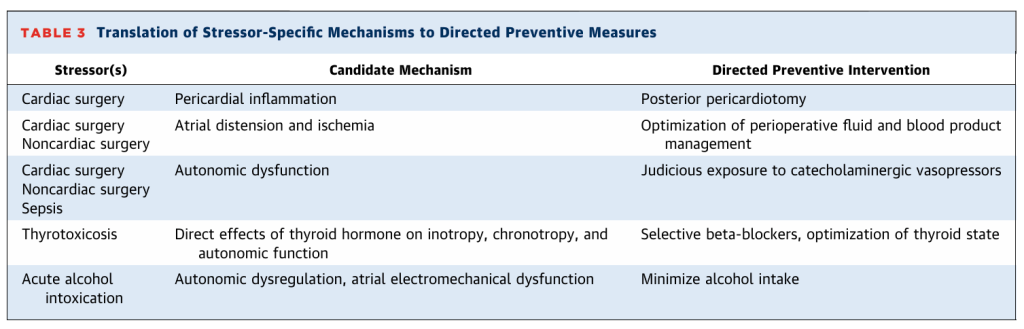
La grasa epicárdica, cada vez más reconocida como un posible contribuyente tanto a la FA primaria como a la FA postoperatoria, se perfila como una diana terapéutica para la prevención de la FA asociada a factores de estrés. Se ha planteado la hipótesis de que la grasa epicárdica contribuye a las arritmias auriculares a través de dos mecanismos principales: 1) cambios fibróticos causados por la infiltración local de tejido adiposo en el miocardio auricular; y 2) regulación positiva de las cascadas inflamatorias impulsadas por la señalización paracrina de los adipocitos. 82,83 La evidencia clínica que demuestra que la supresión de la actividad de la grasa epicárdica con toxina botulínica reduce la recurrencia de la FA en pacientes con FA establecida ha motivado el estudio de su posible papel en la prevención de la FA asociada a factores de estrés. El estudio NOVA (Toxina Botulínica Tipo A [AGN-151607] para la Prevención de la Fibrilación Auricular Postoperatoria en Participantes Adultos Sometidos a Cirugía Cardíaca de Tórax Abierto), un ensayo aleatorizado de 330 pacientes sometidos a cirugía cardíaca aleatorizados 1:1:1 a inyección intraoperatoria de almohadilla grasa epicárdica con placebo, 125 U y 250 U de toxina botulínica A (AGN-151607), no mostró una reducción significativa de la FA postoperatoria o rehospitalizaciones en la cohorte general del estudio, aunque hubo una señal hacia un beneficio potencial en pacientes mayores sometidos a CABG aislada, lo que merece más investigación.
Isquemia miocárdica
Se cree que los síndromes isquémicos miocárdicos contribuyen a la FA asociada a factores de estrés mediante la isquemia del miocardio auricular, que altera la conducción eléctrica, y la disfunción ventricular izquierda, que aumenta la presión auricular izquierda y la tensión parietal. En un estudio prospectivo de 109 pacientes sometidos a angioplastia de las arterias coronarias derecha o circunfleja (que normalmente irrigan el miocardio auricular), se observó que aquellos con oclusión inadvertida de la rama auricular tras una intervención percutánea presentaban tasas más altas de FA perioperatoria en comparación con aquellos sin oclusión de la rama auricular (12 % frente a 0 %). 85 En concordancia, un estudio retrospectivo de 42 pacientes informó tasas más altas de infarto de miocardio de la arteria coronaria inferior/derecha en aquellos con FA asociada a factores de estrés en comparación con pacientes de referencia emparejados sin FA (86 % frente a 33 %). Este estudio también demostró que la presión diastólica ventricular izquierda elevada se asociaba con la FA asociada a factores de estrés, independientemente de la función sistólica. Esta observación está respaldada por modelos animales en los que los aumentos agudos de la presión auricular indujeron una vulnerabilidad reversible a la FA. Los factores perioperatorios asociados con el aumento de la presión auricular izquierda, como el balance hídrico positivo (y la correspondiente elevación de la fracción aminoterminal del propéptido natriurético tipo B), la transfusión intraoperatoria y la ventilación prolongada, también se han asociado con el riesgo de FA asociada a factores de estrés. Por consiguiente, optimizar el manejo de líquidos y hemoderivados puede representar una estrategia modificable para reducir el riesgo de FA en este contexto (Tabla 3, Figura 2).
A diferencia de la lesión isquémica aguda causada por la obstrucción coronaria, la cirugía cardíaca se asocia principalmente con la lesión por isquemia-reperfusión, que promueve la remodelación proarrítmica mediante mecanismos como la inflamación tisular, la disfunción mitocondrial y la apoptosis. La evidencia histopatológica de lesión tisular auricular en individuos con FA postoperatoria tras una derivación cardíaca justificó un ensayo con 2103 pacientes aleatorizados a cirugía de derivación coronaria con o sin bomba, que encontró tasas equivalentes de FA postoperatoria (25% frente a 27%). 95,97-99 Por lo tanto, se necesitan más estudios para comprender mejor los posibles mecanismos de la lesión por isquemia-reperfusión en la cirugía cardíaca e identificar posibles dianas para mitigar la lesión (y quizás reducir el riesgo de FA asociada a factores de estrés) durante la derivación cardiopulmonar.
Disfunción autonómica
La desregulación autonómica es un factor bien reconocido, comúnmente presente en múltiples factores estresantes de la FA, como la sepsis, el infarto de miocardio (IM) y la cirugía poscardíaca y no cardíaca, entre otros. La activación de las ramas simpática y parasimpática del sistema nervioso autónomo puede inducir cambios proarrítmicos que inducen actividad ectópica y alteran el sustrato auricular. La estimulación simpática aumenta la liberación intracelular de calcio, lo que promueve posdespolarizaciones tardías y prolonga la duración del potencial de acción. Clínicamente, esto se evidencia en la asociación de vasopresores catecolaminérgicos, que elevan el tono simpático, y su asociación con la FA asociada a factores estresantes en poblaciones con sepsis y cirugía (Tabla 3). La estimulación vagal, por su parte, acorta la refractariedad auricular al aumentar la actividad de I KACh, lo que resulta en heterogeneidad en la conducción auricular. Estudios en pacientes con FA tras un IM y cirugía cardíaca han demostrado una estrecha correlación temporal entre la aparición de la FA y los marcadores de desregulación autonómica, lo que proporciona evidencia fundamental de su relación.
Toxicosis (hormona tiroidea y alcohol)
El hipertiroidismo, incluso en niveles subclínicos, provoca una elevación de la frecuencia cardíaca basal y un aumento de la actividad ectópica supraventricular en los miocitos de las venas pulmonares, lo que, en conjunto, predispone a la FA. Si bien existe una sólida evidencia de un mecanismo causal que vincula la exposición aguda al alcohol con la FA en entornos controlados, aún no ha sido respaldada de forma concluyente por investigaciones epidemiológicas a gran escala. Se ha demostrado que la intoxicación alcohólica induce de forma aguda una desregulación autonómica y disfunción electromecánica auricular, ambas asociadas con la aparición de FA.
Genética de la fa asociada a factores de estrés
Estudios genéticos han identificado variantes comunes asociadas tanto a la FA asociada a factores de estrés como a la FA primaria, incluyendo PITX2 y NEURL, lo que evidencia una predisposición genética parcialmente compartida. Además, Kertai et al. 129 demostraron que la aplicación de una escala de riesgo poligénico (PRS) desarrollada en una población con FA primaria mejoró la predicción de la FA posoperatoria en una cohorte retrospectiva de 1047 pacientes sometidos a cirugía cardíaca. 130 Al añadirse a factores clínicos, la PRS aumentó la discriminación del modelo (cambio en el estadístico C: 0,04; IC del 95 %: 0,02-0,06) y la calibración, lo que sugiere que la predisposición genética a la FA primaria también influye en el riesgo de FA asociada a factores de estrés. En un estudio relacionado, la inclusión de una PRS de FA primaria también mejoró la predicción de la FA asociada a factores de estrés tras la revascularización coronaria (mediante intervención coronaria percutánea o CABG) en comparación con un modelo que utiliza únicamente factores clínicos, aunque el efecto fue más moderado (cambio en el estadístico C: 0,007; IC del 95 %: 0,005-0,01). La FA asociada a factores de estrés también puede estar asociada a variantes genéticas distintas de la FA primaria, como las identificadas cerca de LY96, que desempeña un papel en la activación inmunitaria innata y se cree que media la respuesta inflamatoria a la lesión por isquemia-reperfusión. Se necesitan más estudios que aprovechen cohortes más amplias de factores de estrés quirúrgicos y médicos más diversos para comprender mejor la base genética de la FA asociada a factores de estrés, lo que a su vez podría revelar nuevos paradigmas de tratamiento (Figura 1).
Predicción de la fa asociada a factores de estrés y resultados relacionados
Predicción de la FA asociada al estresor
Un sólido conjunto de evidencia, derivado en gran medida de poblaciones retrospectivas específicas para factores de estrés, como las sometidas a cirugía cardíaca o tras un infarto de miocardio, demuestra que los factores de riesgo de FA establecidos, como la edad avanzada, el sexo masculino, la hipertensión y la insuficiencia cardíaca, se asocian con el desarrollo de FA en individuos expuestos. Estas observaciones han impulsado importantes esfuerzos para perfeccionar los métodos de identificación de individuos con riesgo de FA asociada a factores de estrés. Las evaluaciones de las puntuaciones de riesgo validadas utilizadas en la FA primaria, como CHA₂DS₂-VASc, APPLE y HATCH, han mostrado un rendimiento limitado en poblaciones con cirugía cardíaca, infarto de miocardio y neumonía. En la población posoperatoria, puntuaciones más complejas que incorporan parámetros clínicos, ecocardiográficos o de procedimiento adicionales han mostrado pequeñas mejoras. En general, la modesta utilidad discriminante, la necesidad de cálculos engorrosos y la insuficiente evidencia de generalización han limitado el uso generalizado de cualquier método existente para estratificar el riesgo de un episodio de FA asociada a factores de estrés.
El uso de enfoques basados en inteligencia artificial (IA), que permiten la integración de información clínica con nuevas fuentes de datos como la telemetría y los ECG, ha demostrado un rendimiento notable en la predicción de enfermedades cardiovasculares, como anomalías cardíacas estructurales e incluso la fibrilación auricular (FA). Los primeros trabajos que exploran la aplicación de enfoques de IA a la predicción de la FA asociada a factores de estrés y sus consecuencias han sentado una base prometedora para futuras investigaciones. Zhang et al. demostraron que un modelo de IA entrenado con monitorización continua del ritmo cardíaco de 505 pacientes con FA y 885 pacientes sin FA pudo predecir la aparición de la FA asociada a factores de estrés en el intervalo de 10 minutos posterior, alcanzando una sensibilidad del 93 % y una especificidad del 97 %. En un estudio de 27.546 pacientes sometidos a cirugía cardíaca y no cardíaca sin antecedentes de FA, un modelo de IA que incorporaba formas de onda de ECG preoperatorio de 12 derivaciones y datos demográficos del paciente predijo el riesgo de FA asociada a factores de estrés a los 7 días con un estadístico C de 0,83 y un valor predictivo negativo del 99 %, superando a otros modelos contemporáneos que requieren datos clínicos detallados. Las futuras investigaciones que investiguen enfoques de modelado que integren datos adicionales de alta dimensión (p. ej., imágenes, nuevos biomarcadores y riesgo poligénico) con variables clínicas tienen el potencial de mejorar aún más la predicción del riesgo de FA asociada a factores de estrés. Para ello, la aplicación de estándares rigurosos a los modelos de IA, basados en los principios básicos de generalización, viabilidad, interoperabilidad, mitigación de sesgos y seguridad, es esencial para su integración exitosa en la práctica clínica. Al igual que con todos los modelos predictivos, la relevancia clínica de estratificar el riesgo de FA asociada a factores estresantes se maximizará al combinar las predicciones con acciones posteriores claras. En resumen, las estrategias actuales para predecir la FA asociada a factores estresantes están limitadas por un rendimiento modesto y requieren refinamiento y validación antes de su uso generalizado en la práctica clínica.
Estratificación del riesgo tromboembólico en la fa asociada a factores de estrés
Puntuaciones de riesgo clínico como CHA 2 DS 2 -VASc, CHA 2 DS 2 -VASc y CHADS-65, ampliamente utilizadas en el pronóstico primario de la FA, también se recomiendan en las guías para la estimación del riesgo tromboembólico tras la FA asociada a factores de estrés (Figura 3). 2,3,48 Datos retrospectivos de la población posoperatoria sugieren que puntuaciones más altas de CHA 2 DS 2 – VASc pueden estar asociadas con un mayor riesgo de accidente cerebrovascular isquémico tras cirugía cardíaca, pero la evidencia en cirugía no cardíaca es menos sólida. De forma similar, en la FA asociada a factores de estrés médicos, CHA 2 DS 2 -VASc discrimina el riesgo longitudinal de accidente cerebrovascular tras un infarto de miocardio, tirotoxicosis y neumonía, pero aún no ha demostrado utilidad para predecir el riesgo de accidente cerebrovascular tras sepsis.
Consecuencias de la FA asociada a factores de estrés
Eventos cardiovasculares adversos relacionados con la FA
La FA asociada a factores estresantes conlleva importantes implicaciones pronósticas, con tasas de eventos adversos cardiovasculares que se acercan a las observadas en la FA primaria (Tabla 4). Los pacientes con FA asociada a factores estresantes, en comparación con aquellos expuestos al mismo factor estresante pero sin FA, tienen una mayor utilización de recursos (p. ej., estancias hospitalarias más prolongadas y mayores costos de hospitalización) y enfrentan un mayor riesgo a corto y largo plazo de resultados cardiovasculares adversos mayores relacionados con la FA, incluyendo accidente cerebrovascular, tromboembolia sistémica, insuficiencia cardíaca y mortalidad. Un análisis post hoc de 3023 pacientes de cirugía cardíaca inscritos en el Ensayo de Revascularización Arterial informó tasas de incidencia acumulada del 6,3 % frente al 3,7 % para aquellos con y sin FA posoperatoria, respectivamente (HR: 1,53; IC del 95 %: 1,06-2,23), en particular para aquellos con puntuaciones elevadas de CHA 2 DS 2 -VASc (HR: 4,05; IC del 95 %: 2,54-6,46). De manera similar, el análisis de 2103 pacientes de cirugía cardíaca en el ensayo On Versus Off Bypass encontró una tasa significativamente mayor de mortalidad por cualquier causa al año (5,2 % en el grupo con FA asociada a factores de estrés frente al 2,3 % en el grupo sin FA; P < 0,05). 183 Los hallazgos de estudios prospectivos se han confirmado en amplios estudios retrospectivos, incluyendo un estudio de registro de 49 264 pacientes en la base de datos de la Sociedad de Cirujanos Torácicos, que informó que la FA asociada a factores de estrés después de la cirugía cardíaca se asoció con una probabilidad de mortalidad dos veces mayor (4,0 % frente al 1,7 % para la FA asociada a factores de estrés y sin FA, respectivamente), con los correspondientes aumentos en la duración de la estancia en la unidad de cuidados intensivos (48 horas), la duración de la estancia hospitalaria (3 días) y el coste total de la hospitalización (9000 dólares). Amplios metaanálisis de pacientes con FA asociada a cirugía cardíaca han mostrado un aumento del doble en los riesgos perioperatorios y a largo plazo de accidente cerebrovascular y mortalidad, en comparación con los pacientes sin FA. En general, las tasas de incidencia acumulada perioperatoria informadas varían de aproximadamente 1,9% a 5,3% para accidente cerebrovascular y de 1,8% a 6% para mortalidad, mientras que las tasas de incidencia acumulada a largo plazo varían de 1,5% a 6,3% para accidente cerebrovascular y de 6% a 30,2% para mortalidad.
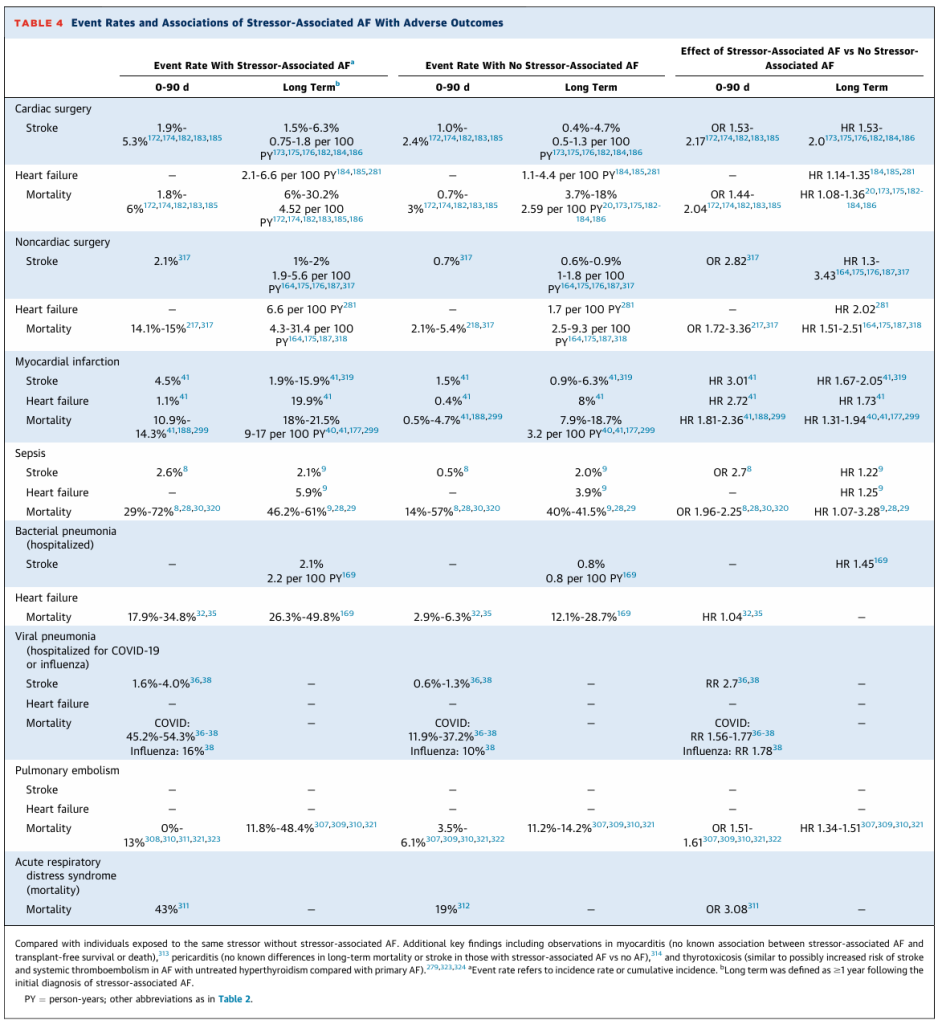
Los resultados tras la FA asociada a factores de estrés tras una cirugía no cardíaca son similarmente peores en comparación con los de las personas sin FA. En un análisis post hoc de 18 117 pacientes incluidos en los ensayos POISE (Evaluación Perioperatoria Isquémica) I y II, la FA asociada a factores de estrés se asoció significativamente con resultados adversos a un año, incluyendo ictus (5,58 frente a 1,54 eventos por 100 personas-año [PA]; HR: 3,43; IC del 95 %: 2,00-5,90), mortalidad por cualquier causa (31,37 frente a 9,34 eventos por 100 personas-año; HR: 2,51; IC del 95 %: 2,01-3,14) e infarto de miocardio (2,62 frente a 0,82 eventos por 100 personas-año; HR: 5,10; IC del 95 %: 3,91-6,64), en comparación con las personas sin FA. Cabe destacar que, en un metanálisis de 35 estudios de FA posoperatoria (n = 2.458.010), los pacientes con FA asociada a factores estresantes de cirugía no cardíaca pueden tener tasas más altas de accidente cerebrovascular en comparación con los pacientes con FA asociada a factores estresantes de cirugía cardíaca, aunque se desconoce el factor subyacente de esta diferencia observada.
En un estudio de seguimiento del ensayo APEX-AMI (Pexelizumab en conjunción con angioplastia en infarto agudo de miocardio), en el que participaron 5745 pacientes con infarto agudo de miocardio (IM) con elevación del segmento ST, la FA asociada a factores de estrés se asoció significativamente con los resultados a 90 días, incluyendo mortalidad (HR: 1,81; IC del 95 %: 1,06-3,09), insuficiencia cardíaca (HR: 2,66; IC del 95 %: 1,74-4,06) e ictus (HR: 2,98; IC del 95 %: 1,47-6,04), con resultados similares observados en estudios poblacionales (Tabla 4). Un inicio más temprano de la FA en relación con el IM y una mayor carga de FA podrían estar asociados con un mayor riesgo de eventos adversos. En el estudio prospectivo de 1.782 pacientes con sepsis analizado anteriormente, la FA asociada a factores de estrés se asoció con un mayor riesgo de muerte (29% frente a 14%; HR: 2,10; IC del 95%: 1,61-2,73) y, asimismo, se encontró que se asocia con mayores riesgos de insuficiencia cardíaca y accidente cerebrovascular en estudios basados en registros y metanálisis.
Recurrencia de FA
Estudios poblacionales, incluido el Framingham Heart Study, basados principalmente en la determinación clínicamente desencadenada (p. ej., FA clínicamente manifiesta), han reportado tasas de recurrencia de FA comparables a las de la FA primaria, con estimaciones de incidencia acumulada del 20 % al año, de ∼40 % a 50 % a los 5 años y de ∼55 % a los 10 años (Tabla 2). Sin embargo, como se observó con la incidencia de FA asociada a factores de estrés, los informes que utilizan la monitorización sistemática para la vigilancia han mostrado tasas de recurrencia aún más altas. Por ejemplo, un estudio prospectivo de 139 participantes con FA asociada a factores de estrés médicos y posoperatorios identificó una tasa de recurrencia al año del 32,3 % utilizando la monitorización periódica del ritmo de 14 días, en comparación con el 3,0 % en el grupo de atención habitual. Como era de esperar, los monitores de ritmo invasivos arrojan las tasas más altas de recurrencia de FA. En un metaanálisis (8 estudios; n = 185) de pacientes con FA asociada a factores estresantes de cirugía cardíaca que recibieron registradores de bucle implantables, la tasa de recurrencia a un año fue del 30,1 % a los 12 meses, aunque las tasas de recurrencia han llegado al 76 % en estudios prospectivos más pequeños. Los datos de estudios de monitorización intensiva en la población de cirugía cardíaca han demostrado además que la recurrencia tiende a ocurrir más cerca del inicio de la FA asociada a factores estresantes, pero el riesgo de recurrencia persiste durante los años posteriores.
Incluso dentro de las limitaciones de los métodos de vigilancia empleados por estudios individuales, las tasas de recurrencia de la cirugía no cardíaca y la FA asociada a factores estresantes no quirúrgicos son sustanciales. Un metaanálisis de 13 estudios (n = 25.726) que evaluaron la FA posoperatoria después de cirugía no cardíaca informó tasas de recurrencia que oscilaron entre el 0% y el 37,3%. Sin embargo, solo un estudio pequeño empleó un protocolo de monitoreo sistemático, y pocos incluyeron un seguimiento ambulatorio de ECG de rutina en toda la cohorte del estudio. En un gran estudio de registro nacional de casi 50.000 pacientes daneses con FA asociada a infección, la tasa de recurrencia a 1 año determinada utilizando códigos de facturación de alta especificidad fue de aproximadamente el 36%, con variabilidad según la etiología infecciosa, probablemente reflejando diferencias subyacentes en la gravedad de la enfermedad. De manera similar, en un estudio del mismo registro danés, la tasa de recurrencia a 1 año después de la neumonía bacteriana fue del 20,5% (IC del 95%: 19,6%-21,5%). En estudios de FA asociada a factores estresantes después de un infarto de miocardio que utilizaron un seguimiento protocolizado integral con proveedores y ECG, las tasas observadas oscilaron entre el 15 % y el 22 %.En el contexto de la FA tirotóxica, se han informado tasas de recurrencia de entre el 25 % y el 60 %, con tasas más altas asociadas con una mayor duración de la FA antes de alcanzar un estado eutiroideo.
Las tasas de recurrencia probablemente reflejan tanto la influencia variable del sustrato inducido por el estresor como los perfiles de riesgo típicos de las personas expuestas a estresores específicos (Figura 1). Generalmente, las tasas más bajas de recurrencia de FA después de la cirugía cardíaca pueden deberse a la naturaleza localizada de la inflamación pericárdica y auricular. De igual manera, el tratamiento oportuno del hipertiroidismo y el mantenimiento de un estado eutiroideo se asocian con una rápida recuperación del ritmo sinusal en la mayoría de los pacientes. Por el contrario, los estresores con tasas de recurrencia más altas a largo plazo, como la sepsis, pueden provocar efectos estresantes más pronunciados y duraderos sobre el sustrato auricular, incluyendo la remodelación eléctrica y estructural debida a la inflamación sistémica prolongada. Además, las características típicas de los pacientes que presentan sepsis pueden reflejar inherentemente una población con mayor susceptibilidad basal a la FA. En otras palabras, dentro de nuestro marco fisiopatológico delineado de la FA asociada a factores de estrés, ciertos factores de estrés (p. ej., cirugía cardíaca, tirotoxicosis) tienen mayor probabilidad de resultar en episodios de FA asociados a factores de estrés más cercanos al extremo de «FA reversible» del espectro, mientras que otros (p. ej., sepsis, infarto de miocardio) son relativamente ricos para episodios de FA más cercanos al extremo de «FA provocada». Una variante clínicamente reconocida de «FA reversible» asociada a factores de estrés incluye episodios tempranos de FA que ocurren durante el período de blanqueo después de la ablación. Se hipotetiza que las recurrencias tempranas de FA dentro de las primeras 4 a 8 semanas después de la ablación con catéter involucran inflamación y edema auricular inducidos por la ablación, y como era de esperar, tales episodios no se han asociado confiablemente con la recurrencia posterior de FA.
Predecir el riesgo de FA recurrente tras un episodio de FA asociada a un factor estresante es esencial para cuantificar el riesgo de ictus y orientar las decisiones individualizadas sobre la monitorización del ritmo cardíaco y la anticoagulación oral (ACO) a largo plazo. Sin embargo, los factores clínicos tradicionalmente asociados con el riesgo primario de FA, como la edad y la hipertensión, han mostrado asociaciones inconsistentes con el riesgo de recurrencia en el contexto de la FA asociada a un factor estresante. Por ejemplo, si bien algunos estudios han sugerido que la edad avanzada se asocia con la recurrencia tras la cirugía cardíaca (HR por incremento de 1 año: 1,05; IC del 95 %: 1,03-1,06) y el infarto de miocardio (HR por incremento de 1 año: 1,05; IC del 95 %: 1,03-1,07), otros análisis prospectivos no han confirmado estos hallazgos. La limitada utilidad predictiva de los factores de riesgo clínicos por sí solos se demostró en un estudio de 314 pacientes con FA asociada a factores de estrés tras cirugía no cardíaca. Los autores observaron que las covariables clínicas incluidas en la escala CHARGE-AF predecían deficientemente el riesgo de recurrencia futura (estadístico C: 0,59). Si bien las personas con FA asociada a factores de estrés suelen presentar una alta carga de comorbilidades cardíacas, lo que puede reducir la utilidad de los modelos de riesgo tradicionales, los marcadores estructurales del remodelado auricular, en particular la dilatación auricular izquierda, han mostrado cierta asociación con el riesgo de recurrencia. Es posible que los modelos que integran parámetros ecocardiográficos, biomarcadores adicionales de distensión auricular izquierda, como la fracción aminoterminal del propéptido natriurético cerebral, u otros tipos de datos novedosos, puedan mejorar el rendimiento predictivo.
Importancia pronóstica de la recurrencia de FA y la carga de la FA
La recurrencia, cuando ocurre, es claramente importante para el pronóstico. En un estudio retrospectivo de 315 pacientes con FA asociada a factores estresantes de cirugía no cardíaca, Hyun et al. encontraron tasas significativamente más altas de hemorragia mayor (26,9 % frente a 4,1 %) y tromboembolia (11,2 % frente a 0,8 %) entre individuos con FA recurrente y sin ella. De manera similar, en un estudio de cohorte que incluyó a 2089 (19 %) pacientes con FA asociada a factores estresantes entre 10 723 pacientes con un nuevo diagnóstico de FA, Wang et al. 4 encontraron que la recurrencia de FA variable en el tiempo se asoció con riesgos notablemente mayores de resultados adversos, con HR ajustados de 4,2 (IC del 95 %: 3,0-5,9), 1,7 (IC del 95 %: 1,1-2,7) y 3,8 (IC del 95 %: 3,2-4,5) para insuficiencia cardíaca, accidente cerebrovascular isquémico y mortalidad por cualquier causa, respectivamente.
El aumento de la carga de FA durante un episodio asociado a un factor estresante, que probablemente indica una mayor predisposición subyacente a la FA, se ha asociado con un mayor riesgo de resultados adversos relacionados con la FA, incluida la recurrencia de la FA. Un estudio de 278 personas con FA asociada a un infarto de miocardio cuantificó la carga de FA hospitalaria mediante monitorización continua y midió su asociación con los resultados clínicos a largo plazo. Encontraron que, en comparación con una carga baja, una carga hospitalaria >10% se asoció con un aumento de dos veces en las tasas de accidente cerebrovascular isquémico (2,20 eventos por 100 años al año; IC del 95%: 1,05-4,61 frente a 4,42 eventos por 100 años al año; IC del 95%: 2,21-8,85), insuficiencia cardíaca (11,35 eventos por 100 años al año; IC del 95%: 8,02-16,04 frente a 31,67 eventos por 100 años al año; IC del 95%: 23,49-43,70) y mortalidad por todas las causas (9,00 eventos por 100 años al año; IC del 95%: 6,26-12,96 frente a 17,41 eventos por 100 años al año; IC del 95%: 12,38-24,49). Sin embargo, se requieren estudios futuros para evaluar cómo el patrón de FA (p. ej., paroxística vs. persistente) y la carga pueden modular los efectos observados de la recurrencia de FA en los resultados tras la FA asociada a factores de estrés y afectar el tratamiento. En conjunto, estos datos sugieren que la recurrencia de FA es frecuente (ocurre entre el 20 % y el 50 % de los pacientes en un plazo de un año), está fuertemente asociada a resultados adversos y sigue siendo difícil de predecir.
Diferencias demográficas en la incidencia y los resultados de la FA asociada a factores de estrés
Además de la edad avanzada y el sexo masculino, la raza blanca autodeclarada también se ha asociado con un mayor riesgo de FA tras una cirugía cardíaca. Si bien las contribuciones relativas de los factores genéticos y ambientales que subyacen a esta asociación son complejas y no se comprenden del todo, los hallazgos que asocian el grado de ascendencia europea con el riesgo de FA entre las personas negras autodeclaradas respaldan la presencia de un componente genético en el riesgo de FA asociada a factores de estrés. En consonancia con estas observaciones, también se ha observado que los pacientes blancos autodeclarados tienen un mayor riesgo de FA asociada a factores de estrés en poblaciones de cirugía cardíaca y no cardíaca. Un estudio de 21.458 pacientes sometidos a cirugía cardíaca, de los cuales 1.176 (5,5%) eran negros, reveló que los pacientes blancos tenían mayor probabilidad de desarrollar FA asociada a factores de estrés que los pacientes negros tras el emparejamiento por puntuación de propensión para comorbilidades, parámetros ecocardiográficos (incluido el tamaño de la aurícula izquierda) y factores sociales (OR: 1,74; IC del 95%: 1,70-1,78). Aunque menos caracterizados, los pacientes hispanos también podrían tener un menor riesgo de FA posoperatoria tras cirugía cardíaca y no cardíaca. A pesar del ajuste por factores clínicos y sociales conocidos, es importante destacar que la incidencia variable de FA asociada a factores estresantes según la raza podría estar parcialmente determinada por factores que afectan la probabilidad de diagnóstico de FA (p. ej., prácticas de monitorización, diferencias en el perfil sintomático, acceso a la atención clínica, etc.).
Si bien la incidencia observada de FA posoperatoria puede variar según la raza, su asociación con los resultados es menos clara. En un estudio con 1215 pacientes sometidos a cirugía cardíaca electiva (13 % de raza negra), la mortalidad operatoria entre los pacientes de raza negra fue mayor en aquellos con FA asociada a factores de estrés (riesgo relativo ajustado [RR]: 5,0; IC del 95 %: 1,3-13), y los pacientes de raza negra con FA asociada a factores de estrés presentaron un riesgo dos veces mayor de muerte operatoria en comparación con los pacientes de raza blanca con FA asociada a factores de estrés. Sin embargo, Rader et al. observaron que, si bien los pacientes de raza negra parecían presentar una mayor tasa de trombosis venosa, no se observaron diferencias en otros resultados adversos relacionados con la FA, como ictus, insuficiencia cardíaca o mortalidad hospitalaria. Por el contrario, un análisis de 294.112 pacientes de la Muestra Nacional de Pacientes Internados sometidos a cirugía no cardíaca informó que, en comparación con los pacientes blancos, tanto los pacientes negros (OR: 0,70; IC del 95 %: 0,55-0,89) como los hispanos (OR: 0,62; IC del 95 %: 0,44-0,86) tenían un menor riesgo de mortalidad, mientras que el estado de seguro no privado y los ingresos más bajos se asociaron con una mayor mortalidad.
La influencia del sexo en el pronóstico también está menos definida. En un análisis retrospectivo de 21.568 pacientes sometidos a cirugía cardíaca, de los cuales aproximadamente el 40% desarrolló FA de nueva aparición, las mujeres presentaron una menor probabilidad de FA posoperatoria (OR: 0,85; IC del 95%: 0,79-0,91) en comparación con los hombres, pero en comparación con los hombres con FA posoperatoria, las mujeres con FA posoperatoria mostraron un riesgo de mortalidad un 12% mayor (IC del 95%: 1,02-1,23). Por el contrario, un amplio estudio basado en reclamaciones de 294.112 personas con FA posoperatoria no encontró una diferencia significativa según el sexo en la mortalidad hospitalaria. Claramente, se necesita una mejor comprensión de los posibles impactos de los determinantes sociodemográficos y sociales en la aparición y el pronóstico de la FA asociada a factores de estrés.
Prevención y manejo de la FA asociada a factores de estrés
Factores de riesgo modificables en la prevención y detección de la FA asociada a factores de estrés
La optimización de los factores de riesgo modificables que aceleran la remodelación auricular estructural y funcional fisiopatológica es esencial para prevenir la FA primaria y la asociada a factores de estrés (Figura 1). Dichos factores de riesgo incluyen la insuficiencia cardíaca, la inactividad física, la hipertensión arterial, la diabetes tipo 2, el tabaquismo, la obesidad, el consumo de alcohol y la calidad del sueño (Figura 2). Si bien la naturaleza esporádica e imprevista de los factores de estrés médicos hace que su aparición a menudo sea impredecible, los procedimientos quirúrgicos planificados pueden brindar una oportunidad para orientar las medidas preoperatorias de modificación del estilo de vida (p. ej., pérdida de peso, abandono del hábito tabáquico) hacia las personas con mayor riesgo de FA asociada a factores de estrés y eventos adversos relacionados con ella.
Más allá de la modificación de los factores de riesgo, no existe una función clara para el cribado electrocardiográfico adicional para la FA subclínica antes de la cirugía, fuera de la evaluación del riesgo cardíaco preoperatorio basada en las directrices actuales. Entre las posibles barreras para un cribado amplio en este contexto se incluyen: 1) la probable baja rentabilidad diagnóstica en pacientes de bajo riesgo que no cumplen los criterios existentes para el cribado electrocardiográfico; 2) la escasa evidencia del beneficio clínico de la detección de la FA en estas poblaciones, basada en estudios de cribado en FA primaria; y 3) la ausencia de evidencia que respalde la rentabilidad.
Profilaxis farmacológica
El uso de betabloqueantes perioperatorios o amiodarona puede considerarse para reducir la incidencia de FA asociada a factores de estrés en pacientes sometidos a cirugía cardíaca, y puede ser de especial importancia en individuos con alto riesgo de FA posoperatoria (Figura 2, Tabla 3). En pacientes sometidos a cirugía cardíaca, los betabloqueantes redujeron significativamente la incidencia de FA (16,3 eventos menos por 100 personas-año; RR: 0,50; IC del 95%: 0,42-0,59; 40 estudios, 5650 participantes) sin bradicardia significativa, hipotensión ni infarto de miocardio (IM). Si bien los betabloqueantes tienen una eficacia similar para reducir la incidencia de FA en pacientes sometidos a cirugía no cardíaca (26 eventos menos por 1000 personas-año; RR: 0,41; IC del 95%: 0,21-0,79; 9 estudios, 9080 participantes), las guías clínicas advierten contra su introducción perioperatoria debido al mayor riesgo de eventos adversos, incluida la mortalidad.
El Estudio de Evaluación Isquémica Perioperatoria, un ensayo clínico de 8351 pacientes sometidos a cirugía no cardíaca de riesgo intermedio a alto en el que los pacientes fueron aleatorizados para iniciar un nuevo tratamiento con metoprolol perioperatorio o placebo, informó que el betabloqueo iniciado en el período perioperatorio aumentó significativamente el riesgo de muerte (3,1 % frente al 2,1 % en el grupo placebo) y accidente cerebrovascular (1,0 % frente al 0,5 %). En un metanálisis a gran escala, los betabloqueantes redujeron significativamente la incidencia de FA (RR: 0,41; IC del 95 %: 0,21-0,79; 9 estudios, 9080 participantes) a expensas de la bradicardia (RR: 2,49; IC del 95 %: 1,74-3,56; 49 estudios, 12 239 participantes) y la hipotensión (RR: 1,40; IC del 95 %: 1,29-1,51; 49 estudios, 12 304 participantes).
Evidencia sustancial apoya el uso de amiodarona profiláctica en cirugía cardíaca (Figuras 2 y 3). El ensayo PAPABEAR (Amiodarona para prevenir arritmias postoperatorias), que aleatorizó a 601 pacientes sometidos a cirugía cardíaca no urgente a amiodarona perioperatoria frente a placebo, informó una disminución del 50% en la tasa de arritmias auriculares (16,1% frente a 29,5% en placebo; HR: 0,52; IC del 95%: 0,34-0,69). 231 El beneficio de la amiodarona se mantuvo en un subgrupo preespecificado de 344 pacientes que recibieron betabloqueantes preoperatorios (27 [15,3%] frente a 42 [25,0%]; HR: 0,58; IC del 95%: 0,34-0,99). La eficacia de la amiodarona se ve respaldada por un metaanálisis de 18 ensayos con 3295 pacientes, en el que la amiodarona redujo la incidencia de FA al 3,2 % frente al 19,8 % en el grupo control (OR: 0,48; IC del 95 %: 0,40-0,57). Cabe destacar que un metaanálisis de ensayos comparativos que compararon la profilaxis con betabloqueantes y amiodarona en pacientes sometidos a cirugía cardíaca no mostró diferencias entre la incidencia de FA ni la duración de la estancia hospitalaria entre los grupos, aunque la retirada obligatoria de betabloqueantes en el grupo de amiodarona podría haber sesgado estos hallazgos. Estudios más pequeños han sugerido una mayor eficacia de la terapia combinada con amiodarona y betabloqueantes. Actualmente no se ha establecido ningún papel de la amiodarona para prevenir la FA asociada a factores estresantes en poblaciones quirúrgicas no cardíacas, aunque estudios más pequeños, incluido un ensayo de 130 pacientes sometidos a resección pulmonar en el que la amiodarona redujo la incidencia de FA del 32% al 14% (reducción del riesgo relativo del 57%), respaldan su uso.
Aunque los betabloqueantes, la amiodarona y la pericardiotomía posterior parecen reducir el riesgo de FA asociada a factores de estrés tras la cirugía cardíaca, una revisión Cochrane no encontró asociación entre estas intervenciones preventivas y un menor riesgo de ictus, mortalidad cardiovascular o mortalidad por cualquier causa. Además, el uso de profilaxis perioperatoria de la FA en la población de cirugía cardíaca sigue siendo bajo, ya que menos de un tercio de los profesionales utilizan betabloqueantes perioperatorios o amiodarona en pacientes de alto riesgo.
Los datos que respaldan las medidas preventivas para la FA asociada a factores de estrés médico son comparativamente limitados (Figura 2, Tabla 3). El ensayo CAPRICORN (CArvedilol PostinfaRct survIval COntRolled evaluatioN) aleatorizó a 1959 pacientes con insuficiencia cardíaca con fracción de eyección reducida e infarto agudo de miocardio (IMC) en los 3 a 21 días previos a recibir carvedilol o placebo, y observó que el carvedilol redujo significativamente la incidencia de FA (2,3 % frente al 5,4 % en el grupo placebo; HR: 0,41). Si bien un subestudio del ensayo TRACE (Trandolapril Cardiac Evaluation) también sugirió cierto beneficio de la inhibición de la ECA en la prevención de la FA tras un IAM en pacientes con insuficiencia cardíaca con fracción de eyección reducida, estudios más amplios con datos poblacionales no han respaldado este hallazgo ni en poblaciones con insuficiencia cardíaca con fracción de eyección reducida ni en poblaciones con IAM.
La elección del vasopresor en la sepsis parece afectar el riesgo de FA: en un metaanálisis que incluyó a 1462 pacientes, la adición de vasopresina a los vasopresores de catecolaminas se asoció con un menor riesgo de FA asociada a factores de estrés (68 episodios incidentes menos de FA asociada a factores de estrés por 1000 años-año en el grupo de vasopresina frente al grupo sin vasopresina; RR: 0,77). En un ensayo con 1679 pacientes con shock séptico aleatorizados a dopamina o noradrenalina, el uso de dopamina aumentó significativamente la tasa de arritmias, en particular la FA (21 % frente a 11 %), aunque los pacientes no fueron excluidos por antecedentes de FA. Sin embargo, en general, nuestro conocimiento sobre el posible papel de los enfoques para prevenir la FA asociada a factores de estrés en el contexto de factores de estrés no quirúrgicos es limitado.
Vigilancia del ritmo longitudinal
Las recomendaciones actuales para la monitorización del ritmo a corto plazo (es decir, 30-60 días) tras un episodio de FA asociada a un factor de estrés tras una cirugía cardíaca se basan principalmente en un ensayo con 523 pacientes con FA asociada a un factor de estrés tras una cirugía cardíaca que fueron aleatorizados a una estrategia de control del ritmo o de la frecuencia (Tabla 3). El estudio observó que entre los pacientes con un ritmo sin FA desde el alta hasta los 7 días, el 84,2 % del grupo de control de la frecuencia y el 86,9 % del grupo de control del ritmo permanecieron libres de FA durante un seguimiento de 60 días, lo que indica que muchos pacientes con ritmo sin FA tras un episodio de FA asociada a una cirugía cardíaca revertirán a la sinusitis, al menos a corto plazo. Sin embargo, cada vez hay más pruebas que indican que más del 20 % de las recurrencias tras una FA asociada a un factor de estrés se producen después de los 30 a 60 días iniciales de monitorización, lo que sugiere que este periodo avalado por las directrices probablemente sea insuficiente.
Dadas las altas tasas de recurrencia a largo plazo de la FA asociada a factores de estrés, la posible subestimación de las tasas de recurrencia en ausencia de monitorización continua y las asociaciones consistentes entre la recurrencia de la FA y los eventos adversos relacionados con la FA, es razonable considerar estrategias de monitorización más intensivas (Figura 2). Dichas estrategias pueden incluir ECG periódicos, monitores de parche o grabadoras de bucle implantables, especialmente para pacientes con factores de riesgo de ictus que no reciben ACO. Dada la considerable demanda de recursos de las grabadoras de bucle implantables y la creciente disponibilidad de tecnologías de salud digital capaces de detectar la FA (p. ej., dispositivos portátiles de ECG de una sola derivación para el consumidor), evaluar la eficacia de estas herramientas para la monitorización tras la FA asociada a factores de estrés representa una importante prioridad de investigación. Cabe destacar que, si bien la evidencia actual respalda la capacidad de muchos dispositivos portátiles y de consumo para detectar la FA, los valores predictivos positivos en la práctica clínica siguen siendo solo moderados, y generalmente se recomienda confirmarlos con monitorización de grado clínico. En el futuro, herramientas de estratificación del riesgo más precisas podrían priorizar mejor la monitorización intensiva (p. ej., grabadoras de bucle implantables, monitorización portátil con capacidad de ECG) hacia las personas con mayor riesgo de recurrencia de la FA.
Manejo de arritmias
Las directrices actuales apoyan el uso del control de la frecuencia (p. ej., betabloqueantes) o el control del ritmo (p. ej., fármacos antiarrítmicos) en pacientes posoperatorios hemodinámicamente estables (Figuras 2 y 3). En un metaanálisis de ensayos controlados aleatorizados que evaluaron el control de la frecuencia frente al del ritmo en la FA asociada a factores estresantes de la cirugía cardíaca (8 estudios), no hubo diferencias en la recurrencia de la FA a los 3 meses ni en la mortalidad perioperatoria, aunque las tasas generales de eventos fueron bajas, con 37 recurrencias y 25 muertes, respectivamente. Si bien hay relativamente menos datos que comparen el control de la frecuencia y el ritmo en la población de cirugía no cardíaca, el control del ritmo parece ser más eficaz en la conversión a ritmo sinusal (RR: 1,93), como se esperaba. En pacientes con mala tolerancia a la FA, como los que experimentan inestabilidad hemodinámica o insuficiencia cardíaca, se recomienda la cardioversión sincronizada. Esto puede ir acompañado de la consideración de fármacos antiarrítmicos y la obtención de imágenes de la orejuela auricular izquierda para descartar un trombo antes de realizar la cardioversión.
Las recomendaciones sobre los agentes específicos para el control de la frecuencia cardíaca y el ritmo en la sepsis se ven limitadas por la falta de evidencia concluyente de ensayos aleatorizados y los resultados mixtos de estudios de cohorte retrospectivos. Si bien los pacientes hemodinámicamente inestables justifican la cardioversión sincronizada, también se pueden considerar los medicamentos intravenosos para pacientes estables o semiestables. Los primeros datos aleatorizados sugirieron que la amiodarona mejoró el control de la arritmia con menores tasas de interrupción del fármaco en comparación con los bloqueadores de los canales de calcio. Sin embargo, la evidencia actual indica que, en comparación con la amiodarona intravenosa, los betabloqueantes intravenosos pueden tener una eficacia equivalente o incluso superior en pacientes con sepsis tanto para el control de la frecuencia cardíaca como del ritmo, así como tasas equivalentes o inferiores de eventos adversos, incluida la hipotensión.
En la FA asociada al hipertiroidismo, se recomiendan betabloqueantes selectivos, que reducen los síntomas sistémicos (p. ej., palpitaciones) e inhiben en cierta medida la conversión periférica de T4 a T3. En particular, en la enfermedad de Graves, la tiroidectomía también ha demostrado resolver las arritmias y podría ser más eficaz que la terapia con yodo radiactivo para lograr la resolución de las arritmias en esta población.
Las estrategias para mitigar el riesgo a largo plazo de recurrencia de FA después de una FA asociada a factores estresantes son comparativamente escasas, y se necesitan investigaciones futuras para evaluar la efectividad comparativa de las estrategias de control de frecuencia frente a las de control del ritmo (médicas o basadas en catéter), tanto para la FA asociada a factores estresantes posoperatorios como médicos.
Anticoagulación en FA postoperatoria
Aunque las guías actuales indican que el uso de ACO es razonable en pacientes con FA posoperatoria con alto riesgo tromboembólico, los resultados contradictorios de estudios retrospectivos y la falta de evidencia de ensayos aleatorizados han generado incertidumbre (Figuras 2 y 3). En un estudio retrospectivo de 2985 pacientes con FA poscirugía cardíaca, de los cuales 612 (20,5%) fueron dados de alta con warfarina, el uso de ACO se asoció con una menor mortalidad ajustada (HR: 0,78; IC del 95%: 0,66-0,92) durante un seguimiento medio de 6 años. Sin embargo, en un estudio poblacional de 7368 pacientes suecos con FA poscirugía cardíaca, seguidos durante 5 años, el inicio de ACO en los primeros 30 días no se asoció con un menor riesgo de ictus (2,0 % frente a 1,7 %), tromboembolia (2,6 % frente a 1,7 %) ni mortalidad (3,0 % frente a 2,8 %), pero sí aumentó el riesgo de hemorragia grave (2,4 % frente a 1,9 %) en comparación con la ausencia de ACO. Cabe destacar que solo la mitad de los pacientes continuaron con ACO después de 1 año, y menos del 40 % lo hicieron al finalizar el seguimiento. Además, un análisis emparejado por puntuación de propensión de 38.936 pacientes con FA posoperatoria de la base de datos de la Sociedad de Cirujanos Torácicos reveló que el tratamiento con ACO se asoció con una mayor mortalidad tanto al año (5,4 % frente al 4,2 %) como a los 5 años (21,1 % frente al 19,5 %) en comparación con la ausencia de ACO (HR: 1,16; IC del 95 %: 1,06-1,26), un hallazgo que se mantuvo constante en todos los estratos de la puntuación CHA 2 DS 2 -VASc. También se observó una tendencia hacia un mayor riesgo de tromboembolia a los 5 años en el grupo de ACO, aunque esta asociación no fue significativa. 163 En consonancia con la inconsistencia de los hallazgos, varios metanálisis, incluido un estudio publicado recientemente con casi 1,7 millones de pacientes, no han sido concluyentes.
Los estudios que evalúan la eficacia de los ACO en la FA asociada a factores estresantes tras cirugía no cardíaca han sido igualmente discordantes. En un estudio de registro nacional de 3830 pacientes con FA tras cirugía no cardíaca, comparado con 15 320 pacientes hospitalizados con FA primaria no valvular de nuevo diagnóstico, ambos grupos presentaron riesgos similares a largo plazo de tromboembolia (3,2 frente a 3,0 eventos por 100 años al año) y mortalidad (13,3 frente a 10,9 eventos por 100 años al año), con beneficios comparables de los ACO. De manera similar, en un estudio de 251.837 pacientes sometidos a cirugía no cardíaca, la FA asociada a factores de estrés se asoció fuertemente con ictus en comparación con la ausencia de FA (3,6 % frente a 2,3 %; RR: 1,60; IC del 95 %: 1,37-1,87), especialmente en pacientes que no recibían ACO (RR: 1,81; IC del 95 %: 1,44-2,28), pero esta asociación se atenuó en el subgrupo de pacientes con FA asociada a factores de estrés que recibían ACO (RR: 1,04; IC del 95 %: 0,71-1,51). Sin embargo, otros estudios y metaanálisis han sugerido, por el contrario, que la FA asociada a factores de estrés tras cirugía no cardíaca se asocia con un mayor riesgo de hemorragia y una mayor mortalidad.
Los efectos variables de los ACO observados en estudios de pacientes con FA postoperatoria pueden estar relacionados con diversos factores, como el sesgo de selección y la heterogeneidad de las poblaciones de pacientes, los factores de confusión (p. ej., el uso de ACO en individuos con mayor riesgo de resultados adversos), el uso de warfarina como principal forma de ACO (que ha demostrado ofrecer un menor beneficio en la prevención del ictus, con mayor riesgo de hemorragia, en comparación con los anticoagulantes no warfínicos en el contexto postoperatorio) y la escasez de datos sobre la continuidad y la adherencia al tratamiento tras el alta. En general, la frecuencia de ACO en el contexto postoperatorio parece baja, y considerablemente inferior a la observada en pacientes con FA no quirúrgica con puntuaciones CHA₂DS₂-VASc comparables (OR: 0,31; IC del 95 %: 0,19-0,52). Sin embargo, dadas las limitaciones de la literatura disponible, se recomienda el uso de índices de riesgo clínico (p. ej., CHA ≥ DS ≥ 2 -VASc, CHA ≥ DS ≥ 2 -VA, CHADS-65) para guiar la anticoagulación en la población posoperatoria (al igual que en otros contextos), haciendo hincapié en que la toma de decisiones debe individualizarse en función del riesgo de sangrado y las preferencias del paciente (Figuras 2 y 4). Además, a la luz de la creciente evidencia que respalda la recurrencia de la FA como un importante factor de riesgo para los eventos adversos relacionados con la FA, en particular la tromboembolia sistémica, la recurrencia debería motivar la reconsideración de la profilaxis del ictus en pacientes que no reciben ACO de forma similar a la FA primaria.
La eficacia demostrada de la oclusión de la orejuela auricular izquierda (OAI) para reducir el riesgo tromboembólico en pacientes con FA establecida ha generado un creciente interés en su uso profiláctico en personas sin FA conocida sometidas a cirugía cardíaca. En un análisis retrospectivo de emparejamiento por propensión de 2067 pacientes sometidos a cirugía cardíaca sin antecedentes de FA, la OAI se asoció con una menor incidencia de ictus posoperatorio entre quienes desarrollaron FA aguda. Sin embargo, la OAI también se relacionó con una tasa significativamente mayor de FA posoperatoria (0 de 145 eventos en el grupo con OAI frente a 7 de 115 en el grupo sin OAI; p < 0,05; OR para FA de nueva aparición: 1,36; IC del 95 %: 1,03-1,80). Si bien múltiples estudios retrospectivos a gran escala han corroborado la asociación entre la OAI y una mayor incidencia de FA posoperatoria (que se ha atribuido a una disminución aguda de la distensibilidad auricular izquierda y la consiguiente distensión), no han demostrado de forma consistente una reducción de los ictus ni de la mortalidad.
Varios ensayos aleatorios están en marcha para aclarar el papel de la ACO y el cierre profiláctico de la orejuela auricular izquierda en la FA asociada a factores estresantes de cirugía cardíaca y no cardíaca, incluidos: 1) PACES (Anticoagulación para fibrilación auricular posoperatoria de nueva aparición después de CABG; NCT04045665), que compara la eficacia de agregar ACO a la terapia antiplaquetaria de base en la FA asociada a factores estresantes después de la cirugía cardíaca; 2) LEAAPS (Exclusión de la orejuela auricular izquierda para el ensayo de reducción profiláctica del accidente cerebrovascular; NCT05478304) que aleatoriza a pacientes con mayor riesgo de FA incidente y accidente cerebrovascular para recibir ligadura profiláctica de la orejuela auricular izquierda o ninguna ligadura durante la cirugía cardíaca; y 3) ASPIRE-AF (Anticoagulación para la prevención de accidentes cerebrovasculares en pacientes con episodios recientes de FA perioperatoria después de cirugía no cardíaca; NCT03968393), que aleatoriza a pacientes sometidos a cirugía no cardíaca con FA posoperatoria y puntuaciones altas de CHA 2 DS 2 -VASc a ACO frente a ningún ACO.
Anticoagulación en FA asociada a factores de estrés no quirúrgicos
Si bien existe evidencia sólida que respalda el uso rutinario de ACO en la FA asociada a infarto de miocardio o tirotoxicosis, los datos retrospectivos sobre su uso en sepsis y en la población general con infección siguen siendo contradictorios (Figura 3). En la tirotoxicosis, las guías generalmente recomiendan el inicio de ACO según el riesgo estimado de ictus. Sin embargo, dada la evidencia que sugiere que el riesgo de ictus asociado a la FA asociada a tirotoxicosis puede estar subestimado por las puntuaciones de riesgo tradicionales, puede ser razonable considerar el uso de ACO en pacientes seleccionados con puntuaciones bajas en la escala CHA 2 DS 2 -VASc. En un estudio de 3992 pacientes con FA asociada a sepsis, de los cuales el 20 % obtuvo la prescripción de anticoagulantes en un plazo de 30 días, el uso de ACO se asoció con un mayor riesgo de ictus isquémico al año (5,7 % frente a 2,3 %; DR [diferencia de riesgo]: 3,37 %; IC del 95 %: 0,36-0,38). 280 Sin embargo, hay algunos datos que apoyan la anticoagulación en infecciones menos graves: en un estudio de registro a nivel nacional de 24.607 pacientes daneses con FA relacionada con infecciones, la anticoagulación se asoció fuertemente con una disminución del riesgo de tromboembolia.
Si bien existe evidencia sólida que respalda el uso rutinario de ACO en la FA asociada a infarto de miocardio o tirotoxicosis, los datos retrospectivos sobre su uso en sepsis y en la población general con infección siguen siendo contradictorios (Figura 3). En la tirotoxicosis, las guías generalmente recomiendan el inicio de ACO según el riesgo estimado de ictus. Sin embargo, dada la evidencia que sugiere que el riesgo de ictus asociado a la FA asociada a tirotoxicosis puede estar subestimado por las puntuaciones de riesgo tradicionales, puede ser razonable considerar el uso de ACO en pacientes seleccionados con puntuaciones bajas en la escala CHA 2 DS 2 -VASc. En un estudio de 3992 pacientes con FA asociada a sepsis, de los cuales el 20 % obtuvo la prescripción de anticoagulantes en un plazo de 30 días, el uso de ACO se asoció con un mayor riesgo de ictus isquémico al año (5,7 % frente a 2,3 %; DR [diferencia de riesgo]: 3,37 %; IC del 95 %: 0,36-0,38). 280 Sin embargo, existen algunos datos que respaldan la anticoagulación en infecciones menos graves: en un estudio de registro nacional de 24.607 pacientes daneses con FA relacionada con infecciones, la anticoagulación se asoció fuertemente con una disminución del riesgo de tromboembolia (HR: 0,75; IC del 95 %: 0,68-0,83) y muerte (HR: 0,53; IC del 95 %: 0,50-0,56), sin aumentar sustancialmente el sangrado (HR: 1,08; IC del 95 %: 0,98-1,18). 181 El estudio sugirió además que los pacientes con FA asociada a infecciones tienen tasas más altas de tromboembolia y muerte en comparación con la FA no relacionada con infecciones, independientemente del tratamiento con ACO. 181 A la luz de estos hallazgos, en concordancia con las directrices, la anticoagulación debe guiarse por la evaluación del riesgo individualizado de accidente cerebrovascular y sangrado, así como por la evidencia de recurrencia de la FA (Figuras 2 a 4).
Más allá del accidente cerebrovascular: la carga ignora de la insuficiencia cardíaca tras una FA asociada a factores de estrés
Aunque se ha demostrado una fuerte asociación entre la FA asociada a factores de estrés y el riesgo a largo plazo de insuficiencia cardíaca en estudios tanto retrospectivos como prospectivos, esta relación sigue siendo poco estudiada. La evidencia disponible sugiere que, al igual que en el caso de la FA primaria, la incidencia de insuficiencia cardíaca tras la FA asociada a factores de estrés puede superar a la del ictus, y algunos estudios indican una tasa dos veces mayor de eventos de insuficiencia cardíaca en comparación con el ictus. Si bien se han realizado importantes esfuerzos para cuantificar el riesgo de ictus y evaluar el papel de los ACO en la FA asociada a factores de estrés, se ha prestado relativamente poca atención a comprender la incidencia y el riesgo a corto plazo de insuficiencia cardíaca en relación con diversos factores de estrés, o a definir estrategias óptimas para la estratificación, la prevención y el manejo del riesgo de insuficiencia cardíaca en esta población.
Consideraciones de manejo en la fa asociada a factores de estrés
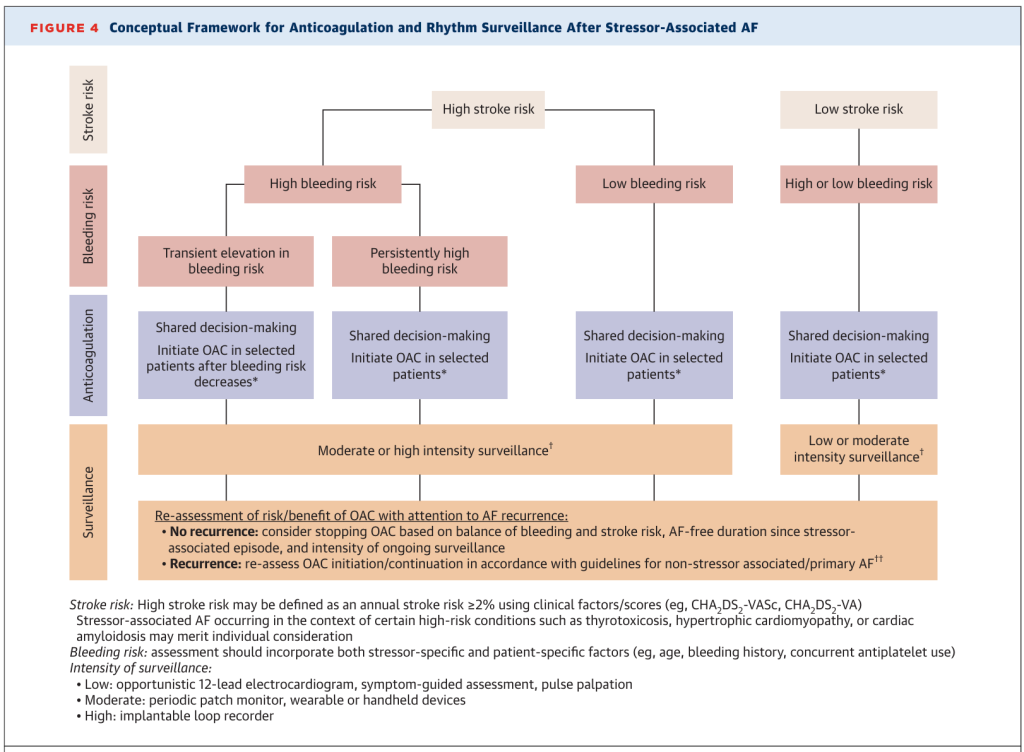
La evidencia actual es insuficiente para ofrecer recomendaciones específicas para la vigilancia y el tratamiento de la FA asociada a factores de estrés. Sin embargo, con base en la evidencia disponible y los principios generales de estratificación del riesgo, proporcionamos un marco conceptual para fundamentar la toma de decisiones clínicas en relación con la monitorización longitudinal y el manejo de la FA asociada a factores de estrés (Figura 4).
De acuerdo con las directrices internacionales, el riesgo de ictus debe estimarse mediante un marco validado (p. ej., CHA2DS2 -VASc, CHA2 DS2 -VA o CHADS-65), y los valores equivalentes a un riesgo anual de ictus del ≥2 % deben considerarse para el tratamiento antitrombótico. De igual manera, el riesgo de sangrado puede evaluarse individualmente, incorporando: 1) factores específicos del paciente, como la edad, los antecedentes de sangrado, el uso concomitante de antiagregantes plaquetarios, la función hepática y renal, y el uso concomitante de antiagregantes plaquetarios; y 2) cualquier consideración específica de los factores de estrés (p. ej., riesgo de sangrado posoperatorio, sepsis).
Las decisiones sobre el inicio de ACO deben tomarse en el contexto de una toma de decisiones compartida, basada en: 1) equilibrar el riesgo estimado de ictus y minimizar los riesgos de hemorragia (incluida la posible transitoriedad de un riesgo elevado de hemorragia); 2) las guías clínicas pertinentes; y 3) reconocer la incertidumbre que rodea tanto el uso de las puntuaciones de riesgo clínico estándar como la evidencia existente sobre ACO en la FA asociada a factores de estrés (Figura 4). Dada la naturaleza transitoria de algunos episodios de FA asociada a factores de estrés y la importancia crucial de la FA recurrente como indicador de riesgo de eventos adversos posteriores, la vigilancia es primordial. La intensidad de la vigilancia debe adaptarse al perfil individual de factores de riesgo de FA, ictus e insuficiencia cardíaca. Un mayor riesgo puede justificar estrategias de monitorización del ritmo más intensivas, que van desde monitores periódicos de ritmo hasta registradores de bucle implantables para facilitar la detección temprana de la recurrencia. En caso de recurrencia, se debe reevaluar el ACO de acuerdo con los enfoques establecidos para la FA primaria. Por el contrario, un período prolongado sin recurrencia de FA podría justificar una reevaluación de los beneficios del uso continuo de ACO, especialmente en pacientes con alto riesgo de sangrado. Aunque probablemente sea poco frecuente, reconocemos que los episodios recurrentes de FA asociados nuevamente a un factor estresante (ya sea debido a otro episodio del mismo factor estresante o a uno diferente) representan un área de particular incertidumbre.
Los riesgos basales de FA e insuficiencia cardíaca también pueden influir en el manejo longitudinal de las arritmias. Sin embargo, aún falta evidencia que demuestre el beneficio del control prolongado de la frecuencia o del ritmo para prevenir la recurrencia de la FA o reducir el riesgo de insuficiencia cardíaca u otros resultados adversos relacionados con la FA tras una FA asociada a factores de estrés.
Resultados informados por los pacientes
Cada vez se reconocen más los importantes efectos de la FA en los resultados informados por el paciente (REP), que abarcan evaluaciones cuantitativas de los síntomas, el estado funcional y la calidad de vida. Si bien la evidencia preliminar sugiere que la FA asociada a factores estresantes puede afectar negativamente a los REP, estos resultados siguen estando mal caracterizados, en particular dada la alta carga de enfermedades comórbidas en las personas afectadas por FA asociada a factores estresantes (incluido el propio factor estresante agudo). Una comprensión más completa de cómo la FA asociada a factores estresantes afecta la capacidad funcional y el bienestar mental es importante por varias razones. En primer lugar, los datos de poblaciones de cirugía cardíaca sugieren que, incluso cuando las características basales son similares con respecto a la carga de enfermedades comórbidas, las personas que desarrollan FA asociada a factores estresantes experimentan reducciones marcadas en la función física y social y refieren mayor dolor posoperatorio que quienes no presentan FA. Estos hallazgos respaldan el valor potencial de la rehabilitación individualizada y las estrategias de manejo de los síntomas tras el alta. En segundo lugar, la evidencia derivada del tratamiento de la FA primaria ilustra la utilidad clínica de los REP para fundamentar las decisiones terapéuticas, como se refleja en la evidencia consistente que respalda la ablación con catéter como la estrategia preferida para el control del ritmo cardíaco con respecto al estado funcional y la calidad de vida. Basándose en estos conocimientos, los estudios futuros, como los que evalúan la vigilancia y el control del ritmo longitudinal después de la FA asociada a factores estresantes, deberían incorporar formalmente los PRO junto con los criterios de valoración clínicos para identificar estrategias preventivas y terapéuticas que mejoren la salud, el estado funcional y el bienestar psicológico.
Resumen de las orientaciones futuras
En las últimas décadas, una extensa investigación ha elevado la FA asociada a factores de estrés, pasando de ser una afección de mínimo interés clínico a un foco importante de la atención cardiovascular moderna. Si bien hemos adquirido diversos conocimientos sobre los factores de estrés comunes, sus probables mecanismos fisiopatológicos, sus implicaciones clínicas y las estrategias óptimas de manejo para ciertas formas de FA asociada a factores de estrés, aún quedan varias áreas críticas de investigación futura. A lo largo de esta revisión narrativa, hemos identificado lagunas de conocimiento clave y destacamos sucintamente las siguientes necesidades críticas no satisfechas:
1. Desarrollo de una prevención más eficaz: La FA asociada a factores de estrés en el contexto posquirúrgico cardíaco ha proporcionado un modelo para traducir los conocimientos fisiopatológicos en intervenciones clínicas eficaces (p. ej., pericardiotomía posterior para prevenir episodios de FA asociada a factores de estrés). Nuestro conocimiento de las estrategias para prevenir la FA asociada a factores de estrés y gestionarla óptimamente cuando se produce es, en comparación, deficiente en otros entornos. Identificar a los pacientes con alto riesgo de FA asociada a factores de estrés en cirugía no cardíaca y en entornos médicos puede facilitar un mayor descubrimiento y orientar el uso de la profilaxis basada en la evidencia.
2. Desarrollo de métodos de precisión para la vigilancia y el tratamiento longitudinales: Mejores métodos para estratificar el riesgo individual de recurrencia de FA y eventos adversos relacionados con la FA tras un episodio de FA asociado a un factor estresante son esenciales para priorizar a las personas en el uso de tecnologías de monitorización más precisas y que requieren muchos recursos (p. ej., registradores de bucle implantables). Además, estos métodos podrían orientar las intervenciones preventivas centradas en la reducción de la insuficiencia cardíaca relacionada con la FA (que aún se desconoce, pero que puede incluir el control precoz del ritmo o incluso ciertas terapias médicas basadas en las guías) y el ictus (p. ej., anticoagulantes ortopédicos empíricos o cierre de la orejuela auricular izquierda). Una mejor comprensión de la evolución natural de la FA asociada a factores estresantes y la posible interacción entre la carga de FA y los resultados adversos podría mejorar aún más el pronóstico y sentar las bases para una toma de decisiones compartida que incorpore los riesgos y beneficios a nivel de paciente. Dadas las limitaciones establecidas en la utilidad predictiva de los factores clínicos, el análisis basado en IA y otros biomarcadores novedosos (p. ej., imágenes, puntuaciones genéticas) pueden representar una vía prometedora. Se requiere mayor trabajo, incluyendo el desarrollo colaborativo de conjuntos de datos exhaustivos que incluyan a pacientes con diversidad étnica, racial, socioeconómica y geográfica, para avanzar en los esfuerzos futuros por lograr un manejo preciso de la FA asociada a factores de estrés. La armonización de las definiciones de FA asociada a factores de estrés (p. ej., estableciendo criterios diagnósticos consensuados y posiblemente introduciendo códigos de facturación únicos) podría facilitar sustancialmente la investigación, reducir la heterogeneidad de los estudios y mejorar la replicabilidad de los hallazgos.
3. Utilizando un enfoque orientado al paciente: La integración de resultados centrados en el paciente y enfoques socialmente informados en el manejo de la FA asociada a factores estresantes puede aliviar la carga sintomática y abordar la ansiedad y la depresión comórbidas. Se necesitan más investigaciones sobre el papel crucial de los determinantes sociales en la aparición de la FA asociada a factores estresantes, los resultados a corto y largo plazo, y el manejo longitudinal para promover una atención equitativa de alta calidad para todos los pacientes con FA asociada a factores estresantes.
Conclusiones
Considerada en el pasado un fenómeno transitorio y benigno, la creciente evidencia destaca que la FA asociada a factores de estrés conlleva un riesgo sustancial de recurrencia de la FA y eventos adversos relacionados, comparable al de la FA primaria. Los avances en la comprensión de la epidemiología, los factores de riesgo y la fisiopatología de la FA asociada a factores de estrés han perfeccionado los enfoques de prevención y tratamiento, especialmente en el contexto posquirúrgico cardíaco. La FA asociada a factores de estrés probablemente representa un espectro que abarca contribuciones relativas variables del factor estresante y la predisposición subyacente, y la ubicación en el espectro representa un marco útil para conceptualizar el riesgo de recurrencia de la FA y los eventos adversos relacionados. Sin embargo, persisten numerosas lagunas de conocimiento clave, como la necesidad de mejores métodos de estratificación del riesgo, estrategias más precisas para la monitorización de la recurrencia y enfoques basados en la evidencia para la prevención, el tratamiento longitudinal de las arritmias y la profilaxis del ictus y la insuficiencia cardíaca. Aunque los factores clínicos tienen una utilidad limitada para el pronóstico, los métodos emergentes basados en IA y otros biomarcadores novedosos (p. ej., análisis de laboratorio, imágenes, riesgo basado en ómicas) representan vías prometedoras para la evaluación y el manejo individualizado del riesgo. La incorporación de PRO en la atención rutinaria tras la FA asociada a factores de estrés puede mejorar la calidad de vida y la salud cardiovascular a largo plazo. La investigación futura debería centrarse en perfeccionar las herramientas de predicción del riesgo, investigar rigurosamente las estrategias de manejo individualizado e integrar enfoques centrados en el paciente para optimizar los resultados tras la FA asociada a factores de estrés.