Rendimiento cardíaco
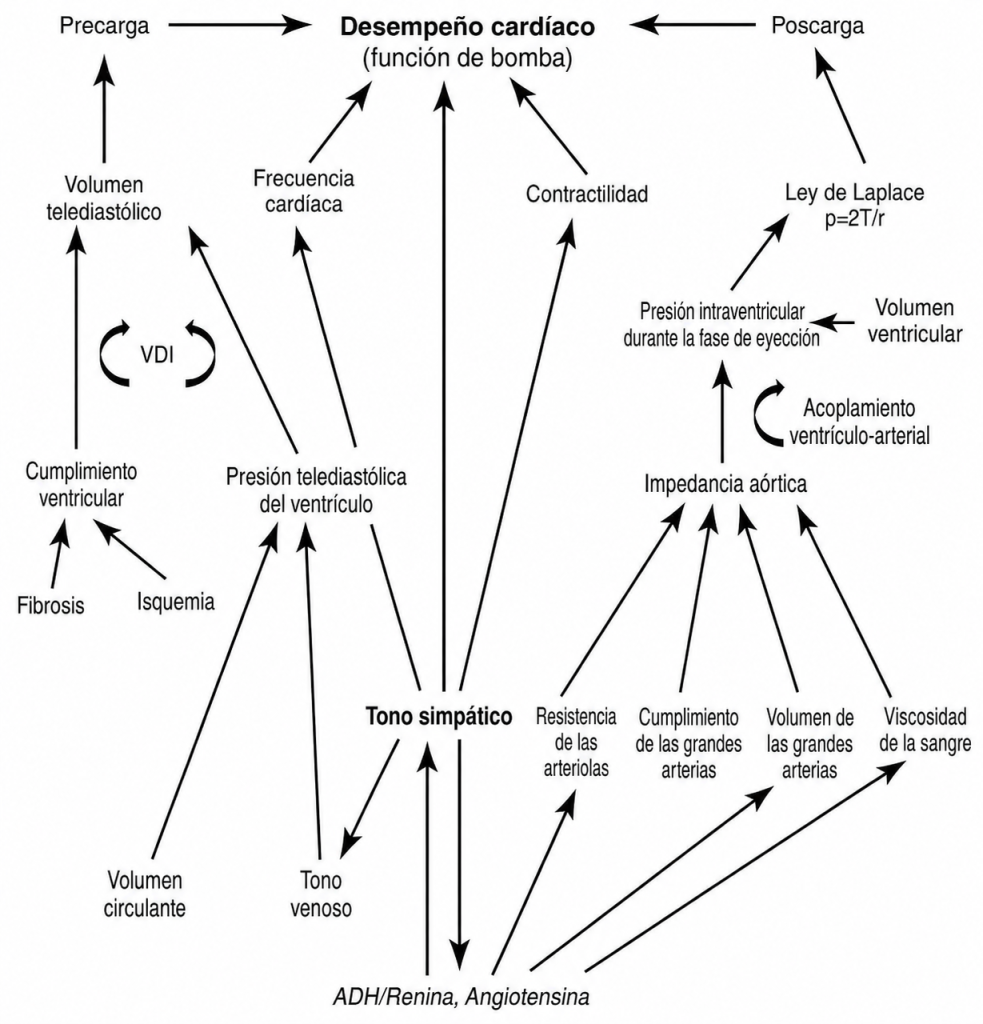
El rendimiento cardíaco depende de una amplia variedad de factores, entre los que destacan la precarga, la poscarga, la frecuencia cardíaca y la contractilidad (Fig. 1). Sin embargo, otros factores desempeñan un papel importante, aunque son menos conocidos. La interacción ventricular diastólica (IVD) y su impacto en la precarga, el trabajo sistólico reclutable por la precarga, el acoplamiento ventrículo-arterial y otras propiedades vasculares y ventriculares, a través de su interacción al final de la sístole, influyen significativamente en el rendimiento cardíaco.
La ecuación fundamental de la circulación
TAM = GC x RVS (Presión = Flujo x Resistencia)
La ecuación fundamental del sistema circulatorio expresa la función básica del corazón: generar flujo y presión para asegurar una perfusión adecuada del organismo.
La resistencia periférica sistémica, difícil de determinar directamente en la práctica, puede calcularse utilizando los parámetros medibles de la presión arterial media (PAM) y el gasto cardíaco (GC). Sin embargo, la resistencia vascular sistémica (RVS) no está determinada por estos parámetros; la RVS y el GC son independientes, mientras que la PAM es la variable dependiente.
La ley de Poiseuille propone tres maneras de modificar la presión arterial:
✅Modificar el flujo,
✅Modificar la resistencia,
✅Modificar ambos.
Por lo tanto, un aumento del flujo sanguíneo y/o un aumento de la relación resistencia/flujo sanguíneo (RVS/GC) pueden modificar la PAM [8]. Si el GC y la RVS cambian de forma recíproca y proporcional, solo entonces la PAM permanecerá inalterada. Si el GC aumenta, pero con una reducción de la RVS debido a la vasodilatación periférica, la PAM aumentará si el aumento del GC es proporcionalmente mayor que la reducción de la RVS. En el caso de la sobrecarga de volumen, el aumento del gasto cardíaco (GC) conlleva un aumento de la presión arterial media (PAM) si la resistencia vascular sistémica (RVS) permanece inalterada.
Kumar demostró que la sobrecarga de volumen en corazones sanos aumenta la contractilidad, el trabajo sistólico, la presión arterial sistólica y la PAM. Sin embargo, en corazones con contractilidad comprometida, la presión arterial podría no aumentar. Michard demostró que el aumento del volumen sistólico (VS) (flujo) depende críticamente de la capacidad contráctil del corazón. Por lo tanto, si la sobrecarga de volumen no produce un aumento del VS, se debe sospechar una insuficiencia cardíaca significativa. Además, cabe recordar que, en los síndromes de insuficiencia cardíaca, la poscarga del ventrículo izquierdo (VI) es el determinante decisivo del rendimiento cardíaco. Por consiguiente, la reducción de la poscarga mediante vasodilatadores es el tratamiento de elección.
Por lo general, en la práctica clínica diaria en la insuficiencia cardíaca aguda, al disminuir la resistencia periférica, se reduce la tensión parietal telesistólica del VI y aumenta el VS, pero la PAM se mantiene o incluso aumenta. Si, en estas condiciones, la presión arterial media (PAM) no aumenta o al menos no se mantiene, deben considerarse las siguientes circunstancias:
✅Insuficiencia mitral grave,
✅Llenado inadecuado del ventrículo izquierdo (VI) debido a disfunción ventricular izquierda (DVI),
✅Desajuste entre el acoplamiento ventrículo-arterial,
✅Volumen intravascular insuficiente (hipovolemia relativa) (rara vez).
Precarga
Definición
La precarga, según la definición de Braunwald y Ross, es «la fuerza que actúa para estirar las fibras musculares del ventrículo izquierdo al final de la diástole y que determina la longitud de reposo de los sarcómeros».
El retorno venoso llena el ventrículo, ejerciendo fuerza sobre el músculo cardíaco, estirando las miofibrillas y siendo uno de los principales determinantes del rendimiento cardíaco.
El volumen ventricular telediastólico, o precarga, se refleja fielmente en la tensión de la pared telediastólica (precarga ≈ tensión de la pared telediastólica).
El mecanismo de Frank-Starling
La presión telediastólica transmural del ventrículo izquierdo (LVEDP) refleja con precisión la presión de distensión efectiva responsable de la longitud de las fibras miocárdicas.
Otto Frank y Ernest Starling obtuvieron una relación entre la longitud de la fibra al final de la diástole y la fuerza de contracción:
Al aumentar la longitud de la fibra, aumenta la fuerza de contracción y, por lo tanto, aumenta el volumen sistólico (VS) del ventrículo izquierdo (VI) o del ventrículo derecho (VD), o, más precisamente, aumenta el trabajo sistólico (TS):
Trabajo Sistólico del Ventrículo Izquierdo (TSVI) = Volumen Sistólico (VS) x (Presión Telesistólica del Ventrículo Izquierdo (PTVI) – Presión Telediastólica del Ventrículo Izquierdo (PTDVI))
El llenado diastólico ventricular está limitado por el pericardio, que es prácticamente indistensible y restringe el llenado de los ventrículos, y por el citoesqueleto, lo que previene la sobrecarga de líquido en los ventrículos (mecanismo de protección fisiológica) y la dilatación patológica.
Con el aumento de la longitud de las fibras en reposo, también aumenta la velocidad de acortamiento muscular de las fibras.
Frank estableció una relación lineal entre el volumen telediastólico del ventrículo izquierdo (VTDVI) como correlato de la longitud de las fibras y la fuerza de contracción ventricular.
Trabajo Sistólico del Ventrículo Izquierdo (TSVI) se correlaciona de manera adecuada con el Volumen Telediastólico del Ventrículo Izquierdo (VTDVI): Volumen Sistólico (VS) ≈ Volumen Telediastólico del Ventrículo Izquierdo (VTDVI)
Starling informó de un aumento en la fuerza de contracción con el incremento de las presiones auriculares. El resultado de Starling es similar al descrito por Frank, siempre que el aumento de la presión telediastólica del ventrículo izquierdo (PTDVI) represente un aumento proporcional del volumen telediastólico del ventrículo izquierdo (VTDVI) (relación lineal entre la PTDVI y el VTDVI). Esto se cumple en la mayoría de las personas sanas, siempre que la PTDVI se mantenga dentro de los rangos normales; sin embargo, en el caso de presiones de llenado ventricular izquierda elevadas y en ciertas circunstancias patológicas, el aumento de la PTDVI suele ser desproporcionadamente alto en comparación con el aumento del VTDVI.
La PTDVI puede incluso aumentar sin que se produzca un incremento en el volumen de llenado ventricular izquierdo, lo que no genera un aumento de la precarga, esencial para reclutar un mayor volumen sistólico (VS). Por lo tanto, aunque la PTDVI aumente, puede que no haya un incremento adecuado del VS; de hecho, incluso puede haber una disminución que corresponda con la «rama descendente» de la curva de Starling. Esta rama descendente descrita por Starling es, sin embargo, un artefacto de sus condiciones experimentales.
Al utilizar la presión de distensión efectiva en lugar de la presión intracavitaria, la relación entre el estiramiento de las fibras y la fuerza de contracción se describe adecuadamente y coincide con los hallazgos de Frank y la siguiente afirmación:
La presión de distensión efectiva o presión telediastólica del ventrículo izquierdo (PTDVI) transmural es la PTDVI intracavitaria (comúnmente denominada simplemente PTDVI) menos la(s) presión(es) circundante(s).
Katz, en 1965, ya asumía que las presiones telediastólicas intracavitaria y transmural del ventrículo izquierdo solo eran iguales cuando la presión que rodeaba el músculo cardíaco del ventrículo izquierdo era despreciable. De lo contrario, la presión externa debe restarse de la PTDVI intracavitaria para calcular la presión de distensión efectiva o transmural.
Presión transmural PTDVI = PTDVI−Presión circundante
Generalmente, la presión circundante se compone en un tercio por la presión telediastólica del ventrículo derecho (PTDVD) y en dos tercios por la presión pericárdica:
PTDVD transmural = PTDVD intracavitaria − (2/3 presión pericárdica + 1/3 PTDVD). En condiciones normales, la presión auricular derecha (PAD) y la presión pericárdica (PP) son prácticamente iguales, y los cambios en la presión pericárdica se reflejan fielmente en los cambios de la presión auricular derecha (PAD).
La estrecha relación entre los cambios en la presión auricular derecha y las presiones pericárdicas permite obtener una estimación razonable de la presión transmural restando la PAD de la presión de enclavamiento capilar pulmonar (PECP):
Presión Diastólica Final del Ventrículo Izquierdo (PDFVI) Transmural = Presión Capilar Pulmonar (o Presión de Enclavamiento) (PCP) – Presión de la Aurícula Derecha (PAD) ≈ Presión Capilar Pulmonar (o Presión de Enclavamiento) (PCP) – Presión Venosa Central (PVC)
La PVC refleja la presión circundante.
Existe evidencia sustancial de que la PCP refleja la LVEDP. La PVC se mide en la confluencia de la vena cava con la aurícula derecha y, por lo tanto, es igual a la PAD. Debido a la estrecha relación entre la PAD y la PP (r = 0,95, p < 0,005), y entre la PAD y los cambios en la PP, respectivamente, la PVC es una buena estimación de la PP en la práctica clínica diaria. Además, tanto la PVC como la PAD reflejan la RVEDP. En un amplio rango, la presión pericárdica, la PAD y la RVEDP son prácticamente iguales. Tyberg demostró que la RVEDP representa bien la PP en rangos entre 4 y 20 mmHg. Sin embargo, en casos de hipertrofia ventricular derecha, cuando el ventrículo derecho está rígido, y en casos de cor pulmonale o hipertensión pulmonar, la PAD y la RVEDP son mucho mayores que la PP. La insuficiencia ventricular derecha siempre provoca un aumento de la PVC.
En personas sanas, la presión ambiente es baja (casi nula) y un aumento de la precarga incrementará la presión telediastólica del ventrículo izquierdo (PTDVI) más que la presión ambiente. Por lo tanto, la PTDVI transmural aumentará junto con el volumen telediastólico del ventrículo izquierdo (VTDVI), incrementando el volumen sistólico reclutable por precarga (trabajo) y, por consiguiente, el volumen sistólico (VS), como describieron Frank y Starling.
En condiciones donde la presión ambiente aumenta sustancialmente, la restricción externa aumenta más que la PTDVI. La PTDVI transmural y la PTDVI intracavitaria diferirán considerablemente y cambiarán en direcciones opuestas con una disminución de la PTDVI transmural, reduciendo la precarga y, en consecuencia, el volumen sistólico reclutable por precarga (trabajo) disminuirá.
Las presiones intraventriculares (PTTDVI intracavitaria y PTDVI ventricular derecha) están influenciadas por:
✅La distensibilidad del ventrículo izquierdo,
✅Alteraciones en la anatomía y fisiología pulmonar que inducen cambios en la presión intratorácica y las presiones en la circulación pulmonar,
✅La presión intraabdominal.
La distensibilidad del ventrículo izquierdo (VI) describe las propiedades diastólicas del músculo cardíaco y se puede representar mediante la relación entre la presión telediastólica del ventrículo izquierdo (PTDVI) y el volumen telediastólico del ventrículo izquierdo (VTDVI).
Teniendo esto en cuenta, las discrepancias entre la PTDVI transmural y la PTDVI intracavitaria pueden estar relacionadas, al menos en parte, con la distensibilidad ventricular.
La distensibilidad ventricular varía casi continuamente en pacientes críticos, produciendo cambios en la PTDVI intracavitaria, pero sin un cambio correspondiente en el VTDVI. Sin embargo, Kumar aportó evidencia de que el cambio continuo en la distensibilidad ventricular es un fenómeno fisiológico presente tanto en personas sanas como en pacientes con enfermedades cardíacas.
En la insuficiencia cardíaca, la distensibilidad del VI casi siempre está reducida; por lo tanto, los aumentos en los volúmenes de llenado provocan un mayor incremento de la PTDVI en comparación con un corazón sano.
La distensibilidad está determinada por factores como la masa muscular, la composición tisular, las propiedades elásticas, las interacciones ventriculares y las condiciones extramiocárdicas, incluyendo la estructura pericárdica y las propiedades intratorácicas.
El aumento de la presión intratorácica debido a neumonía, síndrome de dificultad respiratoria aguda (SDRA), edema pulmonar, etc., así como el aumento de la presión intraabdominal, incrementarán la restricción, en particular sobre el ventrículo derecho (VD), cuyas paredes son delgadas, afectando más a la presión telediastólica del ventrículo derecho (PTDVD) y la presión pericardica (PP) que a la presión telediastólica del ventrículo izquierdo (PTDVI).
Además, cuanto mayor sea la PTDVI, mayor será la fuerza externa que actúa sobre el ventrículo izquierdo (VI), lo que dificulta su llenado, la precarga y el volumen sistólico (VS) reclutable por precarga.
Ejemplos de situaciones que alteran las presiones circundantes o producen una restricción pericárdica externa significativa son:
✅Aumento del agua pulmonar debido a insuficiencia cardíaca congestiva,
✅Ventilación mecánica y PEEP: Ambas inducen un aumento de la presión intratorácica (presión circundante) y de la poscarga del VD. La PTDVD y la PP, normalmente bajas, aumentarán notablemente en caso de ventilación mecánica con presión positiva y/o aplicación de PEEP, neumonía, SDRA, etc., contribuyendo así esencialmente a un aumento de la presión circundante.
✅En pacientes con insuficiencia cardíaca, se espera una marcada restricción externa en la mayoría de los casos, que compromete el llenado ventricular izquierdo y se vuelve significativa si la presión telediastólica del ventrículo izquierdo (PTDVI) > 10¹²–15 mmHg. La restricción externa fisiológica, debida principalmente a la presión pericardica (PP), contribuye hasta en un 30-40% a la PTDVI. En la insuficiencia cardíaca, la contribución de la restricción externa a la PTDVI alcanza entre un 50% y un 80%.
✅Embolia pulmonar aguda: ↑ PTDVI (Presión Telesistólica/Diastólica Final del Ventrículo Izquierdo) y, por lo tanto, ↑ PP (Presion Pericardica), lo que provoca un aumento de la presión circundante que no produce cambios o incluso disminuye la PTDVI transmural.
En caso de restricción externa, la presión telediastólica del ventrículo izquierdo (PTDVI) sobreestima notablemente la presión de distensión efectiva.
Los cambios en direcciones opuestas (PTDVI transmural ↓ y PTDVI intracavitaria ↑) ahora se explican, y solo un aumento de la PTDVI transmural es consistente con un aumento del volumen telediastólico del ventrículo izquierdo (VTDVI) y viceversa.
Numerosas publicaciones han demostrado que la monitorización hemodinámica mediante cateterismo de la arteria pulmonar, que mide las presiones intracavitarias (de llenado), no es una guía precisa de la precarga, ya que las presiones de llenado no reflejan adecuadamente la longitud de las fibras miocárdicas al final de la diástole y, por lo tanto, el VTDVI. Si se utiliza la presión transmural, los cambios en la precarga se reflejan con precisión.
Sin embargo, las presiones de llenado siguen siendo uno de los componentes más importantes en la evaluación y la toma de decisiones terapéuticas en la insuficiencia cardíaca. El corazón siempre intenta generar un gasto cardíaco adecuado con la PTDVI más baja posible. En pacientes con insuficiencia cardíaca, una reducción terapéutica de la PTDVI se correlaciona con una mejoría en el pronóstico. Por lo tanto, la descarga del ventrículo izquierdo y la reducción de la presión telediastólica del ventrículo izquierdo (PTDVI) constituyen la máxima terapéutica que se ajusta a la fisiología y fisiopatología de la situación y mejora el pronóstico. Así, podríamos obtener mejores resultados en nuestros pacientes con insuficiencia cardíaca grave y shock cardiogénico utilizando la PTDVI transmural para la toma de decisiones terapéuticas.
Por supuesto, existe un óptimo fisiológico y un máximo de distensión de las fibras y el consiguiente desarrollo de fuerza (véase la figura 2).
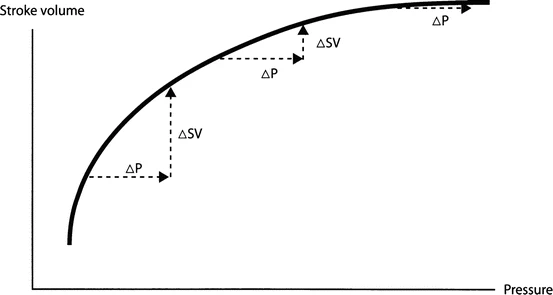
Además, en caso de insuficiencia cardíaca (aguda), el mecanismo de Frank-Starling se ve notablemente disminuido y, por lo tanto, en el corazón con insuficiencia cardíaca, un aumento en la distensión de las fibras (llenado ventricular) no se acompaña del mismo aumento en la fuerza de contracción que en personas sanas.
En el corazón con insuficiencia cardíaca, el volumen sistólico depende sustancialmente de la contractilidad y la poscarga.
Retorno venoso y PVC en la práctica diaria
El volumen sistólico (VS) está determinado por el retorno venoso (responsable de la precarga) y el rendimiento cardíaco (contractilidad, poscarga y frecuencia cardíaca).
Guyton et al. evaluaron la relación entre la función cardíaca total (contractilidad y resistencia periférica total) y el retorno venoso:
“El gasto cardíaco real varía con los cambios en la función cardíaca (FC), pero también con los cambios en el retorno venoso”.
De hecho, dado que el aumento del llenado ventricular y, por lo tanto, la distensión ventricular, conlleva un aumento del VS, este último es básicamente una función del volumen de llenado telediastólico y, como tal (hasta un límite superior: longitud del sarcómero de 2,2 μm), en algunos aspectos de la cantidad de retorno venoso.
Guyton representó gráficamente las relaciones (función cardíaca total y retorno venoso) en un solo gráfico (véase la figura 3).
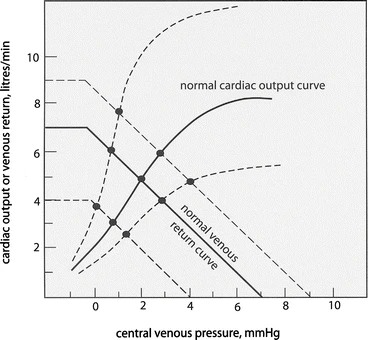
En la mayoría de las condiciones fisiológicas, los cambios en estas relaciones ocurren simultáneamente, aunque un efecto predominará. Por ejemplo:
✅Si el gasto cardíaco (GC) aumenta con una disminución de la presión auricular derecha (presión venosa central), el efecto dominante es una mejora de la función cardíaca (aumento de la contractilidad y/o reducción de la poscarga).
✅Si el GC aumenta con un incremento de la presión auricular derecha (PAD), el efecto dominante es un aumento del volumen y una disminución de la distensibilidad o capacidad venosa, lo que resulta en un mayor flujo venoso para cualquier presión en la aurícula derecha.
Por lo tanto, al interpretar las condiciones hemodinámicas, es fundamental considerar la interrelación entre la PVC y el GC: tanto la PVC como el GC están determinados por la interacción de dos funciones: la función cardíaca y el retorno venoso. La relación PAD/PVC no es un determinante independiente del GC, sino que depende de él tanto como lo determina. En consecuencia, la PVC puede ser baja en una persona con bajo volumen sanguíneo y función cardíaca normal, pero también puede ser baja en casos de volumen normal y buena función cardíaca. La PVC puede ser alta en casos de llenado normal con función cardíaca alterada, pero también en casos de función normal con sobrecarga de líquidos.
El retorno venoso depende de la presión media de llenado sistémico, la presión auricular derecha y la resistencia vascular, en particular del tono venoso. Un aumento del tono venoso precipita un incremento del retorno venoso. La diferencia de presión entre la presión periférica (presión de llenado sistémico, representada principalmente por la presión de las venas extratorácicas) y la presión dentro de la aurícula derecha (presión venosa central) suele ser de 7 a 10 mmHg, con una diferencia de presión auricular derecha (PAD) de 0 mmHg, lo que determina el retorno venoso. La respiración espontánea, al generar presiones intratorácicas negativas, aumenta este gradiente de presión, facilitando el retorno venoso. Por otro lado, los aumentos de la PAD, y en particular las PAD elevadas, dificultan el retorno venoso.
Dado que el nivel de presión auricular derecha se ve afectado decisivamente por afecciones intratorácicas extracardíacas, cualquier aumento de la presión pericárdica (que muestra restricción pericárdica, como en casos de derrame pericárdico o taponamiento cardíaco, ventilación con presión positiva y derrames pleurales por interacción cardiopulmonar) incrementará la PAD. Este aumento de la PAD no se acompaña de un incremento en el volumen de llenado, pero sí dificulta aún más el retorno venoso. El aumento de la poscarga ventricular y la isquemia miocárdica que afectan las propiedades diastólicas del miocardio (disminuyendo la distensibilidad miocárdica) alteran posteriormente las presiones de llenado ventricular y, por lo tanto, la presión auricular derecha (PAD) (o la presión auricular izquierda, respectivamente). En consecuencia, no existe relación entre la PAD y el volumen sistólico (VS) cuando las presiones extracardíacas e intratorácicas están elevadas.
Por lo tanto, el nivel de la presión auricular derecha está determinado por la presión con la que la sangre distiende la aurícula y por los efectos de presión de las estructuras adyacentes pericárdicas, torácicas y pulmonares.
En cualquier caso, una PVC elevada puede estar relacionada con (a) alteraciones extracardíacas/intratorácicas, o (b) indicar disfunción del ventrículo derecho (VD) y/o obstrucción del tracto de salida del VD (es decir, hipertensión pulmonar) con reflujo de sangre hacia la aurícula derecha, o reflejar (c) ambas causas. En cualquier caso, es necesario considerar el diagnóstico diferencial, ya que las diferentes causas implican inevitablemente diferentes medidas terapéuticas.
Mientras que en el sistema arterial la presión depende del flujo y la resistencia arterial (PAM = VS × RVS) y está determinada por ellos, el flujo sanguíneo venoso está determinado considerando el volumen y la capacitancia venosa:
La capacitancia venosa es el factor dominante en el comportamiento venoso, y la presión venosa central está determinada, esencialmente, por la capacidad venosa. No es el retorno venoso (como flujo), sino el volumen, lo que controla predominantemente la presión auricular derecha (PAD) y la presión venosa central (PVC).
Durante el ejercicio, la actividad simpática, estimulada por la disminución de la actividad de los receptores arteriales y auriculares, aumenta el tono venoso y disminuye la capacitancia venosa. Esto incrementa el retorno venoso al corazón y, en caso de existir una reserva de precarga reclutable (que depende del factor de carga), el volumen sistólico (VS) aumenta. El efecto inmediato de una disminución de la capacitancia venosa es un aumento de todas las presiones, incluyendo la presión telediastólica del ventrículo derecho (PTDVD) transmural y, por lo tanto, el llenado del ventrículo derecho, lo que permite que este aumente su rendimiento sistólico.
La infusión de líquidos produce un aumento de la capacitancia venosa, disminuyendo la presión venosa central. Una PVC elevada siempre tiene consecuencias y limita el retorno venoso.
En pacientes con shock séptico, Stephan observó que, a pesar de la vasodilatación de los sistemas arterial y venoso, la sobrecarga de volumen aumentaba significativamente el tono venoso y, por consiguiente, la PVC, elevándola a valores altos (>10 mmHg). Esto se debe a una marcada reducción de la distensibilidad del sistema venoso, secundaria al endurecimiento de las paredes venosas por diversos mecanismos inducidos por la sepsis. Además, los aumentos drásticos de la PVC indican que la capacidad de acomodación en caso de que el retorno venoso haya alcanzado su límite y que la sangre se esté acumulando.
La PVC normalmente es de 0 mmHg en reposo y puede aumentar a 2-4 mmHg durante el ejercicio. La PVC solo se eleva en estados patológicos; una PVC > 10 mmHg suele reflejar una poscarga del ventrículo derecho elevada.
Tanto en pacientes críticos como en personas sanas, se sabe que no existe correlación alguna entre la PVC y la precarga, ni entre los cambios en la PVC y los cambios en la precarga. La falta de correlación se debe a que, en humanos, la distensibilidad de las aurículas y, en particular, de los ventrículos, es muy variable. Además, la precarga no es lo mismo que la respuesta a la administración de líquidos, y la PVC y sus variaciones predicen de forma deficiente (o nula) dicha respuesta.
Por lo tanto, en la práctica clínica diaria, el valor absoluto de la PVC, e incluso sus variaciones dinámicas, son muy difíciles de interpretar y no pueden utilizarse como un indicador válido para el manejo de líquidos.
En general, una PVC ≥ 10-12 mmHg debe considerarse elevada, y la mayoría de los pacientes dentro de este rango no responderán a la administración de volumen. Bafaqueeh observó que el 40 % de los pacientes con una PVC < 6 mmHg no respondieron a la administración adicional de líquidos.
La restricción pericárdica representa el 96 % de la presión auricular derecha (PAD) si la PVC > 10 mmHg: Una PVC ≥ 5 mmHg, y en particular cuando supera los 9-10 mmHg, ejercerá una restricción sustancial sobre el llenado ventricular (izquierdo).
Por lo tanto, una PVC elevada > 9-10 mmHg siempre es patológica, lo que indica que es improbable que la administración de líquidos sea eficaz y que puede existir o producirse una interacción ventricular diastólica (IVD) si la PVC aumenta aún más.
Monitorización hemodinámica
Evaluación y monitorización del estado de los fluidos
La monitorización hemodinámica es fundamental en el manejo de pacientes críticos. Ayuda a identificar estados patológicos y complicaciones de la insuficiencia circulatoria, y facilita el restablecimiento de los parámetros hemodinámicos normales para prevenir lesiones tisulares y orgánicas, corregir la insuficiencia o disfunción orgánica y, por lo tanto, reducir la mortalidad.
Ante una circulación comprometida, la expansión de volumen suele ser la primera medida terapéutica para mejorar el estado hemodinámico. Desafortunadamente, solo entre el 40 % y el 70 % de los pacientes con insuficiencia circulatoria aguda responden a la administración de líquidos (aumento del volumen sistólico/gasto cardíaco), lo que significa que entre el 30 % y el 60 % de los pacientes no responden a la administración de líquidos y esta puede ser perjudicial. Tanto la insuficiencia cardíaca derecha aguda como la crónica, así como la insuficiencia cardíaca izquierda aguda, pueden empeorar con la sobrecarga de volumen.
Por lo tanto, se requiere un enfoque racional para la administración de líquidos, donde la decisión terapéutica se base en una evaluación correcta del volumen intravascular efectivo (precarga) y la respuesta probable al aumento de volumen. Sin embargo, las herramientas clínicas disponibles para evaluar el estado de hidratación del paciente y, específicamente, el llenado intravascular/intraventricular (precarga), como la distensión venosa yugular, los crepitantes a la auscultación, el edema periférico, etc., tienen un valor mínimo y son indicadores muy deficientes del estado de volumen, sobre todo en el paciente crítico con shock (cardiogénico). No pueden validarse como una herramienta útil ni como base para la toma de decisiones terapéuticas. El único signo clínico relevante que, aunque inespecífico, puede indicar un posible déficit de volumen es la frecuencia cardíaca. Los déficits de volumen suelen compensarse con un aumento de la frecuencia cardíaca (>90 lpm) para mantener el gasto cardíaco en caso de bajo volumen sistólico.
En pacientes con insuficiencia cardíaca aguda, una evaluación rápida a pie de cama de dos minutos resulta extremadamente útil para asignar al paciente a un perfil hemodinámico específico (húmedo o seco y frío o caliente) con los regímenes de tratamiento correspondientes. Esta evaluación, sin embargo, no proporciona información útil sobre el estado real del volumen intravascular del paciente (para clasificarlo como normovolémico, hipovolémico o hipervolémico) ni sobre si un paciente frío, y por lo tanto hipoperfundido, responderá y se beneficiará de la administración de líquidos.
Por consiguiente, además de esta útil evaluación a pie de cama, es necesario realizar una valoración adecuada del volumen intravascular del paciente para determinar si cabe esperar un beneficio (respuesta positiva a la administración de líquidos) antes de administrarlos. La administración indiscriminada de líquidos intravenosos puede ser perjudicial debido a un aumento de la presión telediastólica del ventrículo izquierdo (PTDVI), ya que la elevación de la PTDVI provoca principalmente un empeoramiento de los síntomas del paciente y, con el aumento de la PTDVI, también de su pronóstico.
En caso de hipovolemia central, la administración de volumen inducirá un aumento significativo del volumen sistólico (flujo) siempre que se pueda activar una reserva de precarga. Por lo tanto, es importante predecir en un paciente hemodinámicamente inestable si aumentará su flujo sanguíneo sistémico (FS) en respuesta a la expansión de volumen.
Kumar demostró que, en individuos sanos, la administración de volumen aumenta la relación presión arterial sistólica/volumen telesistólico del ventrículo izquierdo (VTSVI) y el trabajo sistólico del ventrículo izquierdo (TSVI) mediante:
✅Un aumento del TSVI debido a una reducción del VTSVI mientras que el volumen telediastólico del ventrículo izquierdo (VTDVI) permanece inalterado y
✅Un aumento de la contractilidad.
La contribución del mecanismo de Frank-Starling es leve a moderada; la contractilidad es el componente principal. Kumar examinó a voluntarios sanos y confirmó los hallazgos de estudios en animales realizados en las décadas de 1960 y 1970. El flujo, representado por el FS, es el parámetro original, central y decisivo que debe evaluarse al definir la respuesta a la administración de fluidos.
En la insuficiencia cardíaca, aunque el VDFVI se encuentre dentro del rango normal, la administración de líquidos puede no aumentar el VS debido a una reducción significativa de la contractilidad. Además, sabemos que el mecanismo de Frank-Starling se ve afectado en la insuficiencia cardíaca, por lo que la expansión de volumen puede ser perjudicial y empeorar la situación hemodinámica.
Braunwald, y recientemente Michard, han demostrado que el aumento del VS debido al incremento del VDFVI depende de la contractilidad y la precarga previa a la infusión (longitud inicial de la fibra telediastólica con respecto al mecanismo de Frank-Starling), especialmente en casos de disfunción cardíaca (véase la figura 4).
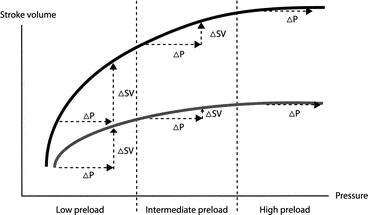
En pacientes con precarga intermedia previa a la infusión (normovolemia), el efecto de la administración de volumen depende exclusivamente de la contractilidad y, en caso de disfunción cardíaca (curva inferior) en pacientes con precarga intermedia, el efecto de la administración de volumen para aumentar el volumen sistólico (VS) y, por lo tanto, el gasto cardíaco (GC) y/o la presión arterial (PA), es mínimo y clínicamente irrelevante.
No obstante, incluso en casos de shock cardiogénico u otros tipos de shock, la administración de líquidos puede ser útil inicialmente. Hasta el 70 % de los pacientes en shock muestran una respuesta positiva (aumento de la presión arterial, incremento de la perfusión de órganos vitales) cuando se administran líquidos. En los pacientes que no responden, la disfunción/insuficiencia del ventrículo derecho (VD) con sepsis suele ser la causa subyacente principal.
Los hechos fisiológicos y fisiopatológicos descritos anteriormente demuestran y enfatizan que la precarga y la respuesta a los líquidos no son lo mismo, como se ha destacado en numerosos estudios publicados. Por lo tanto, como requisitos previos para una respuesta positiva a la administración de líquidos, debe existir tanto una reserva contráctil reclutable (reserva miocárdica) como un sistema vascular y cardíaco central hipovolémico, ya sea absoluto o relativamente, que proporcione una reserva de llenado.
Un aumento del volumen sistólico (VS) ≥15% debido a la administración de volumen es el indicador más aceptado para confirmar una respuesta positiva a la administración de líquidos, aunque otros definen una respuesta positiva si el VS aumenta ≥10% como consecuencia de la expansión de volumen.
Predicción de la respuesta a los fluidos
Mediciones de presión
Las presiones de llenado cardíaco, como la PVC y la relación PVC/PCP, no han logrado predecir ni la precarga ni la respuesta a la fluidoterapia. La relación (si la hay) entre el volumen intravascular/intraventricular y la PVC/PCP es, como ya se mencionó, muy débil tanto en pacientes enfermos como en voluntarios sanos. Incluso en pacientes sedados y con ventilación mecánica, la PVC y la PCP han demostrado ser parámetros poco fiables para reflejar la precarga o predecir la respuesta a la fluidoterapia. Osman afirma que «se ha documentado que la respuesta a la fluidoterapia no guarda relación con la PVC/PAD ni con la relación PCP/PVD, respectivamente».
Mediciones volumétricas
Se ha demostrado que las mediciones volumétricas (RVEDV, ITBV o GEDV) y las áreas ventriculares (LVEDA o LVEDD) son útiles para evaluar la precarga y parecen ser mejores que las presiones de llenado cardíaco para guiar la terapia de volumen; sin embargo, lamentablemente, aún no son muy eficaces para predecir la respuesta a la fluidoterapia.
En particular, se esperaba que el GEDV(I), que refleja el volumen sanguíneo central, y la medición directa del RVEDV superaran las dificultades mencionadas. No obstante, el parámetro volumétrico GEDV, medido indirectamente, no proporcionó información predictiva adicional sobre la respuesta del paciente a la expansión de volumen. La medición directa del valor absoluto del RVEDV permite una evaluación definitiva del estado de volumen; sin embargo, lamentablemente, mientras que el VS aumentó con la administración de volumen, no se observó ningún cambio en el RVEDV medido.
Además, Reuter encontró una correlación débil entre el VS y el LVEDA (obtenido mediante ecocardiografía), y Slama demostró que los cambios en el LVEDD también dependen de la rigidez del ventrículo izquierdo. Otros autores confirmaron posteriormente la escasa correlación entre el diámetro telediastólico del ventrículo izquierdo (LVEDD) y el volumen sistólico/gasto cardíaco (SV/CO).
Por lo tanto, las presiones de llenado como la presión venosa central (CVP)/presión auricular derecha (RAP), la presión capilar pulmonar en cuña (PCWP) o las áreas/dimensiones geométricas del ventrículo izquierdo (LVEDA o LVEDD) no permiten predecir la respuesta a la administración de fluidos, ni las mediciones directas o indirectas de los volúmenes telediastólicos pueden predecir la respuesta del paciente a la expansión de volumen.
La precarga no es lo mismo que la capacidad de respuesta de la precarga.
Osman concluye que, en la evaluación de la respuesta a la precarga, es necesario medir otros parámetros además de las presiones y los volúmenes ventriculares.
Parámetros dinámicos
A diferencia de los parámetros estáticos descritos anteriormente para evaluar las presiones y volúmenes de llenado, así como las áreas del ventrículo izquierdo, contamos con parámetros dinámicos, que comprenden la variación del volumen sistólico (VS-V), la variación de la presión del pulso (PP-V), la variación de la presión arterial sistólica (SP-V) y los cambios en el flujo sanguíneo aórtico. Estos parámetros proporcionan información sustancial y son herramientas valiosas para predecir la respuesta a la administración de fluidos.
Los parámetros dinámicos reflejan los cambios en el VS-VI debidos a las interacciones cardiopulmonares inducidas por la ventilación mecánica. Diversos estudios han documentado que las variaciones en el VS-VI asociadas a la ventilación mecánica son altamente predictivas de la respuesta a la precarga.
Las alteraciones en la precarga cardíaca y, por lo tanto, las variaciones en el VS-VI asociadas a la respiración, se denominan VS-V y se definen por los valores máximo y mínimo de VS durante un período de tres respiraciones, o en un intervalo de tiempo de 20 a 30 segundos. La relación volumen sistólico-volumen (VS-V) se ha validado en varios estudios para pacientes profundamente sedados y con ventilación mecánica, con un volumen corriente de 6 mL/kg y sin esfuerzo respiratorio espontáneo. Una VS-V ≥ 10 % predice un aumento del gasto cardíaco (GC) ≥ 15 % tras la administración de un bolo de líquido de 500 mL.
La ventilación con presión positiva, con sus aumentos cíclicos de la presión intratorácica y el volumen pulmonar, induce variaciones intermitentes en la precarga cardíaca (interacción corazón-pulmón). Esto se debe principalmente a una reducción del retorno venoso secundaria al aumento de la presión en la aurícula derecha durante la inspiración mecánica; por lo tanto, se reduce el llenado del ventrículo derecho (↓ RVEDV). De acuerdo con el mecanismo de Frank-Starling, esto produce una reducción del volumen sistólico del ventrículo derecho (VS-VD). Un efecto adicional, que contribuye al menos parcialmente a la reducción del VS-VD, es el aumento de la impedancia de salida del ventrículo derecho y, por consiguiente, un incremento de la poscarga del ventrículo derecho con la consiguiente alteración de la eyección del ventrículo derecho secundaria a la ventilación con presión positiva.
Sin embargo, esta reducción inspiratoria del volumen sistólico del ventrículo derecho (VSVD) afecta al llenado del ventrículo izquierdo (VI) tras unos pocos latidos, produciendo una disminución del volumen telediastólico del ventrículo izquierdo (VTDVI). En consecuencia, el VSVI se reduce, y este efecto se manifiesta durante la espiración. Por lo tanto, las variaciones del llenado del VD dependientes de la ventilación inducirán variaciones cíclicas en el llenado del VI con una reducción concomitante del VSVI y, por ende, de la presión arterial, si tanto el VD como el VI responden a la administración de fluidos.
Por el contrario, durante la inspiración ocurre lo opuesto: un mayor llenado del VI dará lugar a un VTDVI más elevado y, por consiguiente, a un VSVI y una presión arterial más elevados.
La influencia de la ventilación con presión positiva sobre los cambios hemodinámicos cíclicos es mayor cuando el volumen sanguíneo central es bajo que cuando es normal o alto.
Los parámetros dinámicos perderán su validez si los volúmenes corrientes varían entre respiraciones, como ocurre con la respiración espontánea (asistida) o en caso de arritmias marcadas que inducen variaciones en el VSVI. Se observaron valores exagerados de VS-V con grandes volúmenes corrientes, menor distensibilidad de la pared torácica y atrapamiento aéreo. Además, una presión intraabdominal moderadamente elevada (hasta 20 cm H2O) afecta los cambios circulatorios cíclicos al inducir un aumento progresivo de la presión intratorácica, lo que intensifica las fluctuaciones de la presión pleural y, por lo tanto, puede simular una respuesta a la administración de líquidos; si la presión intraabdominal es superior a 20 cm H2O, se observa una menor influencia.
No obstante, los parámetros dinámicos han demostrado ser mucho mejores que los estáticos para predecir la respuesta a la administración de líquidos y actualmente constituyen el método de elección en pacientes sedados y ventilados.
La variación dinámica del VS-VI es el estándar de oro actual para predecir la respuesta a la administración de líquidos; sin embargo, el VS-V, aunque afectado por la precarga, también parece reflejar predominantemente la respuesta miocárdica a la sobrecarga de volumen. Esto concuerda con nuestro conocimiento de que el volumen sistólico (VS) depende principalmente de la función del ventrículo izquierdo (principalmente de la contractilidad y, en la insuficiencia cardíaca, también de la poscarga) y no de la precarga previa a la infusión. Kumar demostró que, en voluntarios sanos, el aumento del VS debido a la administración de volumen se debe principalmente a un incremento de la contractilidad, más que a un aumento del volumen de llenado, y, por lo tanto, a una mayor distensión de las fibras, como describieron Frank y Starling.
Además de la evaluación del VS-V durante la ventilación mecánica con presión positiva, los indicadores indirectos del VS, como el flujo aórtico, la presión arterial sistólica (PAS-V) y la presión del pulso (PP-V), han demostrado ser índices fiables y valiosos para evaluar el volumen sanguíneo central y la respuesta a la administración de fluidos.
Flujo sanguíneo aórtico descendente como correlato directo de SV/CO
El flujo sanguíneo de la aorta descendente representa la mayor parte del gasto cardíaco (GC) y se acepta como una estimación clínicamente realista del volumen sistólico (VS) y/o del GC. Las mediciones de la velocidad del flujo Doppler aórtico permiten determinar el VS, calculado mediante el producto del intervalo velocidad-tiempo en la aorta ascendente (estimado por ecocardiografía) o descendente (medición Doppler esofágica) y un diámetro aórtico medido o estimado utilizando el nomograma de Boulnois. Se ha demostrado que estas mediciones de la velocidad del flujo predicen con precisión la respuesta a la administración de fluidos.
Variación de la presión sistólica (SP-V)
La variación de la presión sistólica (VPS) es probablemente la forma más sencilla de evaluar la respuesta a la administración de fluidos y se define como un aumento o disminución de la presión arterial sistólica con cada respiración mecánica en relación con la presión sistólica durante la fase de apnea corta. Numerosos estudios han demostrado su utilidad como parámetro sensible para predecir la respuesta a la precarga en pacientes con ventilación mecánica sin respiración espontánea. La sensibilidad de este método no es tan alta como la de la variación de la presión de pulso (VPP) porque no cuantifica los componentes variables de la presión arterial diastólica.
Variación de la presión del pulso (PP-V)
La variación de la presión del pulso (PP-V) podría ser el indicador indirecto más robusto y sensible del estado de volumen. La variación de la presión del pulso aórtico (presión del pulso aórtico ~ VSVI) se ha establecido como un índice basado en la evidencia para evaluar y predecir la respuesta a la administración de fluidos en pacientes con ventilación mecánica. Una variación cíclica de la presión del pulso aórtico, debida a la variación del VSVI durante un ciclo respiratorio, superior al 13 % (r² = 0,85, p < 0,001) implica una probabilidad muy alta (85 %) de que el paciente se beneficie de la administración de fluidos, con un aumento significativo del VS y, por consiguiente, de la presión arterial (valor predictivo positivo del 94 %, valor predictivo negativo del 96 %).
Cálculo de la PP-V durante un ciclo respiratorio:
Elevación pasiva de las piernas (EPL), una autotransfusión de fluidos
Varios estudios publicados recientemente han aportado evidencia alentadora de que la predicción de la respuesta a la administración de fluidos es factible tanto en pacientes con respiración espontánea como en pacientes ventilados.
Elevar las piernas a aproximadamente 30 o 45° se denomina elevación pasiva de las piernas (EPL) y aumenta el flujo aórtico en caso de existir una reserva de precarga reclutable entre 15 y 60 segundos después de elevar las piernas. Este efecto se mantiene durante 30 a 90 segundos (Pinsky, hasta 3 minutos).
Estudios clínicos han demostrado que el volumen de sangre transferido al corazón mediante la EPL es suficiente para aumentar el volumen de llenado del ventrículo izquierdo. Si bien el valor predictivo de los cambios transitorios en el volumen sistólico (VS) es solo aceptable si el VS o sus indicadores indirectos, SP-V y PP-V, se estiman a partir de una curva de presión de pulso periférica —debido a la influencia de la distensibilidad arterial y el tono vasomotor—, se lograron altas sensibilidades al medir las variaciones del VS de forma central, es decir, mediante Doppler esofágico, ecocardiografía o acceso a la arteria femoral, que se considera central: Monnet halló una sensibilidad del 97 % y una especificidad del 94 % para lograr un aumento ≥15 % en el flujo sanguíneo aórtico en respuesta a la administración de volumen si, durante la elevación pasiva de las piernas (EPL), el flujo sanguíneo aórtico aumentaba ≥10 %. Lamia mostró una especificidad similar (100 %), pero con una sensibilidad ligeramente inferior (aunque aún buena) del 77 %.
Por lo tanto, un aumento del flujo sanguíneo aórtico (VS/GC) de ≥10 % o 12,5 % durante la elevación pasiva de las piernas (EPL) predice de forma fiable la hipovolemia central y una respuesta positiva a la expansión de volumen, tanto en pacientes con ventilación mecánica como en aquellos que respiran espontáneamente. En ausencia de hipovolemia central y/o en presencia de un ventrículo derecho (VD) y/o izquierdo (VI) no reactivos (función comprometida, principalmente contractilidad alterada), el VS/GC no aumentará con la maniobra de EPL.
Dado que no se administran fluidos externos, se evitan los riesgos de la sobrecarga de volumen innecesaria y, por consiguiente, la medición del flujo sanguíneo central (flujo sanguíneo aórtico, normalmente representado por VS o GC) en respuesta a la EPL es más robusta y probablemente superior a la presión de perfusión-volumen (PP-V) al evaluar la respuesta a la fluidoterapia de los pacientes, incluso en aquellos que respiran espontáneamente. Además, este enfoque es más independiente de las variaciones del volumen corriente y las arritmias que un enfoque periférico. La medición central del flujo sanguíneo evita las influencias relevantes de la distensibilidad arterial y el tono vasomotor, así como los cambios complejos en la propagación y reflexión de la onda de pulso a lo largo del sistema vascular arterial, los cuales pueden variar durante la elevación pasiva de las piernas con un cambio concomitante en el volumen sistólico.
Desafío de fluidos
La prueba de sobrecarga de líquidos sigue siendo recomendable para evaluar la necesidad de administrar más líquidos, siempre que se realice un seguimiento estricto y se observe atentamente la respuesta. Sin embargo, los parámetros dinámicos descritos anteriormente son claramente superiores y debe evitarse la administración de volumen a ciegas siempre que sea posible.
Una prueba de sobrecarga de líquidos no implica una reanimación con líquidos; simplemente identifica a los pacientes que probablemente mostrarán una respuesta beneficiosa a la administración de líquidos (adicionales). Para minimizar la cantidad de líquido necesaria para evaluar la respuesta, este debe administrarse rápidamente y algunos autores requieren un aumento de la PVC de al menos 2 mmHg para confirmar que se ha administrado una cantidad suficiente de líquido. Se espera que la administración rápida en bolo de 250 ml en 5-7 minutos o de 500 ml en 10 minutos de líquido o de la elevación pasiva de las piernas (EPP) muestre una respuesta hemodinámica adecuada si resulta beneficiosa para el paciente. Si existe una reserva de precarga reclutable, el volumen sistólico (VS) debe aumentar.
Aunque no existe un consenso general sobre qué constituye una prueba de sobrecarga de líquidos adecuada, la mayoría de los estudios coinciden en que una respuesta positiva se indica por una mejoría del estado circulatorio, manifestada por un aumento de la presión arterial (PA), una frecuencia cardíaca sin cambios o disminuida, un aumento concomitante del volumen sistólico (VS) y una mejoría del flujo sanguíneo efectivo, documentada por un aumento de la relación ScvO2/SvO2 y una disminución del lactato.
Es importante recordar que una prueba de sobrecarga de líquidos solo debe realizarse si existe una indicación clara, es decir, en el contexto de hipoperfusión, y cuando la correlación entre el cambio en la PA y el gasto cardíaco (GC) es muy baja. Si no se observa ningún efecto positivo, la administración de líquidos es inútil, potencialmente dañina y debe suspenderse de inmediato.
A pesar de la incertidumbre, incluso en situaciones de riesgo vital como el choque cardiogénico, la administración de cantidades moderadas de líquidos (aproximadamente 3 ml/kg, es decir, entre 250 y 300 ml) como prueba de sobrecarga de líquidos bajo estrecha monitorización es apropiada y puede estabilizar temporalmente la situación aguda.
La reanimación con líquidos adecuada e inmediata en pacientes críticos, si es suficiente, mejorará el pronóstico. McConachie afirma que la prueba de sobrecarga de líquidos es apropiada en prácticamente todos los pacientes críticos en estado de shock con presión arterial demasiado baja y/o hipoperfusión debido a un bajo gasto cardíaco, a menos que presenten insuficiencia cardíaca congestiva grave.
Por otro lado, cabe destacar que, si bien un paciente responde a la administración de volumen, esto no significa automáticamente que lo necesite, ya que los sujetos sanos también responden.
Vincent y Weil propusieron recientemente el siguiente algoritmo como el enfoque adecuado para realizar una prueba de sobrecarga de líquidos. En pacientes hipotensos con compromiso circulatorio, administrar 250-500 ml de solución coloidal (~3-5 ml/kg) durante 15-20 minutos para estabilizar hemodinámicamente al paciente (al menos temporalmente), mejorar la perfusión de órganos y tejidos, y evaluar si es probable que responda positivamente a una mayor administración de líquidos.
Criterios que sugieren una sobrecarga de volumen efectiva:
✅Aumento del volumen sistólico (VS) ≥10% y/o aumento de la presión arterial sistólica ≥10%,
✅frecuencia cardíaca sin cambios o reducida,
✅aumento de la presión venosa central (PVC) ≤ 2–5 mmHg (si >5, suspender la administración; precaución si el aumento es >2),
✅ausencia de signos clínicos de sobrecarga de líquidos,
✅parámetros adicionales, si se monitorizan:
➡️aumento de la presión capilar pulmonar (PCP) ≤ 3–7 mmHg; suspender la administración de líquidos si el aumento es >7 mmHg,
➡️insuficiencia de agua extravascular pulmonar (EVLWI) antes y después de la administración de líquidos ≤ 7–10 mL/kg,
➡️disminución del lactato, resultado positivo en la prueba de sobrecarga de líquidos (ver más abajo),
➡️aumento de la diuresis.
Suspender la administración de líquidos durante o después de la infusión si:
✅El VS/la presión arterial no aumenta adecuadamente (<10%);
✅La hipoperfusión no mejora (clínicamente, no hay aumento de la diuresis, ni disminución de lactato ni de la saturación de oxígeno, ni cambios en la capnografía/OPS que indiquen mejoría en la perfusión tisular);
✅Aumento de la PVC > 5 mmHg debido a la administración de volumen; precaución si el aumento es > 2: mayor riesgo de DVI;
✅Alto riesgo de DVI si la PVC > 9-10 mmHg y, en particular, si el volumen sistólico/la presión arterial disminuyen durante la administración de volumen.
✅Parámetros adicionales, si se monitorizan:
➡️EVLWI > 10 mL/kg,
➡️Aumento de la PCWP > 7 mmHg.
Una Conferencia de Consenso Internacional de 2006 sugirió que un aumento de la PVC de al menos 2 mmHg, ya sea por la administración de 250 ml de líquido en 10-15 minutos o por la elevación de las piernas, indicaría una administración suficiente de líquidos, definiendo una respuesta positiva si la función cardíaca y la perfusión tisular mejoran. Sin embargo, cabe destacar que esta recomendación no es específica y se basa únicamente en la opinión de expertos.
Como sabemos, la PVC no refleja la precarga ni sus cambios, ni en pacientes sanos ni en pacientes críticos. Por lo tanto, la PVC no puede utilizarse como predictor del llenado del ventrículo derecho ni para evaluar el efecto de la sobrecarga de volumen. Un cambio en la magnitud de la PVC de al menos 2 mmHg es el mínimo necesario para una detección fiable en la mayoría de los monitores actuales y, por consiguiente, parece ser una cifra arbitraria. Es importante recordar que, en pacientes con buena función cardíaca, la PVC puede incluso disminuir a pesar de que la sobrecarga de líquidos sea exitosa y, si se utiliza el método de elevación de las piernas, la monitorización central es esencial, ya que la periférica resulta insuficiente.
Monitorización PiCCO (Gasto cardíaco continuo inducido por pulsos)
PiCCO es un método de monitorización hemodinámica que combina la termodilución transpulmonar y el análisis continuo del contorno del pulso arterial.
Este método permite medir volúmenes como el volumen sanguíneo intratorácico (VST), que representa el estado del volumen intravascular; el volumen telediastólico global (VTDG) (de las cuatro cavidades); y, de suma importancia, el agua pulmonar extravascular (APEV).
Estas mediciones volumétricas se realizan de forma semiinvasiva y son superiores a las mediciones de presión habituales, PVC y PCP, para evaluar el estado del volumen intravascular del paciente y la precarga cardíaca. Lamentablemente, estos parámetros (VST y VTDG) no permiten predecir la respuesta del sistema circulatorio a la administración de fluidos. Sin embargo, el método PiCCO cumple con todos los requisitos para evaluar la respuesta a la elevación pasiva de las piernas (EPL).
El APEV es un parámetro sumamente informativo, cuya precisión en la medición de la cantidad real de líquido en el tejido pulmonar ha sido demostrada. Su valor proporciona información sustancial sobre el pronóstico del paciente. Actualmente, es el único método capaz de diagnosticar el edema pulmonar incipiente antes que todos los demás métodos disponibles, incluyendo la exploración clínica, la radiografía de tórax y la medición de la presión mediante catéter de arteria pulmonar (PCPW). Además, permite orientar la investigación de la acumulación patológica de agua pulmonar, ya sea por causas cardíacas o extracardíacas.
Dos tercios de los pacientes con insuficiencia cardíaca y una PCPW media inferior a 18 mmHg (18 mmHg es el límite superior generalmente aceptado en caso de insuficiencia cardíaca, que probablemente proporciona el volumen sistólico máximo reclutable por precarga) presentan un aumento significativo de la relación EVLW/EVLWI, aunque no sea detectable mediante auscultación ni radiografía. Por otro lado, en algunos casos de shock cardiogénico, especialmente en pacientes previamente sanos con infarto agudo de miocardio, la PCPW se considera normal (≤12 mmHg), pero la EVLW ya está elevada, lo que indica la presencia de edema pulmonar. Un aumento de EVLW/EVLWI indica una mayor mortalidad y, en el caso de un EVLW elevado, cualquier reducción de líquidos conducirá a un aumento de CO (Fig. 5).
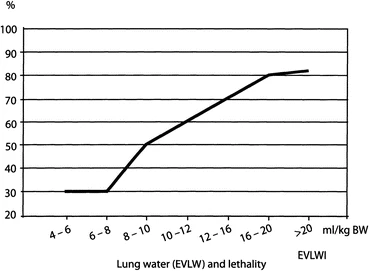
El EVLW es valioso para indicar sobrecarga de líquidos y su valor (rango normal de EVLWI: 3-7 mL/kg) debe influir en la decisión terapéutica. Si el EVLWI supera los 10 mL/kg, la mortalidad aumenta exponencialmente y no se recomienda la administración de más líquidos.
El índice de permeabilidad PVPI (PVPI = EVLW/volumen sanguíneo pulmonar (PBV), donde PBV = ITBV − GEDV) refleja, si está elevado (>3), un aumento de la permeabilidad capilar (fuga capilar que produce edema no cardiogénico), mientras que un índice <3, junto con un EVLW/I elevado, sugiere un edema cardiogénico.
Ecocardiografía
La ecocardiografía es fundamental para diagnosticar la patología subyacente en la insuficiencia circulatoria y/o la disfunción cardíaca. Heidenreich mejoró la precisión diagnóstica al identificar un 28 % más de las etiologías subyacentes en la hipotensión inexplicada mediante ecocardiografía transesofágica (ETE), además de los demás parámetros hemodinámicos obtenidos. De este modo, demostró que la ETE aporta información significativa a los datos hemodinámicos adquiridos de forma invasiva. La ecocardiografía permite diagnosticar rápidamente y facilitar la toma de decisiones terapéuticas cruciales en casos de taponamiento cardíaco y disección aórtica, confirmando el diagnóstico clínico de endocarditis, revelando evidencia de embolia pulmonar hemodinámicamente significativa y, por supuesto, resulta extremadamente útil para evaluar el rendimiento cardíaco.
La evaluación del VS/GC, probablemente el principal determinante de una perfusión orgánica adecuada, es relativamente fácil de obtener mediante la medición del flujo en la aorta descendente. Laupland demostró que este método es sencillo, rápido de aprender y de fácil aplicación en la práctica diaria. Sin embargo, presenta algunas limitaciones. Se asume que aproximadamente el 70 % del gasto cardíaco total (GC) llegará a la aorta descendente y, además, en lugar de medir el diámetro del tracto de salida del ventrículo izquierdo (TSVI) necesario para el cálculo del GC, se utiliza un nomograma de Boulnois. Por lo tanto, este método proporciona una estimación aproximada del GC y las correlaciones con las mediciones invasivas son débiles en comparación con el cateterismo de la arteria pulmonar (PA) o la ecocardiografía transesofágica con contraste (PiCCO). Si se estima el GC mediante cateterismo de la PA, como recomiendan la ESC y la AHA, se requieren habilidades y capacitación avanzadas.
Se han realizado 11 estudios amplios que evalúan el uso de la ecocardiografía como método de monitorización continua en pacientes críticos, la mayoría de ellos utilizando la técnica transesofágica. No se puede llegar a una conclusión definitiva sobre si la ecocardiografía debe recomendarse como equivalente a los métodos establecidos para la monitorización hemodinámica continua.
La ecocardiografía requiere mucho tiempo, formación médica avanzada en adquisición e interpretación de datos, y no es realista implementar esta tecnología las 24 horas del día a nivel mundial. La utilidad de la ecocardiografía radica en su capacidad diagnóstica, y existe consenso en que es absolutamente esencial en la evaluación inicial de todos los pacientes con shock (cardiogénico), por lo que debe realizarse lo antes posible. La ecocardiografía (especialmente la transesofágica) suele revelar anomalías que pasan desapercibidas con las técnicas de evaluación invasivas basadas en catéter, como la obstrucción del tracto de salida del ventrículo izquierdo, la interacción diastólica ventricular, la disfunción/insuficiencia del ventrículo derecho, la disfunción diastólica del ventrículo izquierdo, la valvulopatía, la compresión cardíaca, etc. Además, tiene un gran impacto en las consideraciones terapéuticas, ya que el 60 % de los tratamientos planificados se modifican tras la realización de la ecocardiografía.
La ecocardiografía puede salvar vidas; en pacientes con insuficiencia cardíaca, es mucho más sencilla y rápida que el cateterismo de la arteria pulmonar y proporciona información hemodinámica clave.
Presión arterial
Presión arterial y autorregulación
Una perfusión orgánica adecuada es esencial para evitar el desarrollo de shock. Si bien la presión arterial media (PAM) es la mejor estimación de la presión de perfusión orgánica, no existe un umbral de presión conocido que defina una perfusión adecuada entre los distintos órganos, entre pacientes o en un mismo paciente a lo largo del tiempo. La autorregulación de la mayoría de los órganos mantiene un flujo sanguíneo constante y específico para cada órgano en un amplio rango de presiones arteriales variables y cambios en las tasas metabólicas, pero la hipotensión siempre es patológica.
La mayoría de los autores definen la hipotensión como una presión arterial sistólica < 90 mmHg y una PAM ≤ 65-70 mmHg, aunque en pacientes hipertensos conocidos este umbral puede modificarse a una PAM ≤ 85 mmHg y, en pacientes hipotensos conocidos, ≤ 50-60 mmHg. En pacientes con cardiopatía isquémica, se suele utilizar una PAM ≤ 75-80 mmHg.
La hipotensión altera la distribución autorregulada del flujo sanguíneo, y la presión arterial media necesaria para mantener la autorregulación varía de un órgano a otro y depende de las condiciones clínicas (es decir, si se conoce o no una enfermedad arteriosclerótica).
Riñones
La autorregulación mantiene un flujo sanguíneo renal constante, actuando dentro de un rango de presión arterial media (PAM) de entre 80 y 180 mmHg. Iglesias exige una PAM superior a 70 mmHg para prevenir la insuficiencia renal aguda o, si ya se ha desarrollado una lesión renal aguda, para restablecer una perfusión renal adecuada. Esson subraya que una presión de perfusión renal adecuada es fundamental en el tratamiento de la insuficiencia renal aguda.
Cerebro
La autorregulación funciona dentro de un rango de PAM de 60 a 160 mmHg; las recomendaciones para una presión de perfusión cerebral adecuada en enfermedades críticas varían desde al menos 60 mmHg hasta ≥70 mmHg.
(En caso de lesión cerebral, incluso presiones más elevadas podrían ser deseables).
Corazón
La presión de perfusión coronaria (PPC) se determina mediante:
La autorregulación coronaria funciona entre 50 y 60 mmHg, hasta 140 mmHg. Esto significa que, en caso de una presión telediastólica del ventrículo izquierdo (LVEDP) elevada (>15 mmHg), es fundamental una presión diastólica mínima de >65 mmHg. En la enfermedad coronaria, se requieren presiones aún mayores para prevenir un mayor deterioro debido a la isquemia progresiva.
Choque séptico
En el choque séptico, se recomienda una PAM entre ≥ 65 mmHg y 75 mmHg (en pacientes con enfermedad arterial oclusiva conocida, arteriosclerosis periférica o hipertensión de larga evolución). Un estudio de LeDoux demostró que una PAM entre 65 mmHg y 85 mmHg no se asoció con diferencias significativas en la perfusión orgánica.
Esto fue confirmado por Bourgoin, quien demostró que un aumento de la PAM de 65 mmHg a 85 mmHg con una infusión de noradrenalina no mejoró la función renal. El punto clave es que, siempre que la autorregulación no esté sustancialmente alterada, una PAM de ≥ 65 mmHg es suficiente. Sin embargo, en caso de una alteración de la autorregulación, se requieren PAM más elevadas para restablecerla.
No obstante, incluso una presión arterial generalmente considerada normal no refleja necesariamente la estabilidad hemodinámica ni una perfusión orgánica adecuada. La presión arterial es un indicador inadecuado de choque incipiente en un paciente. Por lo tanto, es esencial evaluar la perfusión tisular.
Evaluación de la perfusión tisular
La perfusión orgánica depende esencialmente del flujo sanguíneo y, por lo tanto, de la función cardíaca. Se sabe que el shock circulatorio causa hipoperfusión tisular, y una perfusión tisular inadecuada se asocia con una mayor morbilidad y mortalidad.
En comparación con la difícil tarea de evaluar el estado de los fluidos vasculares y la probable respuesta del paciente a la expansión de volumen, la hipoperfusión tisular puede evaluarse con bastante precisión mediante la exploración clínica. Los signos clínicos que sugieren hipoperfusión tisular son:
✅taquicardia,
✅hipotensión (PAS < 90 mmHg, PAM < 70 (60) mmHg o descenso de la PA > 40 mmHg),
✅oligo-/anuria,
✅signos clínicos o biológicos de depleción de líquido extracelular (cetoacidosis, vómitos, diarrea),
✅retraso en el llenado capilar,
✅piel moteada,
✅alteración del nivel de conciencia.
Menon recomienda encarecidamente el diagnóstico de shock cardiogénico (SC) en todos los pacientes que presenten signos de perfusión tisular inadecuada en el contexto de una disfunción cardíaca grave, independientemente de la presión arterial.
La saturación venosa mixta de oxígeno (SvO2) refleja el equilibrio entre el aporte y el consumo de oxígeno. Pinsky y Reinhart afirman que una disminución de la SvO2 a <70% representa un aumento de la extracción de oxígeno por los tejidos, lo que sugiere hipoperfusión. Una SvO2 persistentemente <30% se asocia con isquemia tisular grave.
Los niveles de lactato plasmático, aunque inespecíficos, constituyen un indicador fiable de perfusión tisular inadecuada. Una reducción de un valor inicialmente elevado indica una mejoría de la perfusión.
Por lo tanto, un aumento de los niveles de lactato plasmático y una disminución de la SvO2, junto con una exploración clínica sugestiva, pueden contribuir al diagnóstico precoz de hipoxia tisular.
Ander descubrió que la monitorización de la saturación venosa central de oxígeno (ScvO2) y el lactato en pacientes con insuficiencia cardíaca grave (pacientes con miocardiopatía conocida ingresados por descompensación aguda) es superior a la evaluación y monitorización de los signos vitales clínicos para la detección del shock cardiogénico oculto. Si ambos parámetros son anormales (lactato > 2 mmol/L, ScvO2 < 60%), se puede identificar claramente el shock cardiogénico oculto/precardiogénico que requiere un enfoque terapéutico especial, algo que no es posible con los signos vitales.
Los avances más recientes, como la capnografía sublingual, la espectroscopia espectral de polarización ortogonal (OPS) y la espectroscopia de infrarrojo cercano (NIRS), intentan medir el flujo sanguíneo tisular local y la utilización de oxígeno, y evaluar cualquier mejoría debida a la intervención terapéutica.
Dado que el uso del enfoque hemodinámico y de oxigenación global convencional puede no proporcionar información adecuada sobre la perfusión tisular, la monitorización no invasiva de la perfusión periférica podría ser complementaria para alertar sobre una hipoxia tisular global inminente.
Cabe recordar que la monitorización hemodinámica tiene como objetivo restablecer los parámetros hemodinámicos normales para prevenir lesiones orgánicas y corregir la disfunción orgánica; sin embargo, esto no siempre es válido. La monitorización hemodinámica suele evaluar el estado circulatorio global, no la función orgánica ni la microcirculación, y no aborda los mecanismos por los que se produce la enfermedad. Por lo tanto, debemos ser cautelosos al extraer conclusiones terapéuticas de los resultados de la monitorización de la macrocirculación, ya que una mejora de la misma puede comprometer aún más la microcirculación.
Poscarga
Definición
La fuerza que se opone al acortamiento de las fibras miocárdicas durante la eyección ventricular se denomina poscarga.
Propiedades vasculares, elastancia arterial efectiva, tensión de la pared y la ley de Laplace.
Braunwald afirma: «La carga que se opone a la eyección del ventrículo izquierdo, en su forma más simple, se refleja en la presión arterial sistólica». Sin embargo, la fisiología es mucho más compleja y la presión arterial sistólica ha demostrado ser un indicador muy deficiente de la poscarga. De hecho, el sistema arterial impone una carga hidráulica al corazón, y una mayor carga arterial requiere mayor energía para expulsar una cantidad determinada de sangre. Esta carga vascular e hidráulica, que se opone a la eyección ventricular, se describe y refleja de forma más completa mediante la impedancia de entrada aórtica (o, respectivamente, la impedancia de entrada de la arteria pulmonar).
Los principales parámetros que caracterizan la impedancia de entrada arterial son la resistencia vascular periférica, la distensibilidad arterial total y la impedancia característica aórtica. Mientras que la resistencia vascular periférica especifica las condiciones de estado estacionario, los componentes de la carga pulsátil (que es compleja y varía con el tiempo) se representan mediante:
- La distensibilidad arterial total refleja, al cuantificar la relación presión-volumen, el comportamiento estructural general del sistema arterial en su conjunto, pero específicamente representa propiedades relacionadas con la propagación y reflexión de la onda de pulso, lo que afecta las condiciones de carga, ya que la intensidad y el momento de las reflexiones de la onda de presión se ven influenciados por las fuerzas de inercia y se oponen a la eyección del ventrículo izquierdo.
- La impedancia característica aórtica, que contribuye hasta en un 80 % a la distensibilidad total.
La impedancia característica describe propiedades físicas, como la viscoelasticidad y las dimensiones de los grandes vasos arteriales centrales y proximales (aorta y arteria pulmonar, respectivamente), y, por lo tanto, la contribución de las propiedades elásticas vasculares a la carga total. La poscarga pulsátil incluye en gran medida la impedancia característica y las reflexiones de la onda de pulso, que se oponen directamente a la eyección ventricular.
De hecho, es necesario prestar especial atención al impacto de los elementos pulsátiles en la carga vascular total, ya que la intensidad y la sincronización de las ondas de presión reflejadas varían según las propiedades elásticas vasculares (principalmente la aorta proximal), pudiendo así ejercer un impacto sustancial en la carga vascular que soporta el ventrículo. En caso de rigidez arterial, como la que se produce con el envejecimiento (fisiológico) o en personas hipertensas, la velocidad de la onda aumenta, y las ondas reflejadas regresan y se suman a las ondas incidentes, incrementando la presión neta y llegando al ventrículo (ya) al final de la sístole, lo que provoca una poscarga ventricular. Simultáneamente, la impedancia de entrada aórtica aumenta considerablemente. Por consiguiente, se ha demostrado que las ondas de presión reflejadas tienen un impacto sustancial en la carga sistólica impuesta al corazón, y se reconoce que la rigidez arterial produce una poscarga ventricular al elevar la carga sistólica (tardía), aumentando así la elastancia ventricular sistólica, comprometiendo el llenado ventricular e influyendo en las propiedades diastólicas al aumentar las presiones de llenado. De hecho, cabe destacar que la función cardíaca diastólica se ve afectada si disminuye la distensibilidad arterial, como ocurre en la rigidez arterial. Por lo tanto, la rigidez vascular central y las reflexiones de la onda de pulso determinan la carga arterial sistólica tardía.
El impacto de la carga pulsátil, en particular de las reflexiones de la onda, es aún más relevante en la circulación pulmonar: a diferencia de la circulación sistémica, la resistencia y la distensibilidad de la vasculatura pulmonar están inversamente relacionadas entre sí y se distribuyen uniformemente a lo largo de todo el árbol vascular. En consecuencia, una presión de enclavamiento capilar pulmonar elevada, al disminuir la resistencia vascular pulmonar, aumenta la poscarga neta del ventrículo derecho, debido al incremento de la carga pulsátil en relación con la resistiva.
Sin embargo, es difícil obtener la impedancia de entrada aórtica (arteria pulmonar), ya que se requiere un análisis en el dominio de la frecuencia (mediante el método de Fourier) de las presiones y los flujos medidos simultáneamente para describir la relación entre la presión arterial y el flujo dentro de un sistema vascular. Esto representa un desafío técnico y, además, sería bastante complicado aplicar los factores derivados del dominio de la frecuencia a conceptos y rutinas clínicas cotidianas. Sunagawa logró que las propiedades vasculares (evaluadas en el dominio de la frecuencia) fueran comparables con las propiedades ventriculares (expresadas en el dominio del tiempo), al agrupar los elementos principales de la carga vascular (resistencia vascular periférica y compliancia arterial total, impedancia característica e intervalos de tiempo sistólico y diastólico) en la elastancia arterial (efectiva) (Ea), lo que constituye una aproximación cercana a la carga arterial. La elastancia arterial efectiva caracteriza la impedancia de entrada aórtica y, por lo tanto, la carga arterial que se impone al ventrículo. Esta «medida simple», que agrupa los componentes estáticos y dinámicos de la impedancia, ha demostrado un buen desempeño en estudios experimentales. Aunque está dominada por el componente de carga no pulsátil (RVS), la Ea también se ve alterada por la rigidez arterial debida al aumento de la carga pulsátil. La Ea es la representación más completa y razonablemente aplicable de la impedancia de entrada aórtica.
En términos operativos, la Ea se define numéricamente como la relación entre la presión ventricular telesistólica y el volumen sistólico, y está directamente relacionada con la frecuencia cardíaca y la resistencia vascular periférica, e inversamente relacionada con la distensibilidad arterial total (determinada, en gran medida, por las arterias elásticas centrales).
Sin embargo, en la práctica, Ea se deriva de la relación presión-volumen, definida como la relación entre la presión telesistólica del ventrículo izquierdo (LVEDSP) y el volumen sistólico del ventrículo izquierdo (LV-SV):
Esta ecuación se puede simplificar aún más: si la presión sistólica del ventrículo izquierdo (PSVI) es igual a la presión arterial sistólica (PAS), corregida por 0,9, la elastancia arterial (Ea) se puede calcular como: Ea = PSVI/VSVI = PAS × 0,9/VSVI.
Los valores normales de Ea rondan los 2,0 mmHg/mL.
En cuanto a la interacción entre el ventrículo derecho y el sistema vascular pulmonar, se ha descrito que la elastancia arterial pulmonar (Ea-Pulm) es una medida fiable de la carga que soporta el ventrículo derecho durante la sístole, y tiene en cuenta la resistencia vascular pulmonar, la distensibilidad y la impedancia, incluyendo así los componentes pulsátiles de la carga arterial.
Sin embargo, la tensión que los sarcómeros de la pared ventricular deben superar durante la sístole para acortarse está relacionada con:
(a) Las características del sistema arterial
(b) El tamaño y las dimensiones de la cavidad del ventrículo izquierdo (VI)
(c) El rendimiento de bombeo del VI
Por consiguiente, además de las propiedades vasculares que se oponen a la eyección y la afectan, existen propiedades cardíacas específicas que contribuyen a la caracterización de la poscarga. Así, la tensión de la pared miocárdica durante la contracción representa la poscarga «verdadera», ya que refleja tanto las condiciones de carga vascular central aórtica como periférica, así como las propiedades intrínsecas del músculo cardíaco, tales como la geometría y el tamaño del VI y la presión intracavitaria.
La relación entre la poscarga y la tensión sistólica de la pared ventricular se puede definir formalmente mediante la ley de Laplace: ơ = p x r/2h
donde la relación r/h es un determinante principal de la tensión de la pared.
(ơ representa la tensión de la pared, p = presión ventricular, r = radio del ventrículo izquierdo o derecho y h = espesor de la pared).
(La ley de Laplace se aplica a figuras esféricas, por lo que su transposición y aplicación al ventrículo derecho, con su radio interno regional variable, puede resultar problemática).
Por lo tanto, aplicada directamente:
La dilatación provoca un aumento del diámetro del ventrículo izquierdo (VI) y, en general, de la presión de llenado del VI (VD), lo que conlleva un incremento de la tensión en la pared. Un aumento del grosor de la pared (en caso de hipertrofia) reduce dicha tensión.
Los determinantes de la tensión de la pared ventricular izquierda (VI), regida por la ley de Laplace, varían continuamente durante la sístole, lo que produce mediciones variables de dicha tensión según la fase del ciclo cardíaco. La tensión máxima se produce durante el primer tercio de la eyección y, posteriormente, disminuye hasta su valor telesistólico, que es inferior al 50 % del valor máximo. Al mismo tiempo, la tensión sistólica total de la pared (estimada mediante la integral de la tensión en función del tiempo) predice el consumo de oxígeno miocárdico.
Todas las medidas muestran una diferencia significativa, y la elección del índice depende de la pregunta que se plantee:
✅La tensión total refleja el consumo de oxígeno miocárdico,
✅la tensión máxima se correlaciona estrechamente con la progresión de la hipertrofia, y
✅la tensión telesistólica de la pared representa con mayor precisión la poscarga.
La excelente correlación entre la tensión de la pared al final de la sístole y la longitud de las fibras miocárdicas al final de la sístole, así como entre la tensión de la pared al final de la sístole y el volumen ventricular al final de la sístole (VTS), subraya el hecho de que la tensión de la pared al final de la sístole es, literalmente, la (pos)carga que limita la eyección.
Además, varios autores han confirmado la excelente correlación entre la tensión parietal telesistólica y la poscarga del ventrículo izquierdo (VI) en la práctica clínica diaria.
Durante la sístole, el tamaño de la cavidad del VI disminuye a medida que el ventrículo se contrae, lo que reduce la tensión parietal. Cuando la poscarga aumenta, se requiere un mayor incremento de presión para cualquier reducción del tamaño de la cavidad; por lo tanto, la tensión parietal durante la sístole es mayor. El aumento de presión debe ser aún mayor, por supuesto, en un VI con dilatación primaria.
Cabe mencionar que Reichek (evaluación en modo M, tensión parietal meridional) y Greim (evaluación en 2D, tensión parietal circunferencial) describen dos métodos ecocardiográficos que evalúan directamente la tensión parietal telesistólica. Ambos métodos son laboriosos, requieren habilidades avanzadas, y Greim expresa dudas sobre la capacidad del modo M para detectar cambios agudos en la poscarga en pacientes sometidos a cirugía cardiotorácica.
En resumen, dos conceptos biofísicos alternativos pueden describir y caracterizar la poscarga. Ross y colaboradores demostraron que el nivel de tensión de la pared, en lugar de la resistencia de entrada o la impedancia pulsátil, determina el rendimiento ventricular, favoreciendo la tensión de la pared como la característica más precisa para representar la poscarga «verdadera». Además, la impedancia de entrada arterial se refiere específicamente a las propiedades vasculares, mientras que prácticamente ignora las propiedades cardíacas. Por lo tanto, mientras que la tensión de la pared integra las fuerzas que se oponen a la eyección ventricular, Ea es una medida de la carga hidráulica que enfrenta el ventrículo. La tensión de la pared se considera la característica más precisa para describir la poscarga ventricular. Sin embargo, aunque la estimación de la tensión de la pared no ha adquirido relevancia clínica en la práctica diaria, Ea puede obtenerse con un esfuerzo razonable.
Desajuste de la poscarga y síndromes de insuficiencia cardíaca aguda
Para un buen funcionamiento, el rendimiento cardíaco y la poscarga deben coincidir, lo que da lugar al concepto de desajuste de la poscarga: básicamente, «un desajuste puede inducirse de forma aguda en un corazón normal si el volumen telediastólico no puede compensar el aumento de la poscarga». Posteriormente, el VS, la FE y la circunferencia ventricular disminuirán. Algunos ejemplos incluyen: la depleción de volumen en presencia de un aumento rápido y sustancial de la presión sistémica, y los aumentos de la poscarga en un ventrículo que ya ha utilizado la reserva máxima de precarga con una longitud media del sarcómero superior a 2,2 μm, lo que indica un estiramiento máximo (limitado por la restricción pericárdica, lo que explica por qué no hay una rama descendente de la curva de Starling). Imponer una carga adicional a dicho ventrículo provocará una caída brusca del VS, a menos que la contractilidad pueda aumentarse intrínsecamente o mediante la aplicación de agentes inotrópicos.
Observaciones finales
La poscarga se define como las fuerzas que se oponen al acortamiento de las fibras musculares ventriculares. Estas fuerzas incluyen:
(a) la carga impuesta por el árbol vascular y las propiedades de la sangre en dichos vasos, y
(b) las propiedades ventriculares que se oponen a la contracción, como las válvulas y la tensión de las fibras musculares.
La tensión sistólica de la pared integra las fuerzas que se oponen a la eyección ventricular; por lo tanto, puede considerarse la característica más precisa para describir la carga que soporta el ventrículo durante la sístole.
Sin embargo, la viabilidad clínica de aplicar uno u otro método para evaluar la compleja relación entre la contracción ventricular, el sistema arterial y el flujo sanguíneo a pie de cama es prácticamente imposible. Además, no se puede esperar que un solo parámetro abarque todos los aspectos. Medir simultáneamente las presiones, el grosor y el radio de la pared en un sistema en constante cambio para determinar la tensión de la pared no es factible actualmente. Por lo tanto, se requieren derivaciones simplificadas y, como tal, la elastancia arterial efectiva ha obtenido una gran aceptación y se utiliza ampliamente, al menos en la investigación médica, para evaluar las relaciones analizadas y, de este modo, comprender mejor los procesos, interrelaciones y secuencias fisiopatológicas y patogénicas.
En la práctica clínica diaria, la resistencia vascular sistémica (periférica) (RVS) es el parámetro más común para describir la poscarga real y, a menudo, se utiliza como sinónimo de poscarga.
Sin embargo, la RVS solo refleja el componente no pulsátil de la carga periférica en condiciones de estado estacionario. No incluye el impacto de las reflexiones de onda, la impedancia arterial ni las propiedades ventriculares. Cada uno de estos fenómenos afecta la poscarga del ventrículo izquierdo independientemente de la resistencia vascular periférica o la presión arterial. El envejecimiento, la hipertensión y la rigidez aórtica contribuyen considerablemente al componente pulsátil de la poscarga, por lo que este componente se vuelve más prominente en dichas condiciones. Lang demostró en su investigación que la medición de la RVS subestima sustancialmente el cambio en la poscarga cuando la poscarga del ventrículo izquierdo (VI) disminuye, aumenta o permanece sin cambios, pero con un aumento simultáneo de la contractilidad. Estos hallazgos no son sorprendentes, ya que, según la relación presión-flujo periférica, el VI no percibe la resistencia periférica sistémica. Sin embargo, la RVS representa el 90 % de la resistencia a la eyección (la resistencia arterial es el componente dominante de la carga de impedancia) y, por lo tanto, se justifica como el parámetro más utilizado para estimar clínicamente la poscarga. Además, la RVS puede ser muy útil para aclarar el diagnóstico, particularmente en pacientes hipotensos y en síndromes de insuficiencia cardíaca, como demostró Cotter.
La alteración fisiopatológica fundamental en los síndromes de insuficiencia cardíaca aguda es una poscarga sustancialmente elevada e inapropiada, con una resistencia sistémica marcadamente elevada y una impedancia de salida del VI marcadamente aumentada, lo que ejerce una alta carga (final)sistólica sobre el VI durante la eyección ventricular. Esto se conoce como desajuste de la poscarga, definido como “una disminución del volumen sistólico (VS) debido a una poscarga excesiva”. En los síndromes de insuficiencia cardíaca, la poscarga del ventrículo izquierdo (VI) se convierte en el factor determinante del rendimiento cardíaco. Ya en 1977, Cohn y Franciosa publicaron su impresionante diagrama que muestra la correlación entre la poscarga y el rendimiento cardíaco/gasto cardíaco (VS) (véase la figura 6).
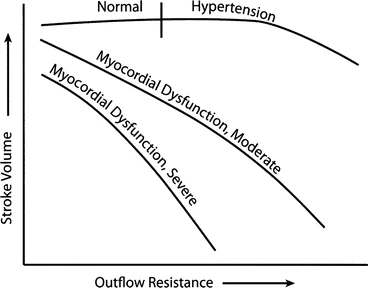
El volumen sistólico (VS) depende decisivamente de la magnitud de la poscarga. Además, una poscarga elevada provoca un aumento de la presión de llenado del ventrículo izquierdo (VI), afectando así las propiedades diastólicas del corazón, ya comprometidas, lo que resulta en una mayor reducción de la velocidad de llenado del VI. La poscarga es inversamente proporcional al volumen sistólico (VS ≈ 1/poscarga), por lo que un aumento de la poscarga debería resultar en una disminución del VS y de la fracción de eyección (FE). Sin embargo, en corazones sanos, a pesar del aumento de la tensión de la pared debido a la poscarga, el acortamiento normal de las fibras se logra mediante un aumento compensatorio de la contractilidad. En caso de disfunción del VI, el aumento de la poscarga no se tolera, el acortamiento de la longitud de las fibras se ve afectado y se produce una disminución de la FE.
Finalmente, recuerde lo siguiente:
✅Poscarga ↑ → Presión telediastólica del ventrículo izquierdo (PTDVI) ↑,
✅Poscarga ↑ → Volumen telesistólico del ventrículo izquierdo (VTSVI) ↑ y Volumen sistólico (VS) ↓ (en personas sanas, el VS puede mantenerse debido a un aumento de la contractilidad),
✅Poscarga ↓ → PTDVI ↓ y Diámetro telediastólico del ventrículo izquierdo (DTDVI) ↓.
Según la ley de Laplace:
✅Poscarga ↓ → Presión telediastólica del ventrículo izquierdo (PTDVI) ↓ → Estrés diastólico de la pared ↓ → Requerimiento de O2 ↓ → Diámetro telediastólico del ventrículo izquierdo (DTDVI) ↓,
✅Dilatación del ventrículo izquierdo → Estrés/tensión de la pared ↑ → Poscarga ↑,
✅Disminución de la PTDVI → Disminución de la poscarga (la implicación es inevitable y concuerda con la ley de Laplace),
✅Disminución de la impedancia aórtica (poscarga ventricular) → Disminución del estrés sistólico de la pared, y viceversa.
Contractilidad
Definición
La contractilidad se define como la capacidad inherente del miocardio para contraerse independientemente de las variaciones en la precarga y la poscarga. Esta capacidad de fuerza intrínseca de contracción se denomina contractilidad o inotropismo.
Braunwald escribe: «Los cambios en el rendimiento cardíaco, independientemente de las alteraciones en la precarga y la poscarga, son causados por la contractilidad. Es necesario distinguirla de los cambios en el rendimiento debidos a una variación en las condiciones de carga».
El tono simpático desempeña un papel importante en la regulación de la contractilidad. El efecto inotrópico positivo del aumento del tono simpático permite al corazón, sin que se produzca un cambio en el llenado diastólico (sin que se produzca un cambio en la precarga), expulsar un volumen sistólico (VS) mayor o mantener el VS en caso de aumento de la poscarga o de la resistencia a la eyección. Kumar observó en voluntarios sanos que el aumento del VS debido a la sobrecarga de volumen se debe principalmente a un aumento de la contractilidad y solo en menor medida al mecanismo de Frank-Starling, confirmando así resultados previos. Debido al aumento de la contractilidad «intrínseca», el volumen telesistólico disminuirá.
Medición y cuantificación
Es muy difícil medir y expresar la contractilidad como un parámetro único e independiente. A nivel del sarcómero, la contractilidad y la carga están interrelacionadas; por lo tanto, no son variables independientes. Cualquier parámetro que intente caracterizar la contractilidad «verdadera» debe ser independiente de los cambios en la precarga y la poscarga, el tamaño y la geometría del ventrículo izquierdo (VI) y la presión del VI.
La tasa de aumento de la presión intraventricular del VI, dp/dt, un índice de la fase isovolumétrica de la contracción, se correlaciona bien con la contractilidad del VI. Se espera que el valor máximo de dp/dt, denominado dp/dtmax, durante la sístole sea proporcional a la contractilidad. El dp/dtmax es sensible a la precarga, pero no a la poscarga, ya que se mide antes de la apertura de la válvula aórtica.
El dp/dtmax muestra una sensibilidad razonablemente buena para detectar y expresar cambios en el estado inotrópico «verdadero» (contractilidad intrínseca). Es el parámetro más valioso para medir y expresar la inotropía y actualmente constituye el estándar de referencia para representar la contractilidad «verdadera» (intrínseca).
Las condiciones contráctiles del ventrículo están influenciadas por sus propiedades intrínsecas al final de la sístole: la elastancia de la cavidad (Ees). Estas propiedades contráctiles del ventrículo pueden cuantificarse mediante la relación entre la presión telesistólica del ventrículo izquierdo (LVESP) y el volumen telesistólico del ventrículo izquierdo (LVESV).
La relación presión-volumen ventricular al final de la sístole es lineal (al menos en condiciones fisiológicas) y su pendiente, Ees, cuantifica las propiedades contráctiles ventriculares (sistólicas) (Fig. 7).
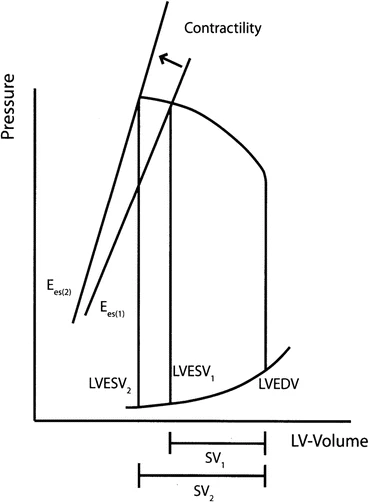
Ees se define como LVESP dividido por LVESV, por lo tanto
La Ees es prácticamente independiente de la carga, y Kass descubrió que, en un amplio rango de carga, la Ees es un potente indicador de la contractilidad real del ventrículo izquierdo (VI).
Al describir las propiedades sistólicas del corazón, debemos diferenciar entre los índices que se refieren a la contractilidad «real» y otros parámetros que describen la función sistólica del músculo cardíaco o el rendimiento cardíaco. Estos dos últimos son menos independientes que los demás índices y caracterizan la función cardíaca de forma más «global».
El rendimiento sistólico del VI se caracteriza por el trabajo sistólico, teniendo en cuenta que el corazón debe generar presión y flujo (volumen sistólico).
Valores normales: 58–104 gm−1 m2.
El rendimiento sistólico está influenciado por la carga y la configuración ventricular; por lo tanto, no es lo mismo que la contractilidad. En consecuencia, puede existir un rendimiento anormal aunque la contractilidad sea normal (p. ej., en caso de poscarga elevada) y viceversa, el rendimiento puede ser normal aunque la contractilidad esté alterada (p. ej., sepsis, insuficiencia mitral).
Mientras que el trabajo cardíaco describe la transferencia de energía de la contracción cardíaca al desarrollo del flujo sanguíneo, la potencia cardíaca de salida (PCS) describe la cantidad de energía generada por el corazón que recibe toda la vasculatura sistémica a nivel de la raíz aórtica. Por lo tanto, caracteriza la reserva reclutable aún disponible en caso de insuficiencia cardíaca aguda o shock para mantener la perfusión de los órganos vitales y, por consiguiente, refleja la gravedad de la enfermedad del paciente. La PCS ha demostrado un importante valor pronóstico en todo el espectro de síndromes de insuficiencia cardíaca aguda y, en particular, en el shock cardiogénico. La PCS se define como
y sigue las leyes físicas de los fluidos. Reflejando la función esencial del corazón (generar presión y flujo), la CPO es una medida del bombeo cardíaco que combina los dominios de presión y flujo.
Además, la CPO y su índice, el IPC, han demostrado ser superiores en la determinación del diagnóstico exacto del síndrome de insuficiencia cardíaca real en comparación con el IC, la PA, la PCP y su combinación. Si bien las medidas hemodinámicas tradicionales y sus supuestos valores objetivo utilizados en los protocolos de tratamiento han sido engañosos, tampoco han mostrado ningún efecto relevante cuando la terapia se ajustaba al alcanzar dichos valores.
La CPO parece ser un mejor parámetro que el IPC para predecir el pronóstico. El ajuste de la CPO según el tamaño corporal, que da como resultado el IPC, mostró una asociación más débil con la mortalidad. Una CPO ≤ 0,53 predice con mayor precisión una alta probabilidad de mortalidad intrahospitalaria.
Tradicionalmente, el SVI y el SWI se utilizaban como potentes predictores de mortalidad a corto plazo en el choque cardiogénico que complica el IAM, pero actualmente se considera preferible el uso de la CPO.
La función sistólica del ventrículo izquierdo (VI) puede describirse de diversas maneras, pero la fracción de eyección (FE, %) sigue siendo el parámetro más utilizado. La FE está determinada por la interacción de las propiedades arteriales y ventriculares y depende de la poscarga, por lo que no está regida exclusivamente por el VI.
Sin embargo,
Por lo tanto, la FE puede considerarse un buen parámetro de acoplamiento, que describe aspectos fundamentales del acoplamiento ventrículo-arterial más que la contractilidad.
La FE dista mucho de ser un parámetro ideal para evaluar la contractilidad. Depende tanto de la poscarga como de la precarga y del volumen o masa cardíaca.
La FE no detectará:
✅el exceso de poscarga (FE reducida aunque la contractilidad sea normal),
✅en caso de precarga aumentada (p. ej., insuficiencia mitral), la FE sobreestimará la función sistólica, pasando por alto la disfunción miocárdica,
✅en la hipertrofia ventricular izquierda concéntrica, la medición de la FE indica una función sistólica normal, aunque puede existir una disfunción sustancial.
Los valores normales son FE > 55%; una FE > 40% se considera razonable.
A pesar de sus limitaciones, Braunwald y Gillebert afirman que la FE es el mejor parámetro para describir la contractilidad global en comparación con todos los demás que se utilizan actualmente.
La contractilidad ventricular izquierda «verdadera» se expresa mejor mediante:
✅v dp/dtmax (mmHg/s), valores normales: 1400–2200
✅Ees (mmHg/mL), valor normal: aproximadamente 2,0.
Un valor de Ees <1 mmHg/mL se observa en corazones dilatados e insuficientes; en caso de hipertrofia, se produce un aumento significativo, hasta 4 mmHg/mL.
Cabe destacar que el índice cardíaco (IC) no es un indicador de contractilidad, sino una medida del flujo cardiovascular: el IC se ve afectado por la contractilidad, la rigidez y la resistencia vascular, el volumen intravascular y las presiones de llenado. Además, no existe un índice de gasto cardíaco (GC)/IC normal, ya que las demandas metabólicas pueden variar considerablemente.
Medicamentos inotrópicos
Los fármacos capaces de aumentar la contractilidad miocárdica se denominan inotrópicos. En los últimos años, la administración de fármacos inotrópicos se ha visto ensombrecida por la creciente evidencia de efectos adversos y un aumento de la mortalidad, especialmente cuando se administran a pacientes con una función ventricular izquierda razonablemente conservada (FE > 40%). Conners y Sandham observaron un aumento significativo de la mortalidad cuando pacientes clínicamente estables fueron tratados con agentes inotrópicos convencionales debido a un gasto cardíaco numéricamente bajo. Solo los pacientes que requieren soporte inotrópico de forma absoluta debido a un gasto cardíaco bajo como consecuencia de una contractilidad gravemente comprometida y que son resistentes a otros tratamientos deben ser tratados con estos fármacos.
La Sociedad Europea de Cardiología (ESC) recomienda los agentes inotrópicos en síndromes de insuficiencia cardíaca cuando la enfermedad se ha deteriorado hasta poner en peligro la vida y la situación depende críticamente de la hemodinámica: «Los agentes inotrópicos están indicados en presencia de hipoperfusión periférica con o sin congestión o edema pulmonar refractario a diuréticos y vasodilatadores en dosis óptimas».
Frecuencia cardíaca y contractilidad
A finales del siglo XIX, Bowditch publicó su observación de que la fuerza de contracción cardíaca aumenta —hasta cierto límite— con el incremento de la frecuencia cardíaca.
La fuerza isométrica máxima aumenta con la frecuencia cardíaca. Esto se debe a que el calcio se acumula en los miocitos cuando la diástole se acorta (lo cual ocurre con el aumento de la frecuencia cardíaca). En el caso de un corazón comprometido o con insuficiencia cardíaca, este efecto se atenúa, o incluso puede ocurrir lo contrario: con el aumento de la frecuencia cardíaca, la fuerza de contracción disminuye. Cuando la taquicardia supera los 130 latidos/min, la gravedad del daño miocárdico se correlaciona con la magnitud de la taquicardia. Además, la taquicardia siempre precede a una caída de la presión arterial.
Por lo tanto, en el caso de taquicardia en un corazón comprometido, la reducción de la frecuencia cardíaca aumentará la contracción cardíaca y, por consiguiente, el volumen sistólico (presión arterial media y perfusión orgánica).
En pacientes con insuficiencia cardíaca que desarrollan o padecen fibrilación auricular, una frecuencia cardíaca de 100-110 latidos por minuto es aceptable.
Interacción/Interdependencia Ventricular Diastólica (IVD)
Definición
El ventrículo derecho e izquierdo están estrechamente interrelacionados anatómica y funcionalmente, ya que comparten el tabique interventricular (TIV), el pericardio y (por su continuidad) partes de las fibras miocárdicas. La interdependencia ventricular caracteriza la “respuesta de un ventrículo a los cambios de presión y volumen del otro” (Elzinga et al.). Sin embargo, las interacciones incluyen aún más características, ya que se refieren a los cambios de tamaño (volumen), forma, presión y (concomitantemente) distensibilidad de un ventrículo debido a un impacto mecánico directo y predominante (independiente de los efectos neurohormonales y circulatorios) sobre el otro, y además a una contribución sistólica del VI al rendimiento contráctil del VD. En consecuencia, la interacción ventricular diastólica se refiere principalmente a la competencia de los dos ventrículos por el espacio dentro del saco pericárdico no distensible, es decir, cuando el VD se dilata, y la interacción ventricular sistólica se aplica a la contribución del VI al rendimiento sistólico del VD. El impacto puede ser incluso drástico en caso de cambios agudos en el tamaño y la presión del ventrículo derecho.
Estas interacciones diastólicas están mediadas por las estructuras compartidas de ambos ventrículos: el tabique interventricular y el pericardio. El pericardio ejerce un efecto restrictivo sobre el llenado ventricular debido a su escasa distensibilidad y a su capacidad de transmisión de presión. La interacción mediada por el tabique y el pericardio se denomina interacción «directa», en comparación con la llamada interacción «en serie», que se refiere simplemente a la relación física entre los dos ventrículos y sus salidas: los dos ventrículos están acoplados en serie, uno tras otro, por lo que su salida necesariamente debe ser igual a lo largo del tiempo.
Presión septal y transseptal
En condiciones fisiológicas, la forma del tabique es cóncava cuando se observa desde el lado del ventrículo izquierdo. No hay diferencias entre la sístole y la diástole, debido a que la presión diastólica final del ventrículo izquierdo (LVEDP) siempre es superior a la del ventrículo derecho (RVEDP) y aumenta proporcionalmente durante la sístole. Kingma demostró que la posición del tabique viene determinada por el gradiente de presión diastólica final entre el ventrículo izquierdo y el ventrículo derecho:
En caso de enfermedad, la posición del tabique interventricular puede variar notablemente debido a cambios en el gradiente de presión, lo que altera sustancialmente los volúmenes telediastólicos. En la sobrecarga aguda de presión o volumen del ventrículo derecho (VD), Kingma demostró que el tabique interventricular se aplana o incluso se vuelve convexo al final de la diástole debido a la dilatación del VD y al aumento de la presión telediastólica del ventrículo derecho (PTDVD), lo que disminuye el gradiente de presión transeptal y empuja el tabique hacia el ventrículo izquierdo. Numerosas publicaciones confirman el cambio en la posición del tabique en diversas enfermedades, como la hipertensión pulmonar aguda y crónica, la insuficiencia cardíaca congestiva y la ventilación mecánica.
Este desplazamiento del tabique hacia la izquierda contribuye significativamente a la reducción del llenado del ventrículo izquierdo (VI); por lo tanto, el volumen total del VI y el volumen telediastólico disminuyen, y el volumen sistólico (VS) se reduce como consecuencia.
El pericardio, con muy poca distensibilidad, contribuye a este proceso ejerciendo una restricción que limita la variación del volumen cardíaco total.
Pericardio
Todas las cavidades cardíacas (excepto la parte posterior de la aurícula izquierda, donde desembocan las venas pulmonares) están rodeadas por el pericardio. Este actúa como una banda tensa e inflexible alrededor del eje menor del corazón, fijando su área transversal y provocando una interacción ventricular directa.
Por lo tanto, un aumento en el área transversal de un ventrículo, por ejemplo, debido a una sobrecarga de volumen o a una dilatación, reduce necesariamente el área del ventrículo opuesto, que tiene menor potencial de llenado, lo que provoca un aumento de la presión pericárdica y altera la presión transmural. El volumen cardíaco total permanece inalterado.
El aumento de las presiones en el espacio pericárdico ejerce un efecto restrictivo progresivo sobre el llenado ventricular, denominado restricción pericárdica. Cuando el pericardio se distiende debido a la dilatación de los ventrículos, como en la insuficiencia cardíaca crónica o por sobrecarga de volumen, el llenado —en particular el del ventrículo izquierdo— se ve significativamente restringido. Con un mayor estiramiento, el pericardio se vuelve aún menos distensible y, especialmente en casos de cambios agudos, su efecto restrictivo desempeña un papel fundamental en las condiciones de carga. En estas condiciones, la presión pericárdica (PP) aumenta progresivamente y restringe significativamente el llenado. La PP aumenta de forma exponencial y, una vez que el pericardio se sobreestira, se observa un aumento exponencial de la presión telediastólica del ventrículo izquierdo (PTDVI).
El aumento de la presión intratorácica, por ejemplo, debido a un aumento de la presión intraabdominal, una infección torácica, etc., afectará, como consecuencia de una mayor restricción sobre el ventrículo derecho (VD) de paredes delgadas, a la PTDVI más que a la PTDVI (el aumento de la PTDVI es mayor que el de la PTDVI). Por lo tanto, la PTDVI transmural (= PTDVI − PAD/PVC) disminuirá con un menor volumen telediastólico del ventrículo izquierdo (VTDVI) y una menor distensión de las fibras telediastólicas del ventrículo izquierdo, lo que resultará en una reducción del volumen sistólico (VS).
La interacción ventricular debida a la restricción pericárdica disminuye mientras la presión de pulso sea <5 mmHg; cuando supera los 9-10 mmHg, el pericardio ejerce una restricción significativa sobre el llenado ventricular. Además, cuando la presión telediastólica del ventrículo izquierdo intraventricular supera los 10(12)-15 mmHg, la relación entre la presión telediastólica del ventrículo izquierdo y el volumen telediastólico del ventrículo izquierdo se vuelve mucho más pronunciada y el pericardio limita los aumentos adicionales del volumen ventricular izquierdo.
Hipertensión pulmonar y riesgo de DVI
En la hipertensión pulmonar, se ha demostrado que la administración de líquidos aumenta la presión telediastólica del ventrículo derecho (PTDVD) más que la del ventrículo izquierdo (PTDVI). El aumento concomitante (junto con la PTDVD) de la presión pericárdica superará el aumento de la PTDVI (debido a un mayor aumento de la PTDVD en comparación con la PTDVI), por lo que la PTDVI transmural y, por lo tanto, la precarga del ventrículo izquierdo se reducirán debido a la restricción pericárdica (Fig. 8).
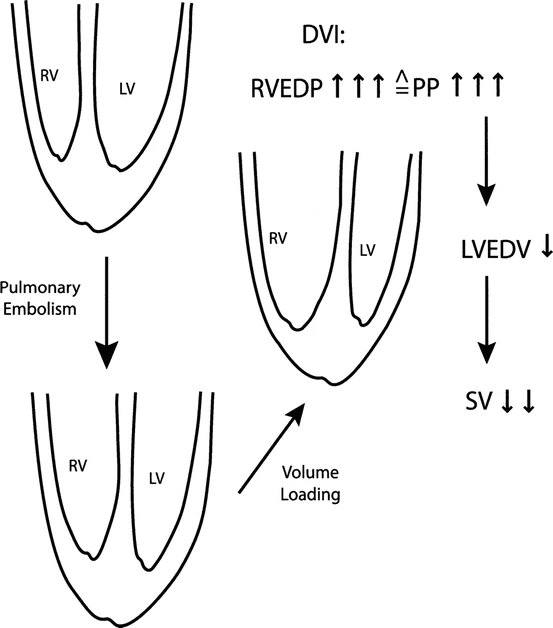
Administración de líquidos en la hipertensión pulmonar
(Un efecto adicional se producirá por el desplazamiento hacia la izquierda del tabique, reduciendo el área del ventrículo izquierdo y, por lo tanto, el volumen telediastólico del ventrículo izquierdo).
Insuficiencia cardíaca congestiva crónica (izquierda o biventricular) con exacerbación aguda
Una exacerbación aguda de la insuficiencia cardíaca congestiva crónica suele ser crucial en la evolución de la enfermedad y puede ser el desenlace de una enfermedad crítica. En esta situación, la disfunción ventricular derecha (DVI) puede tener un impacto sustancial en la hemodinámica y debe considerarse en el tratamiento.
Un aumento repentino de la poscarga del ventrículo derecho (VD) o de la impedancia de salida del VD, por ejemplo, debido a una embolia pulmonar (EP) o una pérdida de contractilidad (por ejemplo, debido a un infarto agudo de miocardio del VD), siempre provocará dilatación del VD, una disminución de la fracción de eyección del VD (FEVD) y un aumento sustancial de la presión telediastólica del VD (PTDVD). Esto implica un aumento considerable de la presión de pulso (PP) y un desplazamiento hacia la izquierda del septo, lo que compromete el llenado del ventrículo izquierdo (VI).
Atherton demostró que, en pacientes con insuficiencia cardíaca congestiva crónica y una presión telediastólica del ventrículo izquierdo (PTDVI) elevada (que causa hipertensión venosa pulmonar), el llenado del ventrículo izquierdo se veía notablemente impedido debido a la interacción diastólica ventricular directa a través del septo y a la distensión del pericardio (restricción pericárdica). La descarga de volumen resultó, como era de esperar, en una reducción del volumen telediastólico del ventrículo derecho (VTDVD), pero el VTDVI aumentó paradójicamente (véase la figura 9).
En casi el 50 % de los pacientes con insuficiencia cardíaca congestiva, la restricción pericárdica desempeña un papel importante y la descarga de volumen conduce a una mejora del rendimiento cardíaco. Incluso cuando la restricción pericárdica es menor, como en el otro 50 % de los pacientes estudiados por Atherton, la reducción del VTDVI secundaria a la descarga de volumen no comprometió significativamente la situación hemodinámica.
Estos resultados concuerdan con los hallazgos de Dupuis, quien demostró que una reducción de la presión capilar pulmonar en cuña (PCPW) en pacientes con insuficiencia cardíaca congestiva resultó en un aumento del volumen sistólico (VS) y del volumen sistólico (VS), incluso cuando la PTDVI disminuyó. En 1986, Stevenson demostró que la descarga de volumen en pacientes con insuficiencia cardíaca congestiva grave y altas presiones de llenado mostraba claros beneficios, con una mejoría en el pronóstico clínico a corto y largo plazo.
Moore exploró los mecanismos fisiopatológicos subyacentes y estableció nuestro enfoque terapéutico actual. En pacientes con insuficiencia cardíaca congestiva y, por lo tanto, hipertensión pulmonar secundaria, la interacción diastólica ventricular directa desempeña un papel fundamental en la disfunción del ventrículo izquierdo responsable de la reducción del volumen sistólico del ventrículo izquierdo. El enfoque habitual de administrar volumen a un paciente con hipotensión arterial, en casos de insuficiencia cardíaca crónica descompensada agudamente, empeora la situación hemodinámica y clínica. La descarga de volumen estabiliza la situación (Fig. 9).
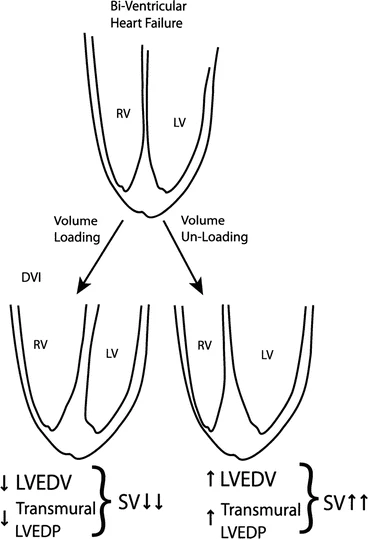
Fisiopatología de la insuficiencia cardíaca congestiva crónica:
La elevación de la presión telediastólica del ventrículo derecho (PTDVD) se debe a la restricción pericárdica según la regla del volumen cardíaco total [488, 490] y/o a un aumento crónico de la poscarga del ventrículo derecho (hipertensión pulmonar causada por un aumento de la PTDVD). Además, una poscarga del ventrículo derecho elevada o una mayor impedancia de salida del ventrículo derecho, como la que se observa en la hipertensión pulmonar debida a una PTDVD elevada, siempre inducirá dilatación del ventrículo derecho, y por lo tanto, un aumento del diámetro telediastólico del ventrículo derecho (DTDVD) y del volumen telediastólico del ventrículo derecho (VTDVD).
Por lo tanto: un aumento progresivo de la PTDVD y un aumento progresivo de los DTDVD y VTDVD conllevan un aumento progresivo de la presión pericárdica (PP).
Sin embargo, como resultado de los cambios de volumen y presión, el tabique interventricular se desplazará a una posición intermedia entre los ventrículos, más hacia la izquierda de lo que es fisiológicamente normal.
Si se proporciona el volumen en esta situación:
1. gradiente de presión transseptal ahora ↓, y por lo tanto desplazamiento hacia la izquierda de la
2. Debido a un aumento paralelo de la PP con la RVEDP, la restricción pericárdica impedirá cada vez más el llenado del LV:
La descarga es el tratamiento de elección (nitroglicerina, diuréticos):
1. El gradiente de presión transeptal aumenta, por lo tanto, el tabique se desplaza hacia la derecha →
2. Menor restricción pericárdica del ventrículo izquierdo debido a ↓ PP →
Aunque el corazón se descarga, el volumen sistólico (VS) aumenta: esto se conoce como el «aumento paradójico» del VS.
(Como puede observarse, el término «VI-VS ↑» siempre se encuentra en el extremo derecho y siempre uno debajo del otro).
Resumen simplificado del proceso de descarga:
Es importante recordar que se encontró evidencia de DVI hemodinámicamente significativa en el 50% de todos los pacientes con insuficiencia cardíaca congestiva, e incluso si no hay una DVI relevante, la descarga redujo el LVEDV solo marginalmente y no comprometió la situación hemodinámica (sin caída de la presión arterial). Por lo tanto, todos los pacientes con insuficiencia cardíaca congestiva crónica descompensada aguda deben ser tratados con descarga de volumen.
Conclusiones
La interacción ventricular tiene un impacto considerable en la situación hemodinámica, especialmente en pacientes críticos con compromiso circulatorio. Las circunstancias que sugieren una interacción ventricular significativa son la combinación de hipertensión pulmonar (HP) y presión venosa central (PVC) elevada, sobre todo en casos de disfunción o insuficiencia cardíaca derecha, lo que siempre implica un aumento de la presión de pulso (PP).
Ejemplos:
✅embolia pulmonar aguda,
✅insuficiencia cardíaca derecha aguda (infarto agudo de miocardio del ventrículo derecho, síndrome de dificultad respiratoria aguda, sepsis),
✅exacerbación de la disfunción ventricular derecha crónica (EPOC con exacerbación aguda),
✅insuficiencia cardíaca congestiva crónica con dilatación del ventrículo izquierdo, especialmente en casos con presión telediastólica del ventrículo izquierdo (PTDVI) elevada,
✅intubación y ventilación mecánica, en particular en pacientes con hipertensión pulmonar aguda o crónica,
✅la presión positiva al final de la espiración (PEEP) afecta al corazón de la misma manera que el taponamiento cardíaco. Cuando se detectó una PEEP >12 mm H2O, una sobrecarga de presión del ventrículo derecho (PVDR ↑) y un desplazamiento del tabique interventricular,
✅otras causas de un aumento considerable de la presión intratorácica, como una infección torácica grave, un neumotórax a tensión y un aumento de la presión intraabdominal, como en el caso de una infección abdominal grave, ascitis o síndrome compartimental abdominal, influyen en el tratamiento.
Todo lo anterior repercute en el tratamiento potencial, y su consideración debería modificar significativamente nuestra práctica clínica diaria.
La sobrecarga de volumen ya no se recomienda en la disfunción/insuficiencia aguda del ventrículo derecho, y la sobrecarga de volumen debida a hipotensión en la insuficiencia cardíaca congestiva descompensada aguda conlleva un riesgo muy elevado de empeoramiento de la situación; por lo tanto, la descarga de volumen es el enfoque de elección.