La regeneración cardíaca se refiere al proceso de reparación del corazón tras una lesión mediante la repoblación de tipos celulares específicos para reemplazar el tejido dañado y recuperar su capacidad funcional. Si bien existía evidencia creíble de este fenómeno en vertebrados inferiores, la creencia en el potencial de regeneración cardíaca en mamíferos es un desarrollo reciente. Anteriormente se creía que el corazón era un órgano «posmitótico» cuya célula principal, el cardiomiocito, era incapaz de dividirse. En las últimas dos décadas, la reputación del corazón cambió drásticamente, pasando de ser un órgano posmitótico a uno altamente proliferativo y, más recientemente, a un órgano con una capacidad de recambio modesta. Estas visiones opuestas sobre el recambio celular en el corazón de los mamíferos generaron una serie de estudios fascinantes y precisos que aportan información novedosa y significativa sobre la regeneración cardíaca. De hecho, ahora contamos con evidencia rigurosa de que el corazón de los mamíferos adultos es capaz de una baja tasa de recambio a lo largo de la vida, con un período notable de potencial regenerativo completo restringido al período neonatal temprano. En este capítulo, describiremos la cardiomiogénesis fisiológica y patológica que se produce en los mamíferos y analizaremos diferentes clases de terapias experimentales con potencial para estimular la regeneración cardíaca en el corazón adulto.
El corazón postnatal no es un órgano postmitótico
Los fundamentos de la idea de que el corazón es un órgano estático incapaz de regenerarse se establecieron a mediados de la década de 1920. Una publicación importante de 1925 afirmaba que las figuras mitóticas no son detectables en los cardiomiocitos humanos,¹ que, por lo tanto, se consideraban células retiradas irreversiblemente del ciclo celular: este estudio introdujo de hecho el concepto de que el corazón es un órgano terminalmente diferenciado y posmitótico.
La idea de que la reserva de miocitos presente al nacer es irremplazable durante la vida del organismo se vio reforzada por una serie de estudios autorradiográficos realizados en la década de 1960, en los que se administró timidina tritiada al miocardio durante el desarrollo posnatal y la sobrecarga patológica para cuantificar la replicación del ADN. El grado de síntesis de ADN en los núcleos de los miocitos fue insignificante, por lo que el aumento del tamaño del corazón que se produce con la edad se correlacionó con el crecimiento del tamaño de los cardiomiocitos debido al aumento del volumen celular (es decir, se pensó que la hipertrofia, en lugar de la hiperplasia, era el mecanismo predominante para el aumento posnatal del peso del corazón).
A finales de la década de 1990 y principios de la de 2000, una serie de publicaciones muy difundidas del grupo de Piero Anversa desafió directamente el dogma del corazón como órgano posmitótico. Evaluaron corazones de pacientes que fallecieron pocos días después de un infarto de miocardio (IM) (así como corazones de control) y observaron la expresión de Ki-67, un antígeno nuclear asociado al ciclo celular, en la zona limítrofe del infarto y en las zonas distantes. Encontraron evidencia putativa de husos mitóticos, formación de anillos contráctiles, cariocinesis y citocinesis en cortes de tejido mediante inmunofluorescencia en corazones lesionados. A partir de estas observaciones, concluyeron que existe un potencial cardiomiogénico significativo en el corazón humano y que «la regeneración de miocitos puede ser un componente crítico del aumento de la masa muscular del miocardio». Este informe impulsó una intensa investigación para caracterizar con mayor detalle el crecimiento cardíaco posnatal y planteó importantes interrogantes sobre la célula progenitora de origen de los nuevos cardiomiocitos. Sin embargo, otro estudio planteó dudas sobre el uso de Ki-67 para demostrar la división celular, ya que mostró que la expresión de Ki-67 después de la MI humana puede deberse a la poliploidización en lugar de a una mitosis genuina.
En informes posteriores, el grupo de Anversa afirmó de forma provocativa que, en promedio, se generaban un 22 % de miocitos nuevos cada año en humanos, lo que sugiere una vida útil de 4,5 años para este tipo celular. Sin embargo, los esfuerzos independientes por replicar estos resultados mediante diferentes técnicas no lograron corroborar este grado de recambio de cardiomiocitos. En los últimos años, el análisis clonal y los métodos de marcaje con radioisótopos han proporcionado los datos más fiables sobre el crecimiento cardíaco y su dinámica tras el nacimiento en mamíferos. Actualmente se cree que el corazón de los mamíferos experimenta una tasa de recambio muy baja —aunque no nula— mediada por cardiomiocitos preexistentes, con un posible pequeño aumento de la cardiomiogénesis tras un infarto de miocardio, con un impacto clínico secundario.
Fuentes de controversia en la proliferación de cardiomiocitos en mamíferos posnatales
Para comprender la base de los resultados contradictorios y la amplia gama de tasas de proliferación de miocitos en este campo, es importante entender el ciclo celular de los cardiomiocitos. La base fundamental de la controversia en este campo es el desacoplamiento de la síntesis de ADN, la división nuclear (cariocinesis) y la abscisión (citocinesis), que da lugar a células multinucleadas y poliploides, y que ocurre en los cardiomiocitos de mamíferos. Esto dificulta la interpretación de los ensayos tradicionales de recambio celular basados en la replicación del ADN.
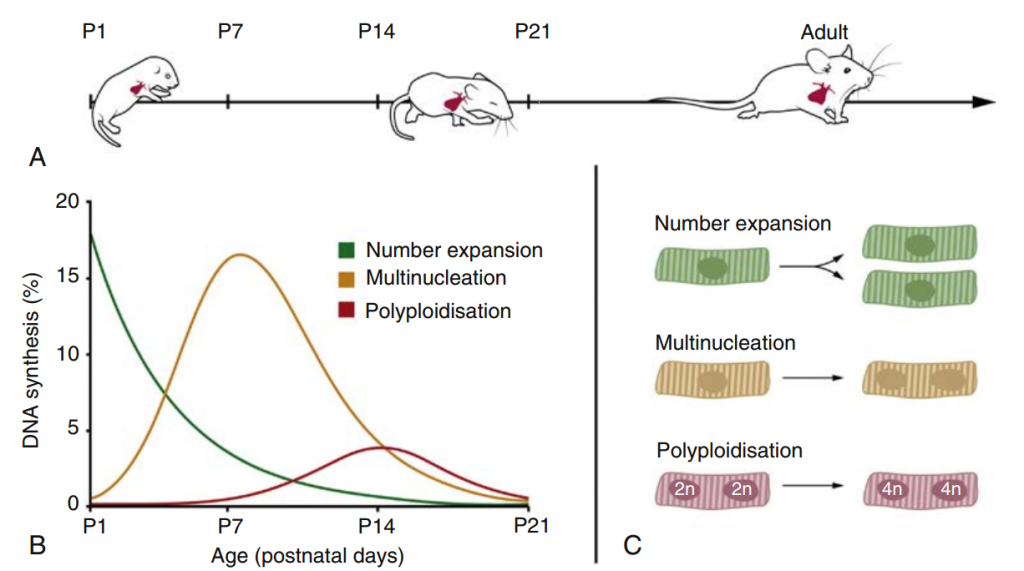
Hace casi 20 años, la administración de análogos de timidina a ratones reveló dos fases de síntesis de ADN temporalmente distintas que caracterizan el crecimiento prenatal y posnatal temprano del compartimento miocárdico. El primer pico de síntesis de ADN se observó en el corazón fetal y se atribuyó a la proliferación de cardiomiocitos. Por el contrario, la segunda fase de síntesis de ADN, detectada 4 días después del nacimiento, se produce principalmente por binucleación sin citocinesis. Estos hallazgos fundamentales se han reproducido numerosas veces utilizando otras metodologías para identificar núcleos en replicación en cardiomiocitos de roedores (Fig. 3.1). Estos hallazgos también ponen de manifiesto el reto de medir la renovación de los cardiomiocitos: no toda la síntesis de ADN da lugar a la citocinesis. De hecho, se observa una disminución progresiva en la tasa de proliferación de cardiomiocitos concomitantemente con un aumento en la síntesis de ADN. En ratones, alrededor del día postnatal 7 (P7) se observa un pico de binucleación en los cardiomiocitos, y alrededor del día P14, un pico de poliploidía (replicación del ADN sin división nuclear), lo que resulta en números de copias cromosómicas de 4n, 8n, 16n, etc. Estos resultados consistentes generan incertidumbre sobre cualquier método que se base exclusivamente en el ADN o la división nuclear como indicador de la división celular en los cardiomiocitos. Además, los marcadores de la fase S del ciclo celular pueden incorporarse durante la reparación del ADN, lo que puede dar lugar a una interpretación falsamente positiva. En definitiva, no existe ningún marcador de mitosis que confirme de forma concluyente que la citocinesis haya ocurrido o vaya a ocurrir: incluso las proteínas asociadas a la citocinesis pueden participar en otras fases del ciclo celular, lo que limita su utilidad para indicar específicamente la abscisión.
Otro factor que complica la interpretación de los ensayos de proliferación en cardiomiocitos es la dificultad para distinguir histológicamente los núcleos de los cardiomiocitos y otros tipos celulares en cortes de tejido. Metodologías sofisticadas como el rastreo de linaje y los modelos de ratón para el mapeo del destino celular han aportado información valiosa sobre la renovación posnatal de los cardiomiocitos, pero presentan limitaciones, como dudas sobre la fidelidad del promotor, la expresión ineficiente del gen reportero y la fusión o transferencia celular de las proteínas reporteras.
En conjunto, estas importantes limitaciones dificultan el uso de ensayos rutinarios para confirmar o cuantificar la mitosis de los cardiomiocitos. Por ello, se hizo imperativo que el campo de la biología cardiovascular recurriera a técnicas más rigurosas para demostrar la aparición de nuevos cardiomiocitos, como el uso de múltiples marcadores mitóticos y el análisis del tamaño y la cuantificación del número de células en un mismo estudio. Además, este campo ha recurrido cada vez más al análisis clonal, ya que permite determinar con precisión las relaciones entre progenitores y descendencia, y se basa en la finalización de la citocinesis. Sin embargo, este enfoque tan riguroso también presenta muchas de las limitaciones del mapeo del destino celular descritas anteriormente. Finalmente, los métodos basados en el marcaje con radioisótopos, combinados con modelos matemáticos sofisticados en ratones y humanos, respaldan los hallazgos del análisis clonal y nos han proporcionado los cálculos más meticulosos de la tasa de crecimiento cardíaco en mamíferos.
Evidencia de recambio de cardiomiocitos en el corazón adulto
Frisen y colaboradores utilizaron una metodología basada en el carbono-14 (¹⁴C) para calcular la tasa precisa de recambio de cardiomiocitos en el corazón humano en 2009. En resumen, obtuvieron muestras de corazón humano de autopsias y aislaron los núcleos de los cardiomiocitos mediante anticuerpos específicos. Posteriormente, determinaron retrospectivamente la fecha de nacimiento de los cardiomiocitos midiendo y correlacionando los niveles de ¹⁴C en el ADN genómico de los cardiomiocitos con los niveles atmosféricos de ¹⁴C. La característica disminución exponencial del ¹⁴C atmosférico tras el Tratado de Prohibición Parcial de Ensayos Nucleares de 1963 les permitió asignar una fecha a cada cardiomiocito. Su trabajo se basó en la premisa de que el nivel de ¹⁴C en el ADN de una célula permanece estable tras su última división celular y refleja la concentración de ¹⁴C en la atmósfera en el momento de dicha división. De este modo, el aumento y la disminución del 14C en la atmósfera terrestre, debido a las pruebas históricas de armas nucleares, facilitaron los cálculos precisos de la cinética de recambio de los cardiomiocitos en los seres humanos.
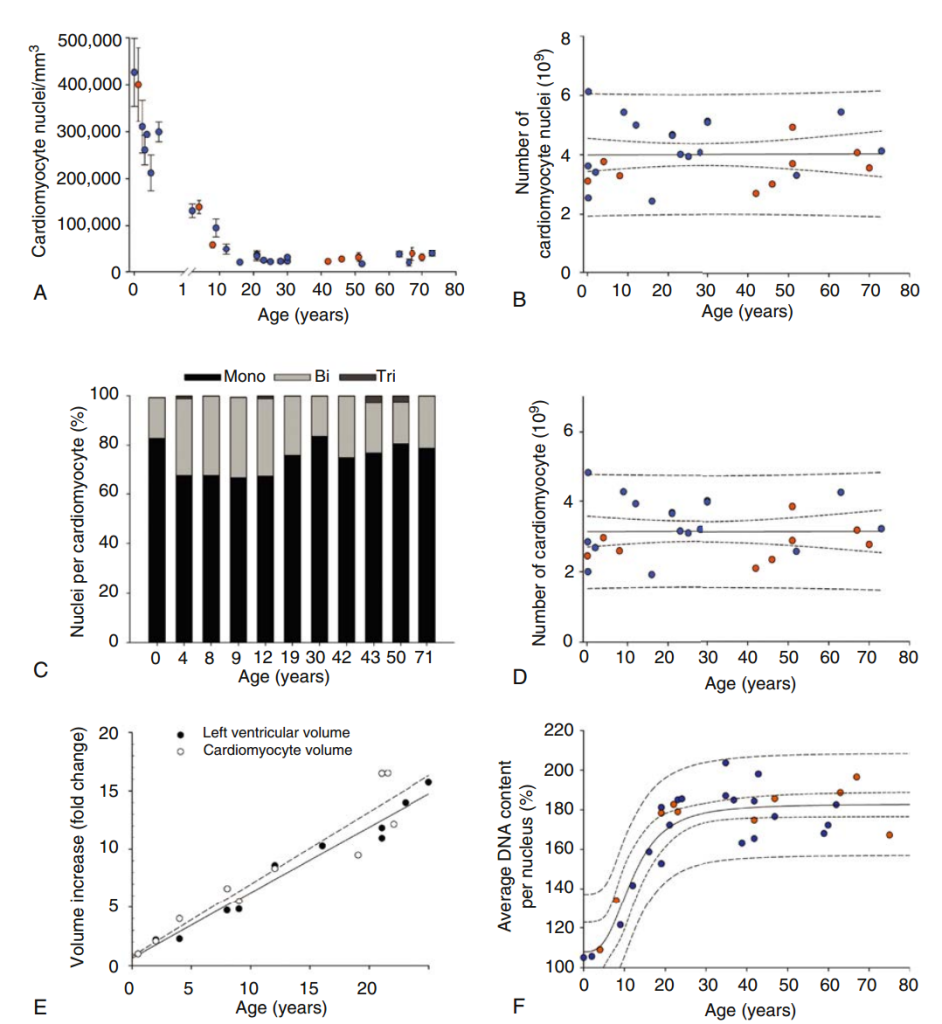
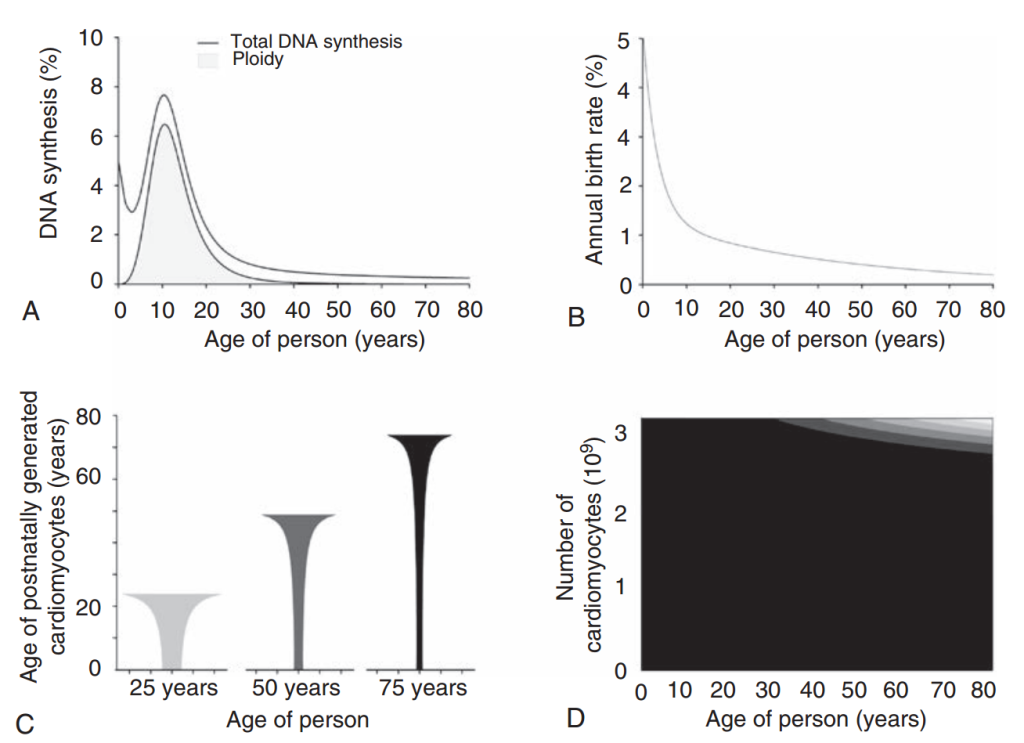
Estas mediciones con el radioisótopo 14C demostraron de forma convincente que el corazón no es un órgano posmitótico. Frisen y sus colegas mostraron que la tasa anual de nacimiento de cardiomiocitos en humanos es máxima durante la primera década de vida y, posteriormente, disminuye a menos del 1 % a lo largo de la misma. De hecho, el patrón es muy similar al observado en ratones (véase la figura 3.1B). Debido a las diferentes interpretaciones de los datos de 14C, Frisen y sus colaboradores realizaron un análisis estereológico adicional para validar aún más sus resultados. Obtuvieron tejido de 29 muestras humanas post mortem sin antecedentes ni evidencia de cardiopatía y midieron la cinética de proliferación de cardiomiocitos, células endoteliales y células mesenquimales en el corazón. Gracias al uso de la estereología, también pudieron medir el número total de células y el volumen celular en una muestra de tejido determinada. Confirmaron que el volumen de los cardiomiocitos aumenta con la edad (figura 3.2E), pero el número total de cardiomiocitos permanece relativamente constante (véase la figura 3.2B). Tras modelar la binucleación y la ploidía que se producen en las tres primeras décadas de vida (Fig. 3.3A; véase también la Fig. 3.2C), confirmaron sus hallazgos iniciales de que la tasa de proliferación de cardiomiocitos en humanos es inferior al 1 % después de los 10 años, y esta tasa sigue disminuyendo con la edad (véase la Fig. 3.3C). Además, investigaron las tasas de proliferación en regiones específicas del corazón y no encontraron diferencias en la cinética de renovación de cardiomiocitos entre las capas miocárdicas (p. ej., endocardio, miocardio, epicardio), zonas (p. ej., ápice, base) o cámaras, lo que contradice la existencia de una población progenitora específica de cada región.
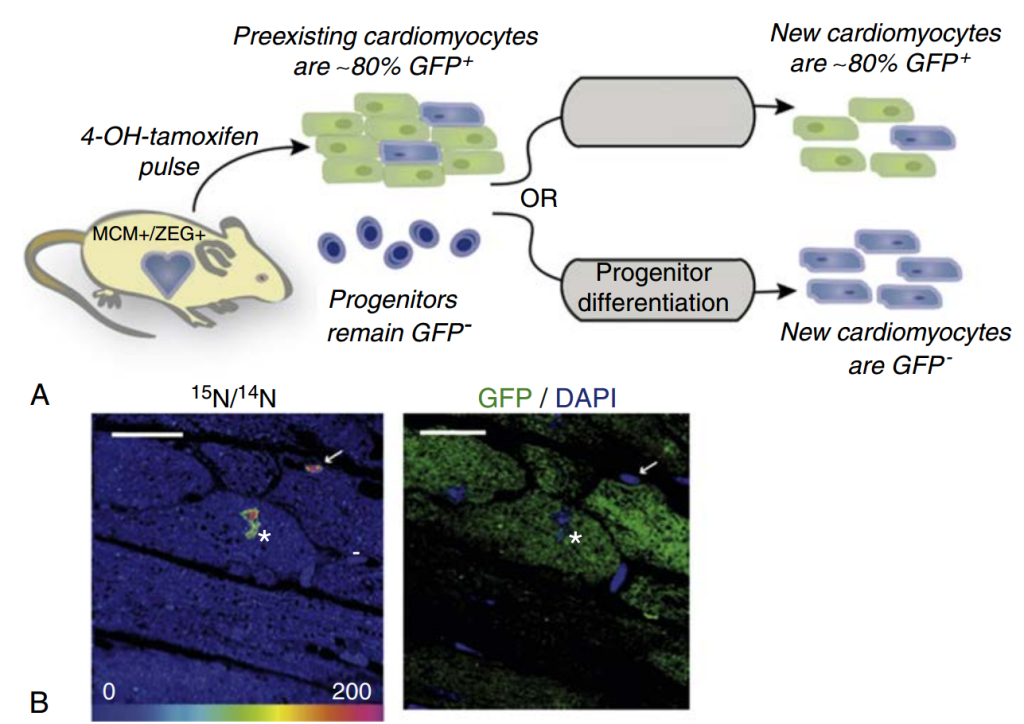
Senyo y sus colegas extendieron los hallazgos mencionados a ratones mediante la combinación del mapeo genético del destino celular con la espectrometría de masas de imágenes multiisotópicas (MIMS), que requiere la administración de [15N]timidina y es análoga a la técnica de marcaje radiactivo con 14C (Fig. 3.4). Calcularon una tasa anual de recambio de cardiomiocitos murinos a partir de cardiomiocitos preexistentes del 0,76 %. También observaron que, ocho semanas después de un infarto de miocardio en ratones adultos, el 3,2 % de los cardiomiocitos en la zona limítrofe del infarto se habían dividido. Sin embargo, al igual que en el trabajo de Frisen y colaboradores, es necesario hacer ciertas suposiciones sobre la fracción de síntesis de ADN que se produce debido a la multinucleación y la poliploidía, en contraposición a la finalización del ciclo celular mediante la abscisión. Por ejemplo, solo se consideraron como verdaderas células hijas recién nacidas los cardiomiocitos diploides mononucleares, mientras que se presumió que los cardiomiocitos poliploides o multinucleados con 15N nuclear eran el resultado de la síntesis de ADN sin citocinesis.
Si bien estos métodos analíticos basados en el marcaje con radioisótopos proporcionaron información detallada sobre la dinámica de renovación de los cardiomiocitos, que se corroboró en diversas especies de mamíferos, estas técnicas no pudieron demostrar la ontogenia de la cardiomiogénesis posnatal a nivel de célula individual. Dado que el origen de los nuevos cardiomiocitos era una cuestión clave en este campo, se utilizaron técnicas de mapeo del destino celular, tanto clonales como no clonales, para obtener una respuesta definitiva.
El modelo de “Análisis Mosaico de Marcadores Dobles” (MADM) es ideal para el estudio del corazón, ya que la recombinación Cre en células en replicación puede dar lugar a una herencia asimétrica de marcadores fluorescentes en las dos células hijas: un núcleo obtiene el gen tdTomato y el otro recibe el gen de la proteína verde fluorescente (GFP). Si no hay división nuclear ni citocinesis, la célula madre permanecerá doblemente positiva para las dos proteínas fluorescentes. Sin embargo, si la célula madre en división experimenta mitosis con citocinesis, las dos células hijas se volverán asimétricamente fluorescentes (Fig. 3.5A). Por lo tanto, la citocinesis es necesaria y suficiente para generar células con un solo marcador, y la relación de parentesco entre las células hijas puede determinarse gracias al marcaje asimétrico. Además, dado que el marcaje es indeleble, MADM permite el análisis clonal de las células hijas (es decir, la evaluación de la capacidad proliferativa de las células individuales a lo largo del tiempo).
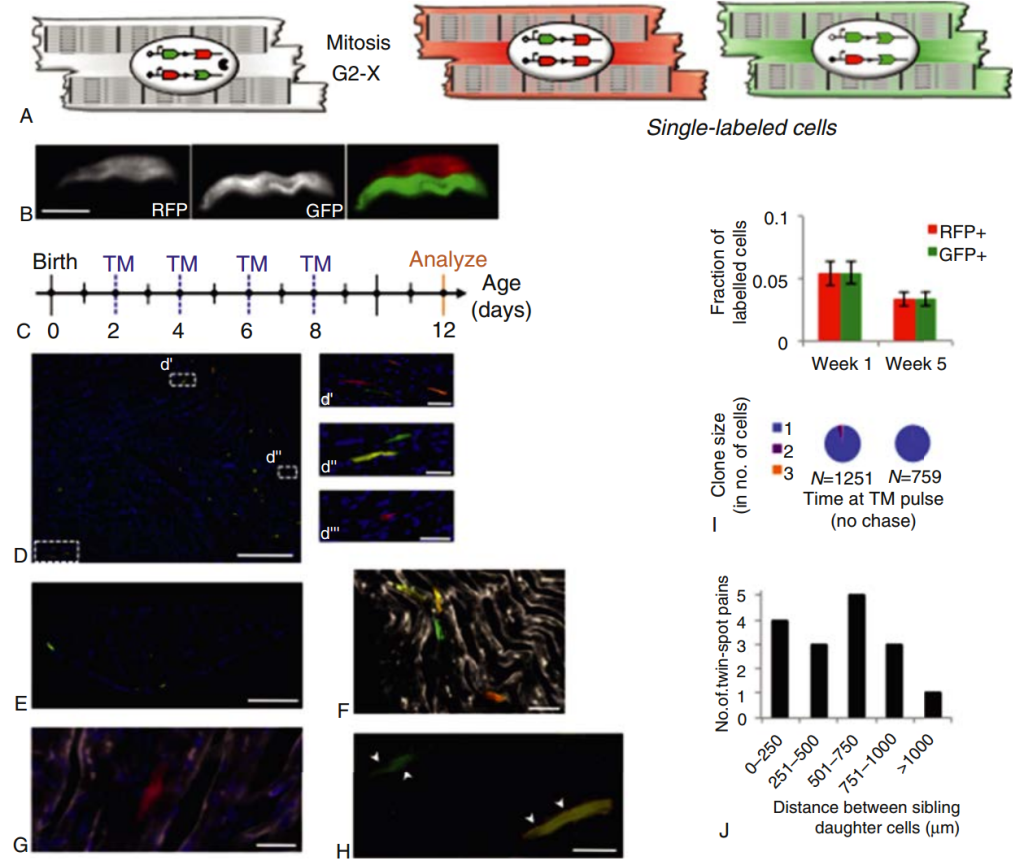
Utilizando MADM, Ali y colaboradores demostraron directamente que los cardiomiocitos existentes que expresan la proteína sarcomérica α-miosina cadena pesada son las células progenitoras de los cardiomiocitos neonatales posnatales (véase la figura 3.5). Los cardiomiocitos que se dividieron parecieron dividirse solo una vez durante el período analizado, lo que contradice la existencia de una pequeña reserva de cardiomiocitos altamente proliferativos. Además, todas las células hijas hermanas eran cardiomiocitos; no se observaron casos de células hermanas no miocárdicas y miocárdicas, lo que contradice la existencia de un progenitor cardíaco bipotente o multipotente. Sin embargo, una limitación de MADM es que, debido a la recombinación Cre ineficiente, subestima la tasa de proliferación de cardiomiocitos y no puede refutar directamente la existencia de una célula progenitora. No obstante, otros modelos de rastreo de linaje estiman la contribución a la cardiomiogénesis de las células madre/progenitoras residentes en menos del 0,01 % anual.
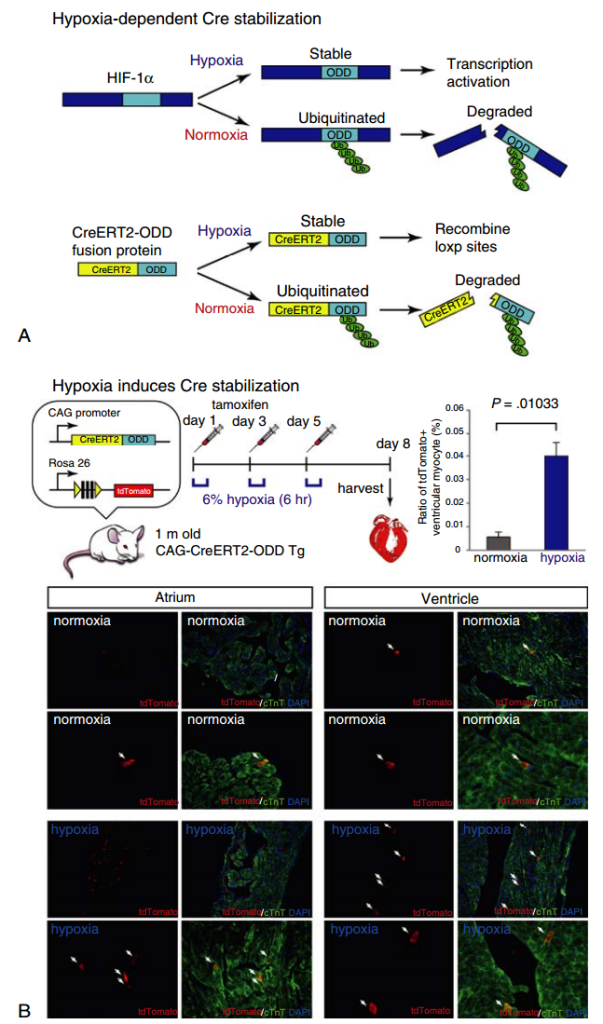
Estos estudios previos dejaron abierta la cuestión de si todos los cardiomiocitos pueden participar en la cardiomiogénesis posnatal o si un subconjunto único de cardiomiocitos posee este potencial. Basándose en sus hallazgos de que la exposición a la normoxia después de la vida fetal se asocia con la detención del ciclo celular de los cardiomiocitos posnatales, Kimura y sus colegas desarrollaron un nuevo modelo de mapeo del destino de la hipoxia para determinar el potencial mitótico de los cardiomiocitos hipóxicos (Fig. 3.6). Demostraron que los cardiomiocitos hipóxicos, marcados por la expresión de Hif-1α, comprenden el subtipo predominante de cardiomiocitos adultos que experimenta división posnatal durante el envejecimiento fisiológico; estas células también proliferan después de una lesión por infarto de miocardio. La mayoría de los cardiomiocitos recién nacidos, identificados mediante la incorporación nuclear de BrdU, parecen provenir de esta cohorte de cardiomiocitos hipóxicos, que son más pequeños, predominantemente mononucleares y acumulan menos daño oxidativo en el ADN que los cardiomiocitos restantes. Estos hallazgos refuerzan la afirmación de que la mayoría de los cardiomiocitos adultos de mamíferos son posmitóticos y señalan la señalización de la hipoxia como un factor importante en la cardiomiogénesis posnatal.
La combinación de rastreo de linaje, marcaje con radioisótopos y análisis clonal ha proporcionado las evaluaciones más minuciosas tanto de las tasas de renovación de los cardiomiocitos como de su ontogenia en el corazón de los mamíferos. Estos estudios demuestran claramente que, si bien la mayoría de los cardiomiocitos adultos de mamíferos no participan en la división celular durante el envejecimiento o tras una lesión, un pequeño subconjunto conserva potencial mitótico que podría ser objeto de terapias.
Bases moleculares del estado de diferenciación terminal de los cardiomiocitos
La evidencia obtenida en modelos animales demostró que solo una pequeña fracción de cardiomiocitos se renueva en el corazón de los mamíferos, mientras que el resto parece estar detenido en su ciclo celular. La búsqueda del control molecular subyacente a la salida del ciclo celular de la mayoría de los cardiomiocitos posnatales dio como resultado la recopilación de una lista de genes que se sabe que promueven la detención del crecimiento en múltiples sistemas. El cese de la proliferación de miocitos al nacer se ha relacionado con la regulación negativa de las ciclinas, las quinasas dependientes de ciclinas (CDK) y los factores de transcripción E2F, y con la regulación positiva de los moduladores negativos de la progresión del ciclo celular: Cdkn1a, Cdkn1b, Cdkn1c y Cdkn2c. La presencia de receptores de factores de crecimiento funcionales en la membrana plasmática de los miocitos maduros les confiere la capacidad de hipertrofia fisiológica y/o patológica necesaria en respuesta a cargas patológicas, en combinación con la reexpresión del programa genético fetal.
Basándose en observaciones en mioblastos esqueléticos, se planteó la hipótesis de que la proteína retinoblastoma (Rb) inhibe permanentemente la transición de los cardiomiocitos de la fase G1 a la fase S del ciclo celular. Por ejemplo, el corazón neonatal presenta Rb inactiva (hiperfosforilada), lo que coincide con la renovación de los miocitos, mientras que los corazones adultos e hipertrofiados se caracterizan por altos niveles de Rb activa hipofosforilada, que se opone a la división de los miocitos. De manera similar, las ciclinas A, D1, D2 y D3, reguladoras del ciclo celular, se expresan en altos niveles en el corazón en desarrollo y su expresión disminuye rápidamente después del nacimiento.
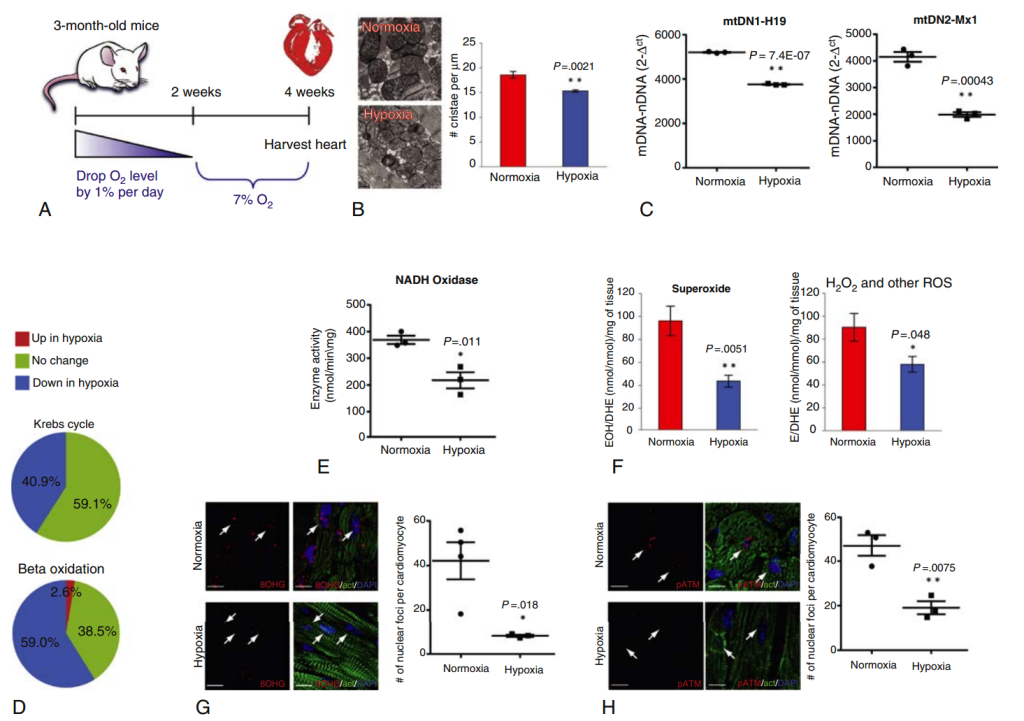
Evidencia reciente respalda la hipótesis de que la activación de la vía de respuesta al daño del ADN (DDR) en el período posnatal conduce a la detención del ciclo celular en los cardiomiocitos de mamíferos. La hipoxemia relativa de la circulación fetal se reemplaza por normoxia después del nacimiento al exponerse al oxígeno ambiental. Simultáneamente con este aumento en la tensión de oxígeno circulante, se produce una transición en el corazón del ratón neonatal de la glucólisis al metabolismo aeróbico, un cambio metabólico que conlleva la dependencia de las mitocondrias para la generación de energía y, por lo tanto, genera altos niveles de especies reactivas de oxígeno (ROS). Puente y colaboradores demostraron que los altos niveles de ROS en el corazón posnatal generan daño oxidativo en el ADN, lo que activa la vía DDR. Demostraron que la exposición a la hipoxemia posnatal, la inhibición de la DDR y la atenuación de las ROS extienden la ventana posnatal de proliferación de cardiomiocitos. Por otro lado, la hiperoxemia y los generadores de ROS acortan dicha ventana. Para respaldar aún más esta hipótesis, Nakada y sus colegas lograron atenuar parcialmente el fenotipo posmitótico de los cardiomiocitos adultos al exponer ratones a hipoxia ambiental. Demostraron que existe una mayor proliferación de cardiomiocitos a un nivel de oxígeno atmosférico del 7% debido a una disminución de las especies reactivas de oxígeno (ROS) y del ADN oxidado, en comparación con los ratones control normóxicos que experimentan un 21% de oxígeno ambiental (Fig. 7).
La poliploidización de los cardiomiocitos de mamíferos también se ha asociado con la pérdida del potencial proliferativo, aunque las células hepáticas poliploides son capaces de dividirse y contribuyen a la regeneración de los hepatocitos. Un estudio reciente y exhaustivo del estado de nucleación de los cardiomiocitos en 120 cepas de ratones endogámicos reveló una amplia variación en la frecuencia de cardiomiocitos diploides mononucleares, que oscilaba entre el 2,3 % y el 17,0 % del total de cardiomiocitos. Curiosamente, se observó que las cepas con mayor proporción de cardiomiocitos diploides mononucleares presentaban una mayor proliferación y regeneración de cardiomiocitos tras un infarto agudo de miocardio en adultos. Esta hipótesis se puso a prueba directamente en el pez cebra, en el que el 99 % de los cardiomiocitos adultos son diploides mononucleares y conservan la capacidad de regenerarse tras una lesión. La perturbación genética transitoria provocó poliploidía en la mitad de los cardiomiocitos del pez cebra (tras la activación de una versión dominante negativa de la proteína clave de la citocinesis, ECT2). En este modelo, los cardiomiocitos diploides mononucleares proliferaron a mayor ritmo que los cardiomiocitos poliploides tras la amputación del ápice ventricular en el pez cebra adulto. Curiosamente, cuando la fracción de células poliploides alcanzó aproximadamente el 50 % del total de cardiomiocitos, la capacidad regenerativa del pez cebra adulto se vio significativamente afectada. Queda por determinar si este mecanismo también se aplica al corazón de los mamíferos. Además, aún se desconoce si los cardiomiocitos binucleares y poliploides de los mamíferos pueden sufrir abscisión durante el envejecimiento o tras una lesión patológica.
Otro desafío para la capacidad de división de los cardiomiocitos posnatales podría residir fuera de la célula: un informe reciente documentó un cambio en la composición de la matriz extracelular durante la primera semana de vida en ratones neonatos, que se correlaciona con la pérdida de una capacidad proliferativa significativa. Específicamente, la agrina, un proteoglicano de la matriz extracelular, está presente en los corazones de ratones neonatos y es necesaria para la regeneración cardíaca neonatal. La expresión de agrina se pierde durante la primera semana de vida, pero una única inyección miocárdica de agrina tras un infarto de miocardio en ratones adultos aumentó la proliferación de cardiomiocitos, redujo la fibrosis y mejoró la función sistólica.
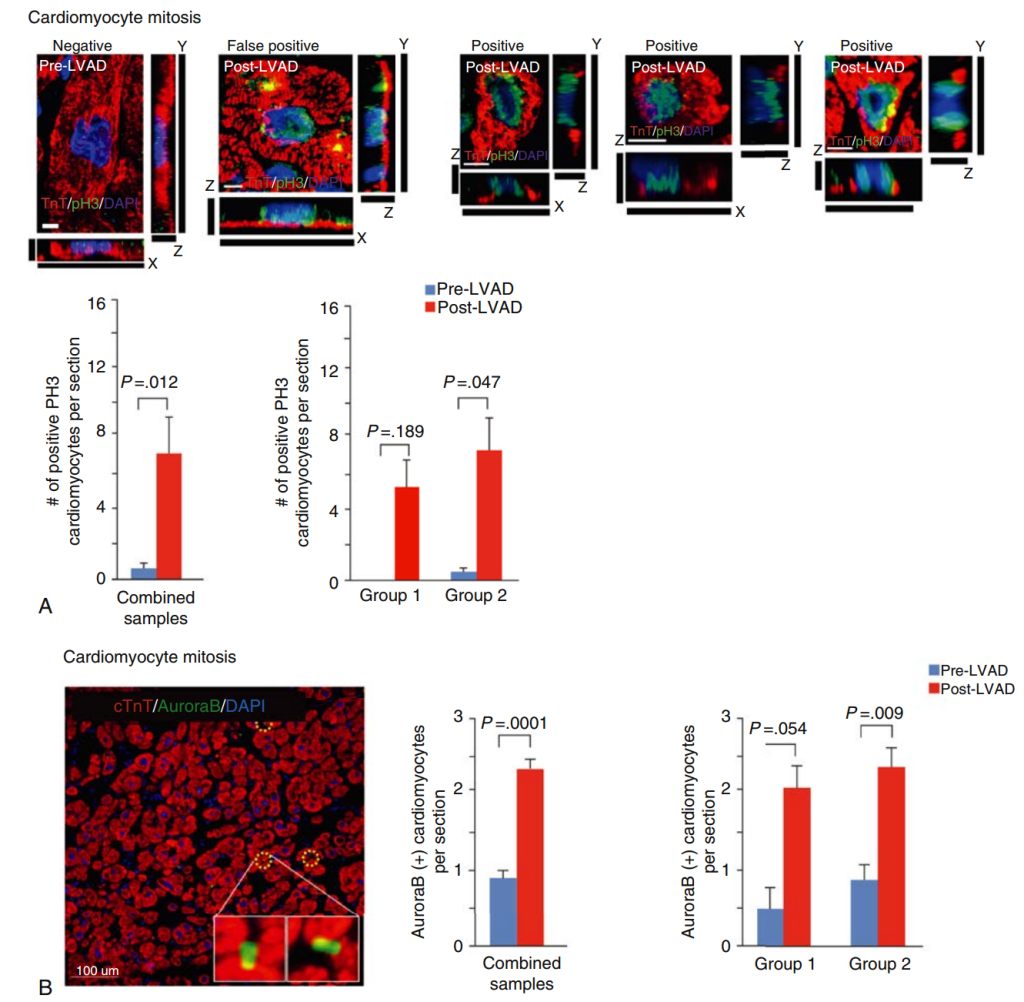
El mecanismo por el cual la matriz extracelular interviene en la proliferación de cardiomiocitos podría ser mediante la transducción de la carga mecánica, la cual ha demostrado influir en el estado nuclear y mitocondrial de los cardiomiocitos en el corazón humano. Un modelo natural para la descarga del ventrículo izquierdo es el dispositivo de asistencia ventricular izquierda (DAVI), que se implanta en pacientes con insuficiencia cardíaca avanzada como puente al trasplante cardíaco ortotópico o como terapia definitiva. Los DAVI son bombas mecánicas que aumentan el gasto cardíaco y la perfusión sistémica, mejorando así la función de los órganos. Cabe destacar que un pequeño subgrupo de pacientes con DAVI ha experimentado una recuperación miocárdica suficiente como para poder someterse a la explantación del dispositivo. La recuperación funcional en estos pacientes sugiere un efecto beneficioso de la descarga de presión del ventrículo izquierdo, lograda mediante un DAVI. Las biopsias cardíacas de pacientes con LVAD mostraron una disminución en la poliploidía global de los cardiomiocitos (que aumenta en corazones con insuficiencia cardíaca) y un aumento en el número de cardiomiocitos diploides, lo que sugiere que la mitosis de los cardiomiocitos y/o la abscisión de los cardiomiocitos poliploides pueden estar ocurriendo en corazones sin carga. Además, los corazones post-LVAD tienen un número reducido de copias de ADN mitocondrial, cardiomiocitos más pequeños y una actividad reducida en la vía DDR. En consonancia con hallazgos previos que indican que la activación de la vía DDR atenúa la división de los cardiomiocitos, los corazones post-LVAD tienen una mayor expresión de proteínas asociadas a la mitosis y la citocinesis (Fig. 8). Estos hallazgos implican que la descarga mecánica puede conducir a la división celular de los cardiomiocitos y, por lo tanto, puede representar otro medio para lograr la regeneración cardíaca.
En conjunto, estos estudios demuestran que diversos mecanismos celulares, tanto autónomos como no autónomos, subyacen al estado de diferenciación terminal que caracteriza a la mayoría de los cardiomiocitos en el corazón de los mamíferos. Aún no está claro si todos los mecanismos descritos previamente se aplican a todos los cardiomiocitos o si las subpoblaciones de cardiomiocitos se ven afectadas de manera diferente. Será necesario seguir evaluando y manipulando estas vías para optimizar las terapias que sustentan la regeneración cardíaca.
Mecanismos de regeneración cardíaca
Regeneración cardíaca endógena en vertebrados inferiores y mamíferos
Existen pocas especies conocidas con la capacidad de regenerar el corazón de forma sustancial. En 2002, Poss y sus colegas demostraron por primera vez que la resección quirúrgica del 20 % del ventrículo único del pez cebra fue seguida de una regeneración completa sin cicatrices fibróticas en 60 días (Fig. 9). El mapeo del destino celular confirmó que la regeneración cardíaca está mediada principalmente por la proliferación de cardiomiocitos preexistentes en el pez cebra adulto.
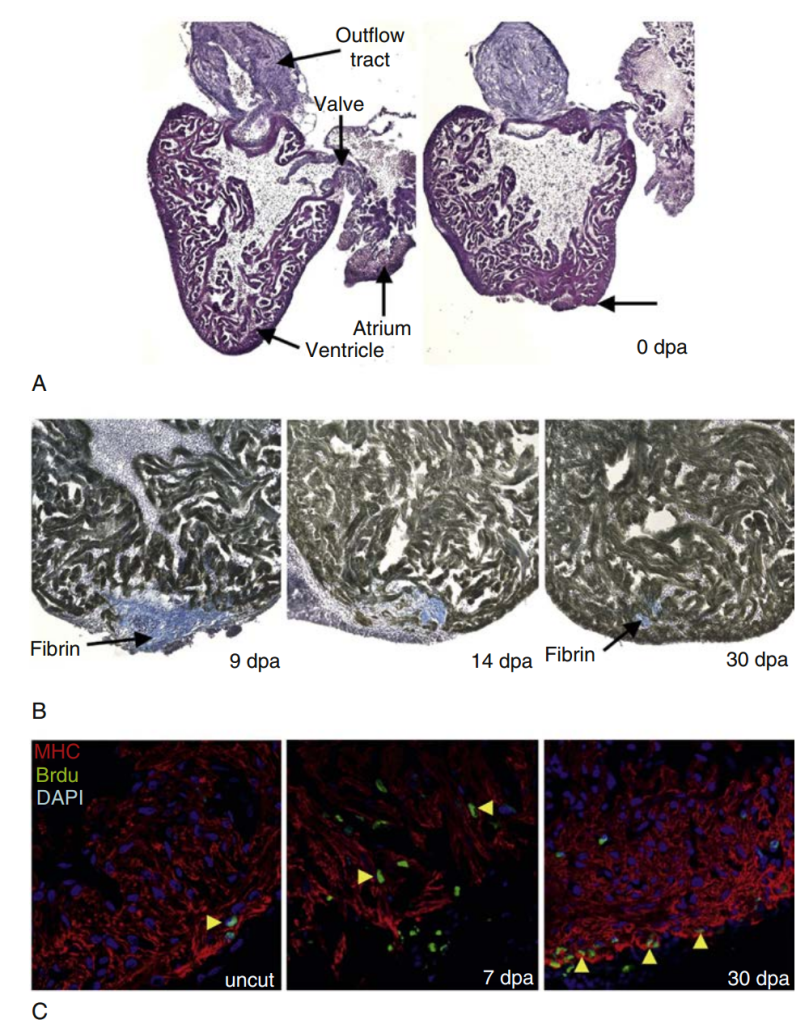
La demostración de que los vertebrados, como los peces teleósteos, podían regenerar el corazón planteó la fascinante posibilidad de que los mamíferos también poseyeran esta capacidad. En 2011, Sadek y sus colegas adaptaron el modelo de resección apical ventricular del pez cebra a ratones neonatos para evaluar la regeneración cardíaca. Este estudio pionero reveló que los ratones de un día posparto (P1) conservan la capacidad de regenerar sus corazones tras la resección cardíaca (Fig. 10). A los ratones P1 se les realizó una resección quirúrgica del 15 % del ventrículo izquierdo, y en 21 días el miocardio se reemplazó por completo, con la normalización de la fracción de eyección del ventrículo izquierdo a los dos meses de la resección. El mapeo genético del destino celular sugirió que la principal fuente de regeneración es la expansión de los cardiomiocitos existentes. Cabe destacar que la resección apical no produjo hipertrofia de los cardiomiocitos ni fibrosis significativa.
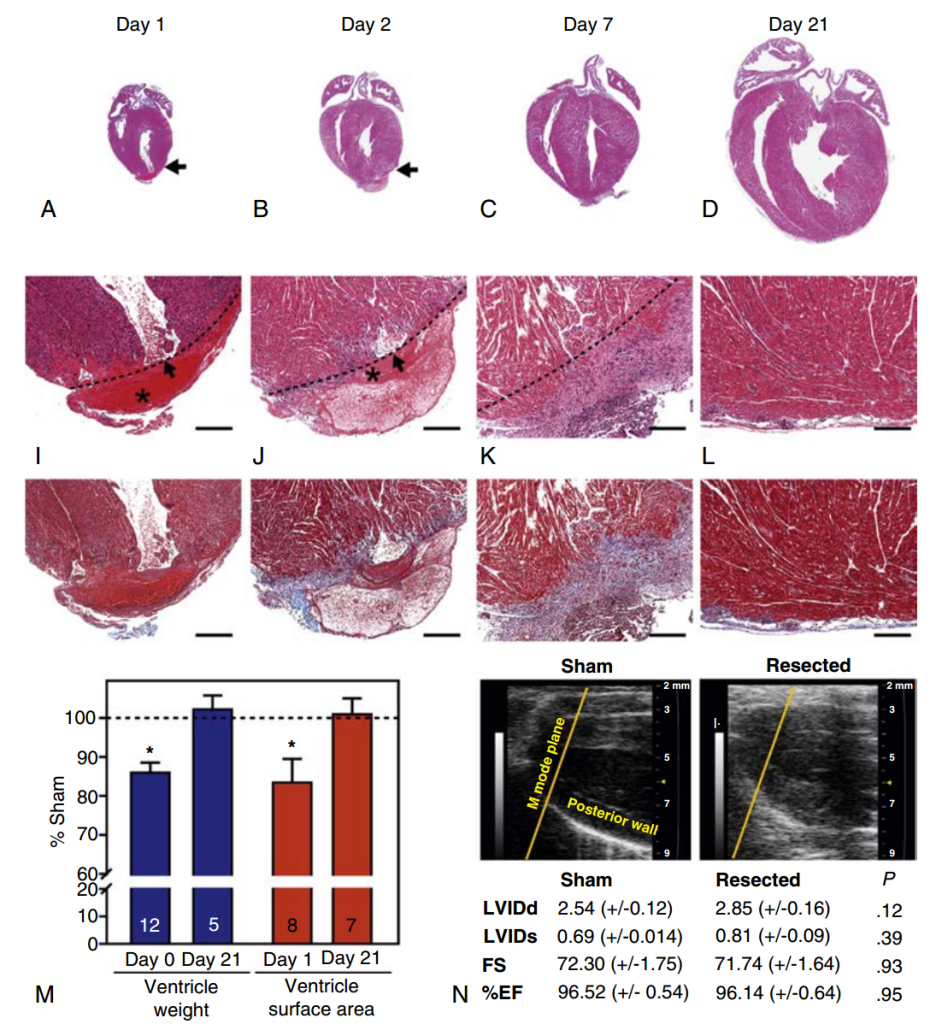
En contraste, la capacidad de regenerar el corazón se pierde en ratones P7. A pesar de una amputación quirúrgica proporcionalmente menor en ratones P7 (debido a una mayor mortalidad quirúrgica), su miocardio no se regeneró y, en cambio, mostró cambios fibróticos. Esta pérdida del potencial regenerativo cardíaco durante la primera semana de vida posnatal coincide con la binucleación de los cardiomiocitos y su salida del ciclo celular (es decir, un cambio de hiperplasia a hipertrofia) en roedores. Un modelo de infarto de miocardio más relevante desde el punto de vista fisiológico, mediante la ligadura de la arteria coronaria descendente anterior izquierda, validó la estrecha ventana regenerativa intrínseca hasta la primera semana de vida en ratones. Desde entonces, numerosos estudios han utilizado el modelo de resección apical y modelos de corazón de ratón neonatal con infarto de miocardio para comprender mejor los factores que promueven o inhiben la regeneración cardíaca. Estos modelos quirúrgicos siguen proporcionando información sobre los mecanismos de regeneración cardíaca en mamíferos que pueden producirse tras la repoblación de tejido perdido o dañado, incluso en presencia de depósitos residuales de matriz extracelular o una pequeña cantidad de depósitos de fibrina.
La exposición de la regeneración cardíaca en ratones recién nacidos lleva a inferir que los mamíferos superiores también podrían poseer tal potencial. Es interesante especular sobre la posibilidad de que, tras una lesión cardíaca, los corazones neonatales humanos también puedan regenerarse. Aparte de informes anecdóticos de mejoría en la fracción de eyección tras un infarto de miocardio en un recién nacido, es difícil pronunciarse sobre la capacidad de regeneración del corazón humano neonatal: en ausencia de estudios de viabilidad que documenten la reversión del miocardio no viable, una mejoría de la función sistólica podría atribuirse a la reversión de una disfunción contráctil transitoria, como en casos de aturdimiento miocárdico o hibernación.
Inducción de la proliferación de cardiomiocitos
Los corazones de mamíferos adultos presentan una baja tasa de proliferación de cardiomiocitos en condiciones fisiológicas para mantener su renovación. Además, el mecanismo predominante de regeneración cardíaca en el pez cebra y los ratones neonatos es la proliferación de cardiomiocitos preexistentes. Por lo tanto, resulta de gran interés identificar mecanismos que promuevan la proliferación de cardiomiocitos adultos como una estrategia potencial para restaurar el tejido cardíaco tras una lesión.
Ciclinas y quinasas dependientes de ciclinas
La progresión del ciclo celular está modulada positivamente por los complejos ciclina/cinasa dependiente de ciclina (CDK), y las ciclinas se encuentran reguladas negativamente en los cardiomiocitos después del nacimiento. La sobreexpresión combinada de CDK1, CDK4, ciclina B1 y ciclina D1 provocó la replicación de los cardiomiocitos adultos. La inducción de estos cuatro factores tras un infarto de miocardio inducido quirúrgicamente conllevó una mejora en la fracción de eyección y una menor extensión de la cicatriz.
microARN
El microARN (miR)-195 es el miR con mayor expresión en el corazón de ratón desde el día P1 hasta el P10 y, mediante la inhibición de genes mitóticos clave como la quinasa de punto de control 1, contribuye a la salida del ciclo celular de los cardiomiocitos que ocurre durante este período. La sobreexpresión cardíaca transgénica de miR-195 perjudica la proliferación de cardiomiocitos y produce corazones más pequeños, mientras que la inhibición de miR-195 aumenta el número de cardiomiocitos mitóticos. Por otro lado, múltiples miRs pueden regular positivamente la proliferación de cardiomiocitos neonatales en cultivo. Cabe destacar que miR-590 y miR-199a aumentan la división de cardiomiocitos en modelos animales y, cuando se administran en el corazón de ratones adultos en el momento del infarto de miocardio, pueden mejorar la función sistólica y reducir el tamaño del infarto. Estos y otros estudios demuestran que la alteración de miRs críticos puede permitir la regeneración cardíaca.
Factores de transcripción
La alteración de la actividad de los factores de transcripción FOXO y MEF2 en cardiomiocitos cultivados demostró su papel en la modulación del ciclo celular de los cardiomiocitos in vitro. Un mayor conocimiento de los efectos de diversos factores de transcripción sobre el estado posmitótico cardíaco en modelos animales podría tener implicaciones terapéuticas. MEIS1 es un factor de transcripción con homeodominio que regula la diferenciación cardíaca durante el desarrollo. Durante la primera semana de vida en ratones, la proteína MEIS1 se expresa, pero no se localiza en el núcleo. En el día postnatal 7 (P7), la translocación nuclear de MEIS1 se correlaciona con la salida de los cardiomiocitos del ciclo celular, mediada en parte por la activación de los inhibidores de CDK p15, p16 y p21. Los ratones transgénicos con expresión forzada de MEIS1 específica de cardiomiocitos pierden la capacidad de regenerarse tras un infarto de miocardio en el día postnatal 1 (P1). En cambio, la ventana de proliferación normal se extiende más allá del día postnatal 7 (P7) cuando se elimina Meis1 en los cardiomiocitos (Fig. 11).
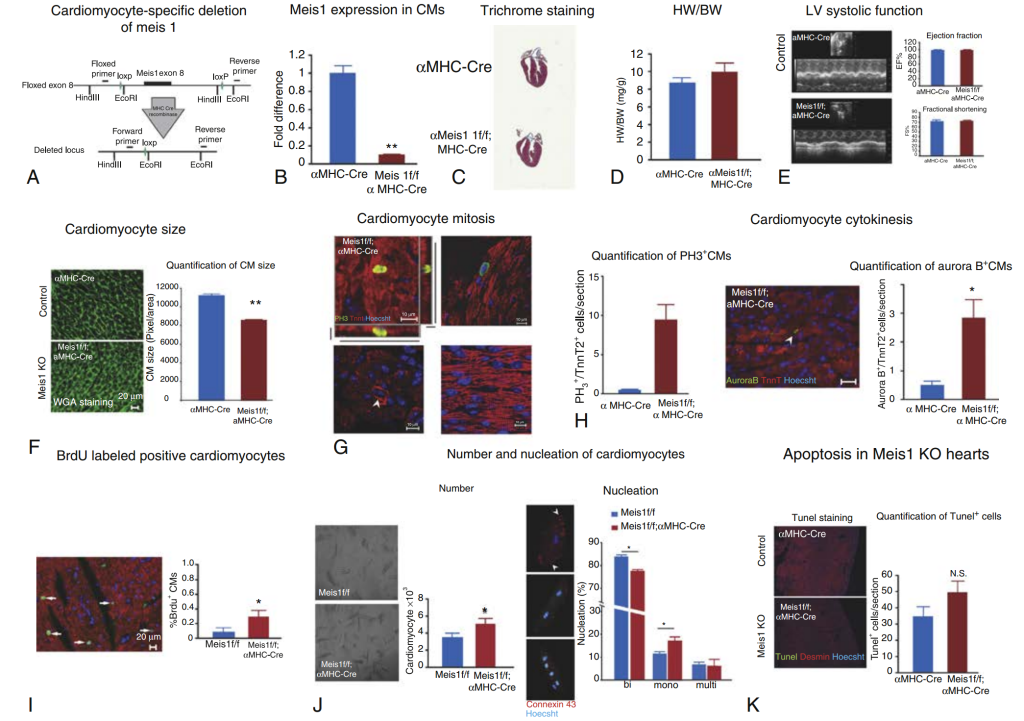
A diferencia de MEIS1, el factor de transcripción GATA4 pierde su expresión tras la primera semana de vida en ratones. El aumento de los niveles de GATA4 inducido por adenovirus tras una criolesión en el día postnatal 7 incrementa la proliferación de cardiomiocitos y mejora la función cardíaca. Por el contrario, la anulación de la actividad neonatal de GATA4 afectó negativamente la regeneración tras una criolesión en el día postnatal 0.
Nervios
Un importante eje cardíaco-neural podría ser la base de la regeneración cardíaca neonatal: los corazones de ratones P1 tratados con atropina en el momento de la resección apical mostraron una menor proliferación de cardiomiocitos en comparación con los controles, probablemente debido a la inhibición de la transmisión colinérgica. La resección apical en P1 combinada con vagotomía izquierda también disminuyó la proliferación de cardiomiocitos. Estos hallazgos sugieren un papel de la señalización colinérgica en la regulación de la regeneración cardíaca en mamíferos. En un estudio independiente, la simpatectomía química de ratones P2 sometidos a resección apical provocó fibrosis y una regeneración deficiente del miocardio. Estas observaciones podrían estar mediadas por el factor de crecimiento nervioso, que ha demostrado aumentar indirectamente la proliferación de cardiomiocitos en larvas de pez cebra.
La vía de señalización Hippo
Descubierta en Drosophila, la vía de señalización Hippo tiene una función evolutivamente conservada en la regulación del tamaño de los órganos mediante el control de la proliferación y la apoptosis celular. La alteración de la señalización Hippo en el corazón del ratón puede aumentar la proliferación de cardiomiocitos y provocar cardiomegalia, lo que indica que Hippo participa en el desarrollo y las lesiones cardíacas (Fig. 12). Yap, el componente más distal de la vía de señalización Hippo en ratones, es un coactivador transcripcional que se secuestra en el citoplasma tras su fosforilación. Una vez desfosforilada, la forma activa de Yap se acumula en el núcleo e interactúa con factores de transcripción del dominio TEA para promover la división de los cardiomiocitos. Los ratones con una mutación específica en el corazón, que produce una activación constitutiva de YAP, presentan una mayor proliferación de cardiomiocitos y un aumento del tamaño del corazón, así como una prolongación de la ventana regenerativa cardíaca neonatal mediante la activación de las vías de señalización Wnt e IGF. Por el contrario, la eliminación del gen Yap en los cardiomiocitos provoca un adelgazamiento del miocardio y una función cardíaca comprometida entre las 6 y las 12 semanas de vida, y resulta en una muerte prematura entre las 11 y las 20 semanas.
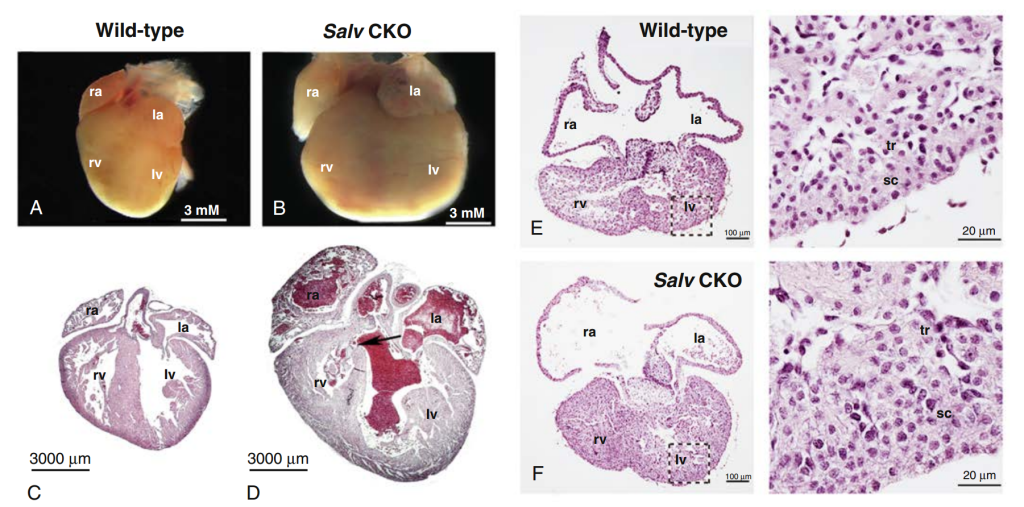
Descarga ventricular
La descarga ventricular aumenta la progresión del ciclo celular en los cardiomiocitos y mejora la función cardíaca. Un estudio de caso de un lactante con insuficiencia cardíaca grave que recibió un trasplante cardíaco heterotópico proporciona un ejemplo natural de descarga ventricular, ya que el corazón nativo permaneció en su lugar sin la función exclusiva de proporcionar soporte circulatorio. Sorprendentemente, el corazón del paciente recuperó su función durante este período. Debido en parte a los efectos secundarios relacionados con el trasplante, se extrajo el corazón del donante: el propio corazón del paciente reanudó su función circulatoria completa. Se desconoce el mecanismo subyacente en este informe, pero se hipotetiza que reducir la carga de trabajo del corazón puede ayudar a la recuperación de la función cardíaca. De manera análoga, el soporte mecánico mediante dispositivos de asistencia ventricular izquierda (DAVI) puede promover la capacidad del corazón para regenerarse, posiblemente debido a la descarga de presión del corazón nativo por el dispositivo de bombeo.
Cardiomiocitos exógenos para terapia celular
Desde la generación de líneas de células madre embrionarias humanas (hESC) y el descubrimiento de células madre pluripotentes inducidas (iPSC) en 2006 por Yamanaka y sus colegas, la capacidad de estas células madre pluripotentes (PSC) para generar células y tejidos que potencialmente podrían tratar enfermedades humanas ha sido muy valorada. La promesa de las células pluripotentes en el tratamiento de enfermedades cardíacas radica, en parte, en su capacidad para generar sustratos para la terapia de trasplante celular, cuya premisa fundamental es la hipótesis de que un aumento en el número de cardiomiocitos tras una lesión miocárdica beneficia la función cardíaca.
En la última década, se han logrado avances significativos en la identificación de las condiciones de diferenciación que dan lugar a poblaciones purificadas de cardiomiocitos con un alto rendimiento. El uso de ciertas citocinas mejora notablemente la eficiencia de la diferenciación cardíaca de las células madre pluripotentes (CMP). Si bien ahora es posible obtener células similares a cardiomiocitos a partir de CMP, un desafío para el campo —especialmente en lo que respecta al posible trasplante celular— radica en la caracterización precisa de estas células. El análisis transcripcional de cardiomiocitos (CM) derivados de CMP ha demostrado que expresan genes asociados con componentes del aparato contráctil, la maquinaria de manejo del calcio y la conectividad eléctrica, por lo que fenotípicamente parecen ser CM. Sin embargo, la semejanza es mayor con los CM embrionarios inmaduros que con los CM adultos. Con este fin, un trabajo reciente utilizó un cribado funcional de organoides cardíacos derivados de células madre embrionarias humanas (hESC) para identificar un método metabólico que permita «madurar» los CM derivados de CMP. Además, si bien los protocolos actuales para diferenciar células madre pluripotentes (CMP) en cardiomiocitos (CM) no se ven afectados por la derivación de otros tipos celulares, la población resultante es heterogénea, ya que se obtienen subtipos ventriculares, nodales y auriculares de CM, los cuales presentan propiedades electrofisiológicas distintas. Por lo tanto, se requiere más investigación para purificar específicamente los diferentes subtipos de cardiomiocitos.
Varios grupos han trasplantado células derivadas de células madre pluripotentes (CMP) en modelos animales, con resultados prometedores que también generan cierta inquietud. Uno de los primeros ejemplos de implantación de cardiomiocitos derivados de células madre embrionarias humanas (CMhE) en un modelo de roedor se publicó en 2005: se inyectó una población mixta de células derivadas de CMH enriquecidas con células cardíacas en corazones de ratas, demostrándose el injerto a largo plazo de los CMhE. Posteriormente, este grupo trasplantó cardiomiocitos purificados derivados de CMH en un modelo de corazón de cobaya y demostró que la adición de células donantes mejoraba la función mecánica tras una criolesión y reducía las arritmias espontáneas. Ardehali y sus colaboradores ampliaron estas observaciones demostrando que los progenitores cardiovasculares derivados de CMH pueden injertarse en tejido fetal humano (trasplantado quirúrgicamente en el pabellón auricular del ratón) y generar cardiomiocitos, células musculares lisas vasculares y células endoteliales. Uno de los primeros estudios en primates utilizó macacos como huéspedes y demostró que los cardiomiocitos derivados de células madre embrionarias humanas (hESC) se injertan y acoplan electromecánicamente al corazón del primate tras una lesión por isquemia miocárdica con reperfusión (Fig. 13). Sin embargo, los hESC-CM permanecieron inmaduros tres meses después del trasplante y, a diferencia de los datos de estudios en animales pequeños, se observaron arritmias ventriculares no fatales.
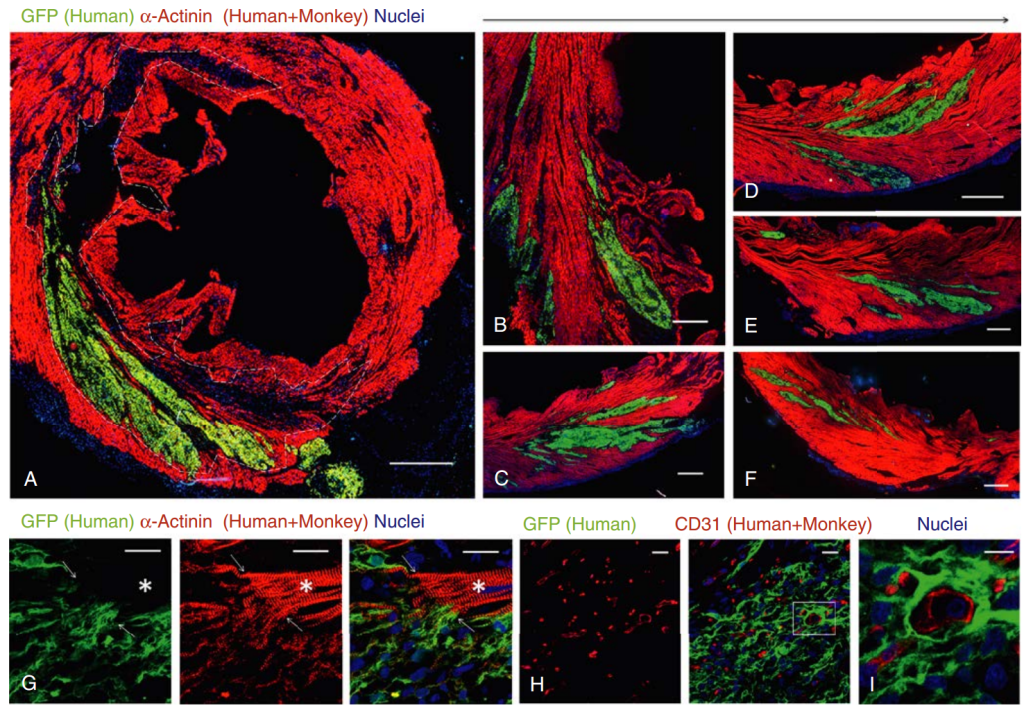
Los estudios en animales también han revelado que las células trasplantadas suelen ser inviables tras la inyección intramiocárdica directa, lo que puede deberse a las altas presiones de inyección y/o a un microambiente tisular local desfavorable.
Por lo tanto, se están explorando enfoques de bioingeniería para mejorar la viabilidad celular. El uso de tejido a base de hidrogel que contiene proteínas de la matriz extracelular (MEC) como material de soporte para células derivadas de PSC ha tenido resultados inconsistentes cuando se trasplantan colectivamente en diversos modelos animales. Se han desarrollado láminas celulares tridimensionales (3D) desmontables de cardiomiocitos derivados de iPSC como sustrato para el trasplante celular, con un efecto más duradero en la viabilidad de las células trasplantadas. Otro soporte innovador que se asemeja más al miocardio humano nativo es el tejido cardíaco cadavérico descelularizado, obtenido a partir de tejido primario o mediante un enfoque de impresión 3D. Cada vez es más evidente que el mecanismo de administración de las células derivadas de PSC trasplantadas es un aspecto importante del desafío de la terapia de trasplante celular.
El primer caso clínico de trasplante de cardiomiocitos derivados de células madre pluripotentes (PSC-CM) en humanos se publicó en 2015. Se seleccionaron células cardíacas diferenciadas a partir de una línea de células madre embrionarias humanas (hESC) según sus marcadores de superficie y se incorporaron a un parche de matriz de fibrina. El parche se implantó quirúrgicamente en un hombre de mediana edad con insuficiencia cardíaca avanzada durante una cirugía de revascularización coronaria, sobre la superficie epicárdica de una región cardíaca infartada, acinética y no revascularizada. Tras el trasplante celular, el paciente recibió tratamiento inmunosupresor. Tres meses después de la cirugía, se observó contractilidad en la zona tratada con el parche mediante ecocardiografía, mejoró su clase funcional según la clasificación de la Asociación del Corazón de Nueva York (NYHA) y no presentó arritmias ni evidencia de formación de tumores. En 2018, el mismo grupo informó sobre el trasplante de progenitores cardiovasculares derivados de células madre embrionarias humanas (hESC) en seis pacientes con miocardiopatía isquémica avanzada durante la cirugía de revascularización coronaria. Si bien los pacientes no presentaron arritmias ni tumores cardíacos a los 18 meses de seguimiento, la mitad desarrolló aloimunización clínicamente asintomática. Los beneficios clínicos en estos pacientes no fueron significativos, pero se observó un aumento en el movimiento sistólico de los segmentos miocárdicos trasplantados y una mejoría sintomática en todos ellos. Este ensayo demuestra la seguridad a corto y mediano plazo del trasplante celular con células cardíacas derivadas de células madre pluripotentes inducidas (PSC).
A pesar de los resultados alentadores de estos ensayos en humanos, la experiencia con el trasplante de células epiteliales retinianas (EPR) derivadas de iPSC en un paciente con degeneración macular obliga a reflexionar sobre el campo del trasplante celular derivado de células madre pluripotentes. Takahashi y colaboradores observaron dos cambios genéticos tanto en las iPSC del paciente como en las EPR diferenciadas a partir de dichas iPSC. Ninguna de las mutaciones está asociada con la formación de tumores; sin embargo, este incidente deja claro que el campo de la terapia de trasplante celular para el tratamiento de enfermedades cardíacas aún se encuentra en sus inicios, con una serie de cuestiones cruciales por resolver.
Reprogramación directa del destino de los cardiomiocitos
Si bien en la década de 1980 se demostró que la expresión ectópica y forzada del factor de transcripción MyoD en fibroblastos podía «transdiferenciarlos» en células de músculo esquelético, la búsqueda de un único factor de transcripción capaz de convertir un tipo de célula somática en otro había resultado infructuosa para otros tipos celulares. En 2010, el avance de la «reprogramación celular» se extendió al corazón106: una pequeña fracción de fibroblastos en cultivo se convirtió en un estado similar al de los cardiomiocitos, conocido como «cardiomiocitos inducidos» (iCM), tras la adición de una combinación de factores de transcripción.
Los informes iniciales utilizaron los factores de transcripción clave para el desarrollo cardíaco GATA4, Mef2c y Tbx5 (GMT), que se administraron mediante vectores retrovirales a fibroblastos cardíacos en cultivo. Al igual que con la pluripotencia inducida mediante los factores de Yamanka, la eficiencia de la generación de iCM fue baja, del 6,5 % de los fibroblastos cultivados. Además, la mayoría de los iCM solo se reprogramaron parcialmente y se observó un aumento temporal en la expresión génica de los cardiomiocitos. El análisis transcripcional de las células iCM mostró una regulación positiva de genes cardíacos funcionalmente importantes y una disminución de genes de fibroblastos, lo que concuerda con un cambio en el fenotipo y la identidad celular. Sin embargo, el análisis funcional de estas células reveló que solo aproximadamente un tercio de los iCM mostraron oscilaciones espontáneas de Ca2+, cuyo patrón fue más similar al observado en miocitos neonatales. Curiosamente, los estudios de mapeo genético del destino celular mostraron que la reprogramación conduce a una conversión directa de un tipo celular diferenciado y comprometido a otro de diferente origen embrionario. Dos semanas después de la inducción de los tres factores de transcripción, las células convertidas conservaron un fenotipo de cardiomiocito sin necesidad de expresión adicional de GMT, lo que indica que la conversión de linaje es un proceso estable.
A continuación, estudios clave demostraron que los fibroblastos (y otras poblaciones no miocárdicas) del corazón de ratón podían convertirse directamente en cardiomiocitos in situ mediante la administración retroviral de GMT: la conversión de linaje tras un infarto de miocardio mejoró la función cardíaca en ratones (Fig. 14). La eficiencia de la reprogramación in vivo también fue baja: entre el 2,4 % y el 6,5 % de los cardiomiocitos derivaban de fibroblastos. La evaluación transcripcional mostró que los cardiomiocitos inducidos (iCM) se asemejan más a los cardiomiocitos ventriculares neonatales y adultos. Los análisis de la expresión de proteínas de uniones comunicantes, la transferencia de colorante y el registro de corrientes iónicas (patch clamping) en los iCM sugieren que se acoplan eléctricamente con los cardiomiocitos endógenos. Estos estudios de prueba de concepto respaldan aún más la hipótesis de que aumentar la cantidad de cardiomiocitos tras un infarto de miocardio tiene un efecto beneficioso sobre la función sistólica cardíaca global.
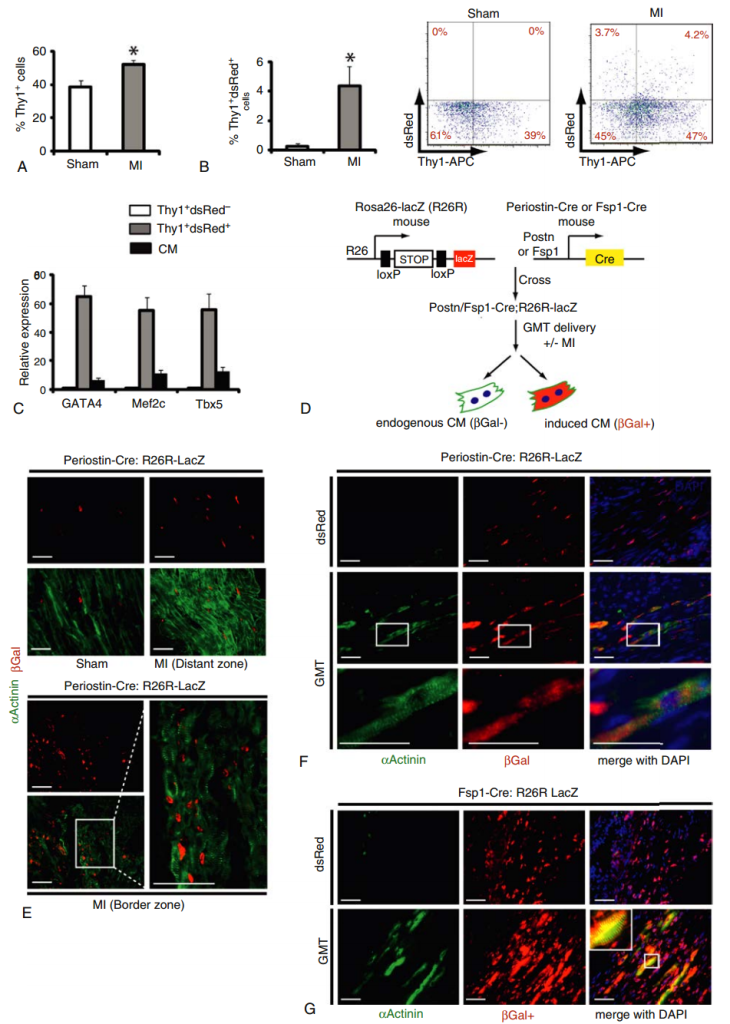
El mecanismo por el cual la reprogramación celular induce la conversión del linaje hacia el destino de miocito se basa en un cambio en el estado epigenético de la célula tras la expresión forzada de los factores de transcripción del desarrollo cardíaco GMT. Diversas combinaciones de factores de transcripción, microARN, inhibidores de moléculas pequeñas, etc., activan una familia de genes específicos de cardiomiocitos y, simultáneamente, desactivan genes específicos de fibroblastos. El análisis de las modificaciones de histonas en los cardiomiocitos inducidos (iCM) mostró que estos adquieren un patrón de cromatina similar al de los cardiomiocitos endógenos en algunos genes específicos cardíacos. La modulación de las vías del factor de crecimiento transformante β (TGF-β) y Wnt mediante inhibición química mejoró la eficiencia de la reprogramación, lo que subraya la importancia de las vías de señalización durante la conversión del linaje.
Actualmente, los estudios en el campo de la reprogramación directa buscan determinar la proporción estequiométrica óptima de factores de transcripción, microARN e inhibidores químicos que permita la conversión más eficiente de células no cardiomiocíticas en cardiomiocitos. Si bien la reprogramación directa in vivo para la conversión in situ de células representa una prometedora posibilidad terapéutica, aún quedan muchas incógnitas antes de realizar pruebas en animales de mayor tamaño y, en última instancia, en humanos. Por ejemplo, al igual que con los cardiomiocitos derivados de células iPS, es fundamental caracterizar completamente las similitudes y diferencias fenotípicas entre los cardiomiocitos endógenos nativos y los cardiomiocitos inducidos (iCM). La combinación básica de GMT puede generar múltiples subtipos de cardiomiocitos, incluyendo células del sistema de conducción. Por lo tanto, podría ser importante identificar una combinación específica de factores de reprogramación y dosis relativas que dé lugar a un subconjunto único de cardiomiocitos. En general, los prometedores resultados obtenidos hasta la fecha con la reprogramación directa de iCM en ratones generan gran esperanza en esta técnica como posible terapia para humanos.
Terapia con células no cardiomiocíticas: ¿En qué punto nos encontramos?
Una de las cuestiones más controvertidas en el campo de la regeneración cardíaca ha sido la existencia de células madre o progenitoras cardíacas residentes. Una célula madre específica de órgano se divide asimétricamente, genera células hijas restringidas a tejidos, es multipotente y, por lo general, posee un importante potencial regenerativo. En 2001, el grupo de Anversa afirmó que la médula ósea tenía una plasticidad notable y podía formar células en el corazón del ratón, incluyendo cardiomiocitos. Los investigadores aislaron células con expresión de c-kit y sin marcadores de linaje de la médula ósea de ratones GFP y las trasplantaron a corazones de ratones adultos de tipo silvestre en el momento del infarto de miocardio. Identificaron la formación de novo de miocardio y vasos sanguíneos directamente a partir de las células de la médula ósea del donante. Posteriormente, se realizaron ensayos clínicos en los que se inyectaron diversos tipos de células de la médula ósea a pacientes, ya sea por vía intravenosa o directamente en el corazón. No se observó una mejora significativa en los resultados clínicos, y cualquier efecto beneficioso se atribuye ahora a un efecto paracrino. Investigaciones independientes sobre esta notable hipótesis de transdiferenciación indican que, en lugar de una conversión de linaje, se produjo una fusión celular y una técnica analítica subóptima.
Una población celular bien estudiada y ampliamente utilizada en estudios de regeneración cardíaca son las células residentes cardíacas que expresan c-kit. En modelos murinos, se demostró que las células madre cardíacas positivas para c-kit regeneran el corazón tras un infarto de miocardio. Sin embargo, un riguroso seguimiento del linaje de las células derivadas de c-kit en modelos murinos reveló que estas células no contribuyen significativamente al linaje de los cardiomiocitos durante el desarrollo, el envejecimiento o tras una lesión cardíaca (Fig. 15). Cabe destacar que se realizó un ensayo clínico controlado aleatorizado, SCIPIO, en el que se aislaron células que expresan c-kit de las aurículas de pacientes con miocardiopatía isquémica, se expandieron en cultivo y se administraron autólogamente a los pacientes mediante inyección intracoronaria. Los resultados de este pequeño ensayo de fase I mostraron una mejora en la fracción de eyección para el grupo receptor de c-kit, pero este informe recibió una notificación de «Expresión de preocupación» por parte de The Lancet en 2014 debido a las investigaciones en curso en la institución anfitriona sobre la integridad de los datos publicados.
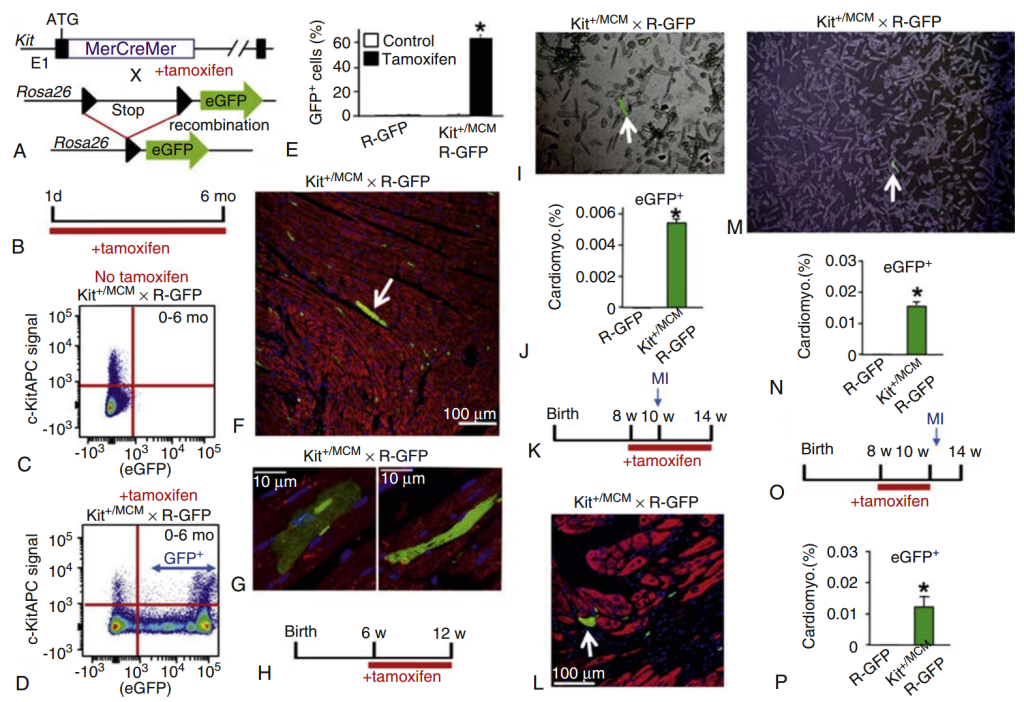
Otra población de células progenitoras putativas bien descrita, aislada del corazón, es el conjunto de células derivadas de cardioesferas (CDC). Estas células se obtienen mediante la formación de cardioesferas tridimensionales a partir de tejido cardíaco humano. En un ensayo clínico de fase I a pequeña escala, CADUCEUS, se administraron CDC autólogas a pacientes con miocardiopatía isquémica mediante inyección intracoronaria, lo que resultó en una mejoría de la función sistólica. Sin embargo, Marban y colaboradores han determinado que el beneficio de las CDC se debe a efectos paracrinos, más que a la cardiomiogénesis directa.
Un reciente ensayo clínico de fase temprana financiado por el Instituto Nacional del Corazón, los Pulmones y la Sangre (NHLBI), denominado POSEIDON-HF, evaluó la seguridad y la eficacia de las células madre mesenquimales humanas alogénicas (allo-hMSC) y autólogas (auto-hMSC) en pacientes con miocardiopatía dilatada no isquémica. Se trasplantaron allo-hMSC o auto-hMSC en múltiples sitios del ventrículo izquierdo de 37 pacientes; no se incluyó un grupo placebo. El estudio POSEIDON-HF mostró mejores resultados para el grupo de allo-hMSC, como una leve mejoría en la fracción de eyección, posiblemente debido a que las allo-hMSC se obtuvieron de una cohorte más joven y sana. Estos resultados sientan las bases para un ensayo clínico de fase más amplia que investigue el potencial clínico de las allo-hMSC en la miocardiopatía dilatada.
Conclusiones y perspectivas futuras
Hemos revisado la literatura que respalda el concepto de proliferación limitada de cardiomiocitos en el corazón como fuente de cardiomiogénesis en mamíferos, con un periodo de regeneración restringido al periodo neonatal. Analizamos las fuentes de controversia en este campo, específicamente el uso de ensayos de proliferación basados en la división del ADN, que muestran una utilidad limitada en el corazón de los mamíferos, donde los cardiomiocitos experimentan replicación del ADN sin citocinesis ni cariocinesis. Por lo tanto, se han generado nuevas herramientas para estudiar la regeneración cardíaca, como los métodos de marcaje isotópico para cuantificar la cinética de renovación de los cardiomiocitos en humanos, así como estudios de mapeo genético del destino celular y análisis clonal que confirmaron la evidencia de una división infrecuente de los cardiomiocitos. Algunas de las terapias regenerativas más prometedoras en desarrollo incluyen la terapia celular con células cardíacas derivadas de células madre pluripotentes, la reprogramación de células no miocárdicas endógenas a cardiomiocitos y la activación del ciclo celular en cardiomiocitos quiescentes. En definitiva, este campo se encuentra ahora en un momento crucial, gracias a una mayor comprensión de por qué los cardiomiocitos de los mamíferos no se dividen, así como a una serie de mecanismos biológicamente plausibles para crear nuevo miocardio funcional.
- Ali SR, et al. Existing cardiomyocytes generate cardiomyocytes at a low rate after birth in mice. Proc Natl Acad Sci USA. 2014;111:8850–8855.
- Kimura W, et al. Hypoxia fate mapping identifies cycling cardiomyocytes in the adult heart. Nature. 2015;523:226–230.
- Bergmann O, et al. Dynamics of cell generation and turnover in the human heart. Cell. 2015;161:1566–1575.
- Senyo SE, et al. Mammalian heart renewal by pre-existing cardiomyocytes. Nature. 2013;493:433–436.
- Poss KD, Wilson LG, Keating MT. Heart regeneration in zebrafish. Science. 2002;298:2188–2190.
- Porrello ER, et al. Transient regenerative potential of the neonatal mouse heart. Science. 2011;331:1078–1080.
- Mohamed TMA, et al. Regulation of cell cycle to stimulate adult cardiomyocyte proliferation and cardiac regeneration. Cell. 2018;173:104–116. e112.
- Heallen T, et al. Hippo pathway inhibits wnt signaling to restrain cardiomyocyte proliferation and heart size. Science. 2011;332:458–461.
- Qian L, et al. In vivo reprogramming of murine cardiac fibroblasts into induced cardiomyocytes. Nature. 2012;485:593–598.
- Song K, et al. Heart repair by reprogramming non-myocytes with cardiac transcription factors. Nature. 2012;485:599–604.


