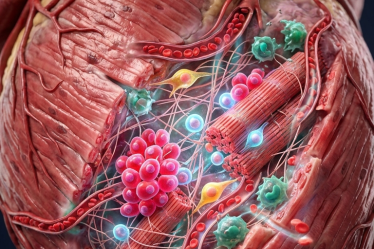
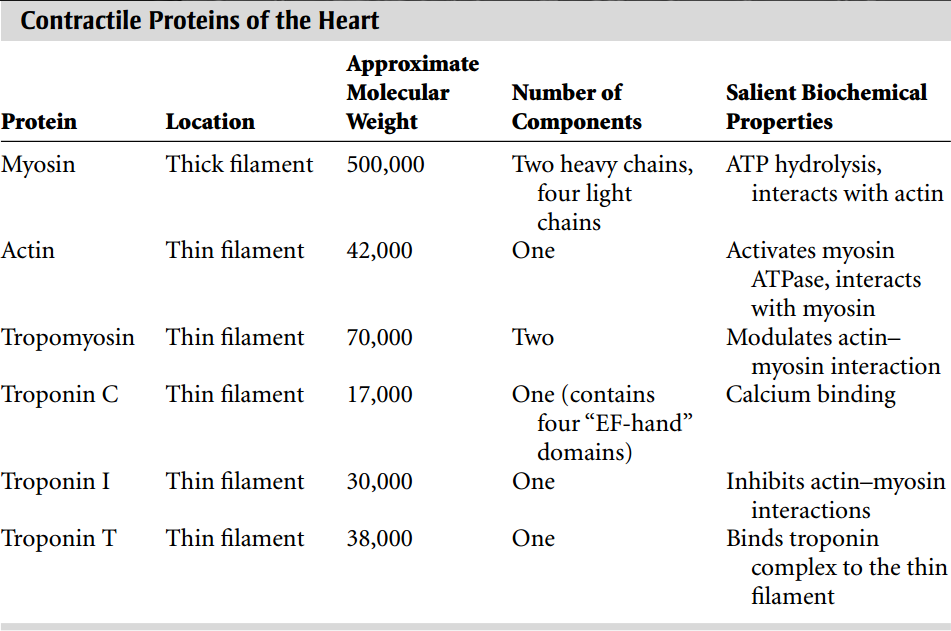
La contracción y relajación cardíaca dependen de las interacciones entre las seis proteínas enumeradas en la Tabla 1. En este capítulo se describe cada una de estas proteínas, cómo interactúan como actomiosinas in vitro para hacer que las paredes del corazón se acorten y desarrollen tensión, y cómo se regulan estas interacciones.
Miosina
Las miosinas, junto con las quinesinas y las dineínas, son «proteínas motoras» que participan en una variedad de funciones, incluida la contracción muscular, la citocinesis, la endocitosis, el transporte de orgánulos celulares, la transducción de señales y funciones sensoriales como la audición y la visión. Al igual que los motores de ferrocarril, las proteínas del motor se mueven a lo largo de las vías; En el caso de la miosina, las interacciones son con los filamentos de actina, mientras que las quinesinas y las dineínas se mueven a lo largo de los microtúbulos. Todos utilizan la energía química liberada durante la hidrólisis del ATP para realizar trabajos mecánicos.
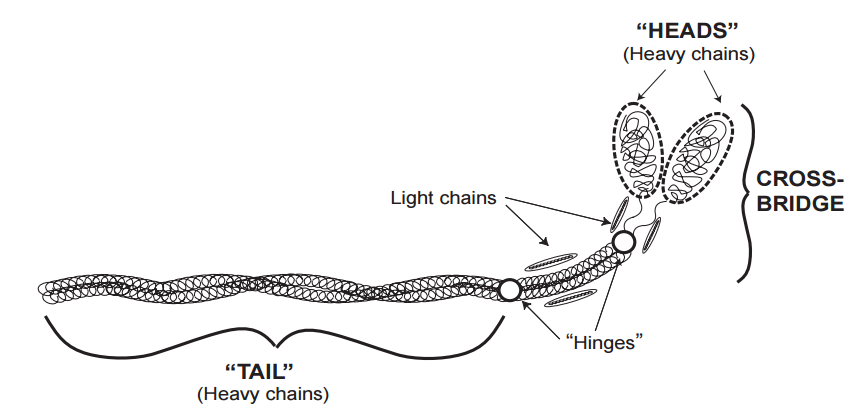
La miosina cardíaca es una molécula en forma de renacuajo formada por dos cadenas pesadas y cuatro cadenas ligeras (Fig. 1). La «cola», que es una «bobina enrollada» formada por dos cadenas pesadas helicoidales enrolladas entre sí, proporciona rigidez a los filamentos gruesos. Las cadenas pesadas contienen «cabezas» pareadas que, junto con las cadenas ligeras, forman los puentes cruzados que se proyectan desde los filamentos gruesos. Las interacciones entre los puentes cruzados, que contienen el sitio ATPasa de la miosina, y los filamentos de actina liberan la energía química que impulsa la contracción.
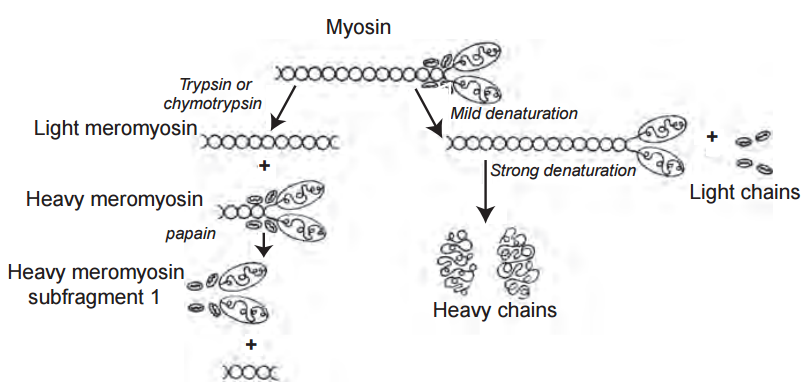
Dos fragmentos, llamados meromiosinas, son liberados de la miosina por las enzimas proteolíticas tripsina y quimotripsina. El fragmento más pequeño, la meromiosina ligera, se deriva de la cola de la molécula, mientras que la meromiosina pesada más grande incluye la cabeza, una pequeña porción de la cola y las cadenas ligeras (Fig. 2). La digestión adicional de la meromiosina pesada con papaína, otra enzima proteolítica, elimina el resto de la cola, dejando una proteína globular llamada subfragmento 1 de meromiosina pesada que incluye las cabezas emparejadas de las cadenas pesadas de miosina y las cuatro cadenas ligeras. La actividad de la miosina ATPasa y la capacidad de interactuar con la actina están presentes en la meromiosina pesada y en el subfragmento 1 de la meromiosina pesada.
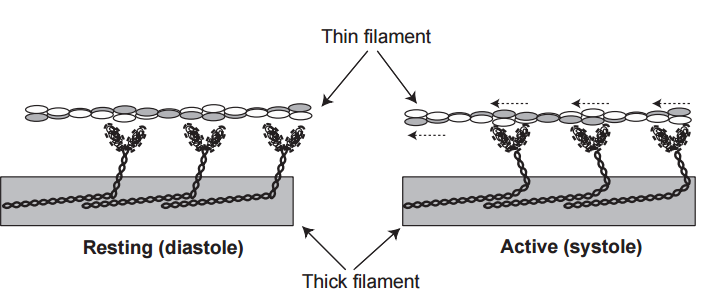
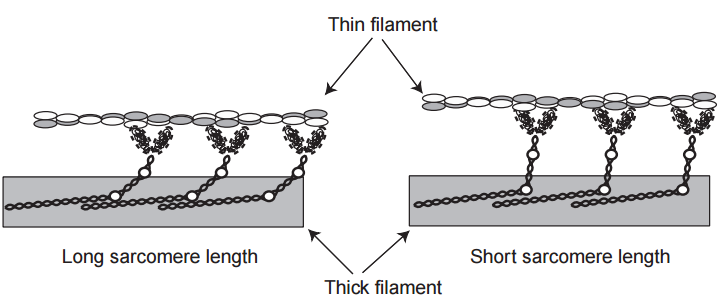
La miosina forma filamentos in vitro en los que los puentes cruzados se proyectan lejos del centro de estos agregados (Fig. 3). Estas estructuras, que se asemejan a los filamentos gruesos del músculo estriado, permiten interacciones polarizadas entre los puentes cruzados y los filamentos delgados que ingresan a la banda A desde cada una de las dos bandas I adyacentes. En los corazones en reposo, donde los filamentos gruesos y delgados están separados, los puentes cruzados son casi perpendiculares al eje largo del músculo (Fig. 4). Después de la activación, los puentes cruzados se unen y se separan de la actina en una serie de pasos que, como los remos de un caparazón de carreras, atraen los filamentos delgados hacia el centro del sarcómero. Debido a que el volumen muscular permanece prácticamente constante durante la contracción, la distancia lateral entre los filamentos gruesos y delgados se modifica por los cambios en la longitud del sarcómero. Los efectos de estos cambios en el espaciamiento de la red en el desarrollo de la tensión y la velocidad de acortamiento se minimizan mediante «bisagras» en la molécula de miosina (Fig. 1) que permiten que los puentes cruzados mantengan contacto con los filamentos delgados en longitudes cortas de sarcómeros al variar la medida en que las cabezas de miosina se extienden desde los filamentos gruesos (Fig. 5).

Cadenas pesadas
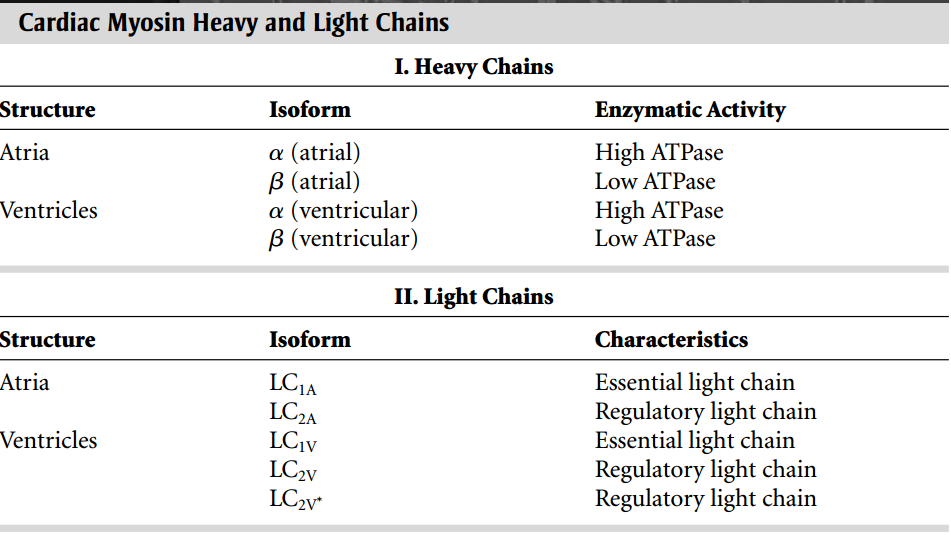
Las aurículas y ventrículos humanos adultos contienen diferentes isoformas de cadena pesada de miosina (Tabla 2); Se encuentran isoformas adicionales en el corazón fetal y neonatal. El ventrículo humano contiene principalmente una cadena pesada de ATPasa β-miosina baja junto con una pequeña cantidad (10%) de una cadena pesada de ATPasa α-miosina más alta. Las aurículas humanas contienen dos isoformas de cadena pesada de miosina auricular, las cuales difieren de las de los ventrículos. Las células miocárdicas que contienen las isoformas α y β de cadena pesada se distribuyen en un patrón de «mosaico» en el que se encuentran diferentes isoformas en las células adyacentes. La sobrecarga crónica induce una respuesta hipertrófica que se acompaña de un cambio de isoforma en el que la isoforma de cadena pesada de baja ATPasa reemplaza a la isoforma de alta ATPasa.
Cadenas ligeras
Las miosinas cardíacas contienen dos pares de cadenas ligeras, a menudo denominadas cadenas ligeras esenciales y reguladoras (Tabla 4-2). Estos nombres se refieren al hecho de que la extracción de las cadenas ligeras esenciales (también llamadas LC1, ELC, MLC-1 o cadenas ligeras alcalinas) inactiva la miosina, mientras que las cadenas ligeras reguladoras (también llamadas cadenas ligeras LC2, RLC, MLC-2 o DTNB o EDTA) se pueden eliminar sin abolir la actividad de la miosina ATPasa. Todas estas cadenas ligeras de miosina son miembros de la familia de proteínas de unión al calcio de la mano EF que incluye troponina C y calmodulina.
Se encuentran cinco isoformas diferentes de cadenas ligeras en la miosina auricular y ventricular humana. Dos, LC1A y LC1V, son las cadenas ligeras esenciales de la miosina auricular y ventricular, respectivamente. Las otras tres son cadenas ligeras regulatorias; dos se encuentran en los ventrículos (LC2V y LC2V*) y uno (LC2A) en las aurículas. En los ventrículos crónicamente sobrecargados, la cadena ligera esencial auricular LC1A reemplaza parte de la LC1V. La LC1A también se encuentra en los ventrículos en desarrollo. Las cadenas ligeras de miosina cardíaca humana no se unen al calcio, pero proporcionan sustratos para las fosforilaciones que regulan la velocidad de acortamiento muscular.
Actina
La actina, una proteína altamente conservada que se encuentra en todas las células eucariotas, recibió su nombre debido a su capacidad para activar la actividad de la miosina ATPasa. La actina se puede estabilizar in vitro como un monómero, llamado G-actina (G globular), o como el polímero filamentoso de F-actina (F fibroso). Tanto la actina G como la F contienen sitios de unión a nucleótidos y cationes. El nucleótido unido en la G-actina es ATP, mientras que la F-actina normalmente contiene ADP unido; En ambos, el catión unido puede ser calcio o magnesio. Los monómeros de actina, que son mucho más pequeños que la miosina (Tabla 1), son proteínas globulares ovoides de 55 Å de diámetro. El polímero, una hélice macromolecular en la que dos cadenas de monómeros de actina se enrollan una alrededor de la otra como dos cadenas de cuentas, constituye la columna vertebral de los filamentos delgados (Fig. 6) y representa uno de los tres tipos de filamento del citoesqueleto.

En el corazón humano se encuentran dos isoformas de actina, la actina α-cardíaca y la actina α-esquelética. Los ventrículos humanos adultos contienen principalmente actina α-cardíaca; actina α-esquelética, que está presente en cantidades más pequeñas, es la isoforma fetal.
Las actomiosinas reconstituidas in vitro a partir de actina y miosina purificadas pueden hidrolizar el ATP y sufrir cambios fisicoquímicos similares a los que ocurren durante la contracción muscular. Sin embargo, estas dos proteínas no están reguladas por el calcio porque carecen de la proteína reguladora.
Tropomiosina
La tropomiosina es un homodímero o heterodímero formado por dos cadenas peptídicas α helicoidales, llamadas α y β tropomiosina. Aunque esta proteína no tuvo ninguna función conocida durante los primeros 15 años después de ser purificada por primera vez, su estructura era de interés para los químicos físicos porque, al igual que la cola de la molécula de miosina, es una bobina rígida en espiral. La tropomiosina en sí misma no tiene actividad biológica, pero cuando se incorpora a las actomiosinas reconstituidas, esta proteína aparentemente inerte regula las interacciones entre la miosina y la actina. Estos efectos reguladores surgen de cambios en la posición de la tropomiosina en los surcos entre las dos cadenas de F-actina en el filamento delgado (Fig. 7). La actividad de las proteínas contráctiles cardíacas se inhibe cuando p38-MAPK, una proteína quinasa activada por mitógenos activada por estrés, hace que una serina reguladora en la tropomiosina sea desfosforilada.

El complejo troponina
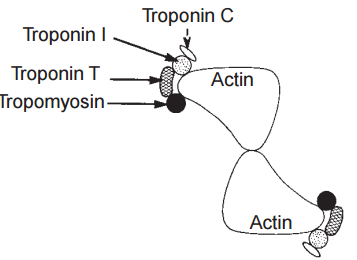
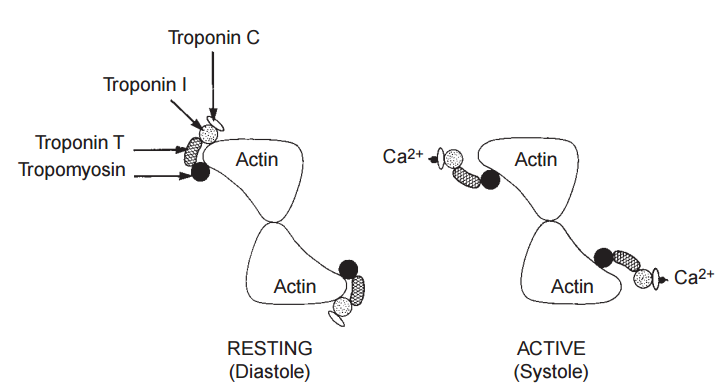
El complejo troponina incluye tres proteínas (Tabla 1) que, junto con la tropomiosina, se encuentran en los filamentos finos (Figs. 8 y 9). La troponina I recibió su nombre porque su efecto más importante es inhibir las interacciones actina-miosina, la troponina T une el complejo de troponina a la tropomiosina y la troponina C contiene los sitios de unión al calcio que participan en el acoplamiento y la relajación de la excitación-contracción.

Troponina I
Los cambios en la fuerza de un enlace lábil que une la troponina I y la actina permiten que el calcio regule la contracción cardíaca. En el corazón relajado, donde la troponina C no se une al calcio, la troponina I se une fuertemente a la actina en una conformación que hace que la tropomiosina «bloquee» los sitios de unión a la miosina de la actina. La unión del calcio a la troponina C induce un cambio alostérico en el filamento delgado que afloja el enlace que une la troponina I con la actina, lo que permite que los sitios activos de la actina interactúen con los puentes cruzados de la miosina. De esta manera, los cambios en la afinidad de unión a actina de la troponina I proporcionan un interruptor molecular que reconoce un aumento en el calcio citosólico como una señal para iniciar la contracción.
Se encuentran diferentes isoformas de troponina I en los músculos cardíacos, esqueléticos rápidos y esqueléticos lentos; se ha identificado una isoforma adicional de troponina I en el músculo en desarrollo. La troponina I cardíaca contiene una serina reguladora que, cuando es fosforilada por la proteína quinasa A [PKA, proteína quinasa dependiente de monofosfato de adenosina cíclico (AMPc)], reduce la sensibilidad al calcio de la troponina C; Esta respuesta postraduccional acelera la relajación durante la estimulación simpática al favorecer la disociación del calcio activador de las proteínas contráctiles. La proteína quinasa C (PKC) también cataliza la fosforilación de la troponina I cardíaca, pero las consecuencias de este cambio postraduccional no se comprenden bien.
Troponina T
La troponina T, el más grande de los tres componentes de la troponina, media los efectos alostéricos dentro del filamento delgado que influyen en la sensibilidad al calcio del desarrollo de la tensión. La troponina T no es un sustrato para la PKA, pero la fosforilación de la troponina T cardíaca por PKC reduce la sensibilidad al calcio, ralentiza el ciclo entre puentes y disminuye la generación de fuerza por las proteínas contráctiles cardíacas. Los cambios de isoforma que involucran a la troponina T cardíaca, que resultan del empalme alterno del gen que codifica esta proteína, modifican la contractilidad miocárdica y la sensibilidad al calcio del proceso contráctil.
Proteínas EF-Hand
La troponina C pertenece a una familia de proteínas EF-hand de unión al calcio intracelular que incluye las cadenas ligeras de miosina y la calmodulina. Todos contienen cuatro cadenas peptídicas de 30 aminoácidos en las que dos regiones helicoidales, designadas E y F, están separadas por una corta secuencia no helicoidal. El término mano EF refleja el hecho de que estas hélices, que evolucionaron por duplicación y modificación del gen que codificaba la proteína ancestral de la mano EF, se asemejan al dedo índice extendido y al pulgar de una mano derecha (Fig. 10). Esta estructura incluye varios aminoácidos que contienen oxígeno y forman una «bolsa» aniónica que se une a los iones de calcio con muy alta afinidad. Las sustituciones de aminoácidos en estas regiones de unión al calcio han hecho que algunos miembros de esta familia pierdan su capacidad de unirse al calcio; en otros, la especificidad del calcio, en relación con el magnesio, se perdió.

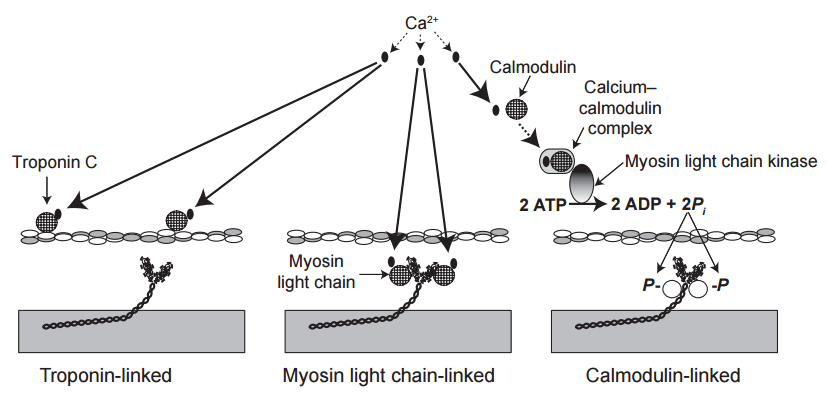
Varios mecanismos permiten que diferentes proteínas EF-hand activen la contracción muscular en respuesta a un aumento del calcio citosólico (Fig. 11). En el corazón y el músculo esquelético de los mamíferos, la troponina C, una proteína de la mano EF ubicada en el filamento delgado, provoca un reordenamiento de las proteínas reguladoras cuando se une al calcio activador. En algunos otros músculos, como el aductor de la vieira, la contracción se activa cuando el calcio se une a una cadena ligera de miosina EF-hand en lugar de troponina C. En el músculo liso vascular, el calcio se une a la calmodulina, una proteína soluble de la mano EF, en lugar de una proteína de la mano EF en los miofilamentos; el complejo calcio-calmodulina resultante activa una quinasa de cadena ligera de miosina (MLCK) que inicia la contracción mediante la fosforilación de una cadena ligera de miosina de músculo liso. La capacidad de esta última, que es una proteína EF-hand que ha perdido la capacidad de unirse al calcio, para estimular la contracción cuando se fosforila en respuesta a una señal mediada por el calcio ilustra cómo varios miembros de una sola familia de proteínas pueden realizar funciones similares pero de diferentes maneras.
Troponina C
La troponina C es una molécula con forma de mancuerna que contiene cuatro secuencias de aminoácidos EF-hand (Fig. 12). Algunas de estas secuencias se unen solo al calcio y, por lo tanto, se designan como sitios específicos del calcio, mientras que otras, llamadas sitios de calcio y magnesio, también se unen al magnesio. Debido a que la concentración de magnesio ionizado en la mayoría de las células es mucho más alta que la del calcio, los sitios de calcio-magnesio no pueden mediar las señales que se inician por pequeños cambios en el calcio citosólico porque permanecen ocupados por el magnesio. Por esta razón, solo los sitios específicos de calcio son capaces de reconocer un aumento en la concentración de calcio citosólico como una señal para activar la contracción.
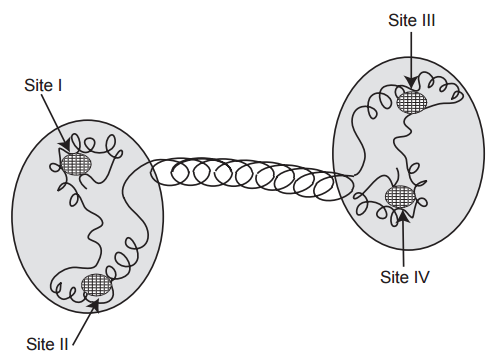
En el músculo estriado de los mamíferos se encuentran tres isoformas de troponina C: la troponina C cardíaca y la troponina C esquelética rápida y lenta. Todos contienen dos sitios específicos de calcio (sitios I y II) y dos sitios de calcio-magnesio (sitios III y IV). En la troponina C cardíaca, dos residuos de ácido aspártico cargados negativamente en el sitio I son reemplazados por leucina y alanina, lo que hace que este sitio pierda su capacidad de unirse al calcio con alta afinidad. Por esta razón, sólo el sitio II, el otro sitio específico del calcio, es capaz de servir como receptor fisiológico de calcio de las proteínas contráctiles cardíacas.
Calmodulina
La calmodulina, que contiene cuatro regiones EF-mano, responde a un aumento del calcio citosólico formando un complejo calcio-calmodulina en el que una región hidrofóbica queda expuesta en la superficie de la molécula de calmodulina. Una vez expuesta, esta superficie hidrofóbica puede interactuar con dominios hidrofóbicos en otras proteínas, incluidos los miembros de una familia de proteínas quinasas llamadas quinasas de calcio-calmodulina (quinasas CaM) que participan en la señalización celular mediante la catalización de una variedad de fosforilaciones reguladoras. Como se señaló anteriormente, MLCK, una de las quinasas CaM, regula la contracción en el músculo liso vascular.
Actomiosina
Debido a que la insolubilidad de las proteínas contráctiles dificultaba el estudio de la cinética de su enzima ATPasa, los primeros bioquímicos musculares fueron vistos con desdén por aquellos cuyos elegantes estudios de la cinética de las enzimas solubles representaban el «estado del arte» en bioquímica. ¡Se prestó poca atención al hecho de que un músculo soluble sería de poca utilidad para desarrollar tensión! Sin embargo, las combinaciones de actina y miosina, llamadas actomiosina, proporcionaron sorprendentes modelos in vitro de contracción muscular. En la década de 1940, A. Szent-Györgyi descubrió que la adición de ATP hace que los hilos de actomiosina reconstituidos a partir de miosina y F-actina se acorten y, si se adjunta una carga, realicen trabajos e incluso generen curvas hiperbólicas de fuerza-velocidad. Otra observación fascinante fue que la adición de grandes cantidades de ATP a suspensiones lechosas de partículas insolubles de actomiosina fue seguida por una respuesta bifásica: la suspensión inicialmente se volvió clara, después de lo cual apareció una nube de partículas más pequeñas y densas. La centrifugación a baja velocidad de las suspensiones inicial y final reveló que el ATP había disminuido el volumen del pellet porque las partículas de actomiosina se habían encogido, de la misma manera que una esponja en contracción podría exprimir el agua de sí misma. Este experimento demostró que el ATP tiene dos efectos sobre las proteínas contráctiles; a altas concentraciones, el ATP tiene un efecto «plastificante» que disocia la miosina y la actina, por lo que las suspensiones de actomiosina se hicieron inicialmente claras. Las partículas de actomiosina reaparecieron porque la actividad de la ATPasa de la miosina disociada había disminuido la concentración de ATP, lo que permitió que la miosina se recombinara con la actina, después de lo cual las partículas se encogieron cuando el ATP energizó las interacciones entre la actina y la miosina análogas a las que ocurren durante la contracción muscular.
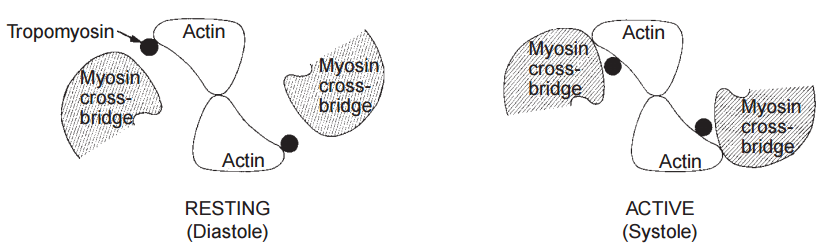
Los dos efectos del ATP descritos anteriormente (disociar la actina y la miosina, lo que facilita la relajación, y energizar las interacciones entre la actina y la miosina que causan la contracción) ocurren en el corazón vivo. Durante la diástole, el efecto plastificante del ATP inhibe las interacciones entre filamentos gruesos y finos disociando la miosina y la actina, mientras que durante la sístole, el ATP que se hidroliza cuando el sitio catalítico de la miosina es activado por la actina proporciona energía para la contracción.
En la década de 1950, cuando se reconoció que el calcio era el activador fisiológico de la contracción, se descubrió que las actomiosinas reconstituidas a partir de actina y miosina altamente purificadas permanecían activas después de que poderosos quelantes de calcio redujeran las concentraciones de calcio ionizado casi a cero. Esta sorprendente observación estimuló una búsqueda del receptor de calcio de las proteínas contráctiles que terminó con el descubrimiento de las funciones de la tropomiosina y el complejo troponina. Se encontró que la inclusión de estas proteínas reguladoras en las actomiosinas reconstituidas permite la eliminación de calcio para inhibir las manifestaciones in vitro de la contracción descritas anteriormente. La capacidad del calcio para revertir esta inhibición documentó dos características esenciales del control fisiológico de las interacciones actina-miosina por el calcio: que las proteínas reguladoras son inhibidoras a bajas concentraciones de calcio, y que el calcio estimula la contracción al revertir este efecto inhibidor.
Calcio como mensajero intracelular
El calcio media una serie de señales intracelulares, generalmente sirviendo como activador cuando se une a una de las proteínas de la mano EF descritas anteriormente. En el músculo, la señalización del calcio representa el paso final en el acoplamiento excitación-contracción, el proceso por el cual la despolarización de la membrana plasmática activa la contracción. El calcio desempeña un papel similar en el control del acoplamiento de excitación-secreción, el flujo citoplasmático y el movimiento de cilios y flagelos.
Una serie de hipótesis planteadas por Kretsinger (1979) explica cómo el calcio podría haberse convertido en un mensajero intracelular. Estos se centran en la muy baja concentración de calcio ionizado dentro de las células eucariotas, que es aproximadamente 10.000 veces más baja que la de los fluidos circundantes. La concentración de calcio citosólico en los miocitos cardíacos en reposo es de 0,2 μM, mientras que la concentración de calcio en la sangre y el espacio extracelular, como el agua de mar, está en el rango milimolar. Kretsinger, al notar la baja solubilidad del fosfato de calcio, sugirió que el calcio se excluyó inicialmente del citosol para permitir que las células retuvieran el fosfato necesario para sintetizar ATP, ácidos nucleicos, fosfoazúcares y otras moléculas clave. Con la evolución de las bombas e intercambiadores de iones dependientes de la energía que podían transportar calcio cuesta arriba, fuera del citosol, la entrada pasiva de pequeñas cantidades de este catión a través de los canales de la membrana plasmática proporcionó un mecanismo útil para la transducción de señales. Además de servir como una señal química reconocida por las proteínas EF-hand, la afluencia de iones de calcio cargados positivamente genera una señal eléctrica al despolarizar la membrana plasmática (ver Capítulo 13). Aunque especulativo, este escenario es útil para comprender el papel de señalización de la afluencia de calcio en el citosol.
Respuesta de las proteínas contráctiles al calcio
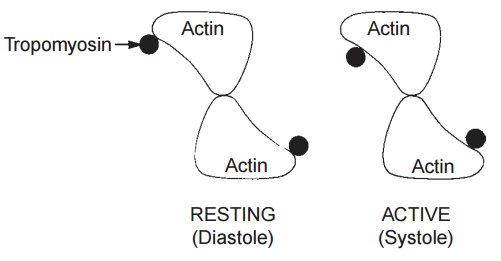
La unión del calcio a la troponina C regula las interacciones entre la actina y la miosina iniciando una serie de interacciones cooperativas entre las proteínas del filamento delgado que cambian la posición de la tropomiosina en el filamento delgado (Fig. 13). En el corazón relajado, donde la troponina C no se une al calcio, la tropomiosina se encuentra hacia el exterior de las ranuras del polímero de F-actina de doble cadena, donde evita que los sitios activos de la actina interactúen con los puentes cruzados de miosina. La unión del calcio a la troponina C debilita el enlace que conecta la troponina I con la actina (ver arriba), lo que desplaza a la tropomiosina lejos de su posición de «bloqueo» (Fig. 14) y permite que la actina interactúe con los puentes cruzados de miosina (Fig. 15). El músculo se relaja cuando la eliminación del calcio de la troponina C devuelve la tropomiosina a su posición inhibitoria en el filamento delgado.
Además de proporcionar un interruptor de «encendido-apagado» que inicia la contracción, la tropomiosina y el complejo de troponina regulan la intensidad de la respuesta contráctil. La relación longitud-tensión y la ley del corazón de Starling se deben en parte a la capacidad de los cambios en la longitud del sarcómero para modificar la sensibilidad al calcio de las proteínas contráctiles. Una serie de otras modificaciones postraduccionales de las proteínas del filamento delgado varían las interacciones entre las proteínas contráctiles; estos incluyen la fosforilación de troponina I, que facilita la relajación al reducir la sensibilidad al calcio de las proteínas contráctiles cardíacas (ver arriba), la fosforilación de troponina T que modifica la generación de fuerza, y un efecto alostérico que reduce la contractilidad cuando los protones se unen a la troponina I en corazones acidóticos. Los cambios de isoforma y las mutaciones que involucran a las proteínas del filamento delgado también tienen efectos importantes en el rendimiento cardíaco.
Bioquímica de la contracción
¿Es el ATP esencial para la contracción o para la relajación?
Los efectos aparentemente contradictorios del ATP para disociar las suspensiones de actomiosina y hacer que se contraigan se observan en el músculo vivo, donde la hidrólisis del enlace terminal de fosfato de alta energía del ATP proporciona la energía para la contracción, y el agotamiento severo de ATP causa rigor. Estas y otras observaciones llevaron a los primeros investigadores a preguntarse si la función principal del ATP es hacer que el músculo se contraiga o se relaje. Una respuesta se centró en el papel del ATP en la contracción:
Actina + miosina (relajada) + ATP ➡️ actomiosina (activa) + ADP + Pi
El segundo, que enfatizó el papel del ATP en la relajación, destacó la capacidad del ATP para disociar la actina y la miosina:
Actomiosina (activo) + ATP ➡️ actina + miosina-ATP (relajado)
Ahora está claro que ambos mecanismos operan cuando el corazón se contrae y se relaja, y que este doble papel refleja la interacción del ATP y sus productos hidrolíticos, ADP y Pi, con las proteínas contráctiles. Estos se pueden entender examinando las funciones de ATP, ADP y Pi durante la secuencia de reacciones entre actina y miosina que ocurren durante cada ciclo cardíaco. La siguiente discusión comienza con la reacción más simple de la ATPasa de la miosina sola, que luego se contrasta con la de la actomiosina para aclarar las interacciones entre las proteínas contráctiles que hacen que el corazón se contraiga y se relaje.
Reacción de la miosina ATPasa
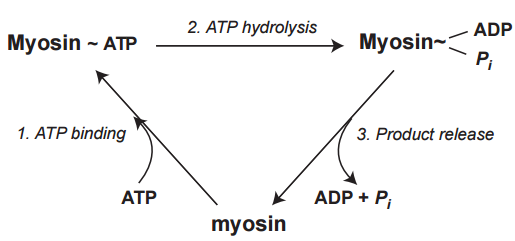
La miosina se une al ATP con alta afinidad para formar un complejo miosina-ATP en el que la energía química del nucleótido permanece en su fosfato terminal (paso 1, Fig. 16). El siguiente paso, la hidrólisis de ATP por el sitio enzimático de la miosina (paso 2, Fig. 17), no disocia inmediatamente los productos; en su lugar, se forma un complejo energizado en el que ADP y Pi permanecen unidos a la miosina. La lenta disociación de ADP y Pi de la miosina, que devuelve a esta última a su estado basal (paso 3, Fig. 16) es limitante de la baja actividad de la ATPasa de la miosina sola.
Reacción a la ATPasa de actomiosina: el ciclo de puente cruzado
La actina aumenta la actividad de la miosina ATPasa cuando interactúa con la miosina energizada que está unida a ADP y Pi (paso 3 en la Fig. 16, que es limitante de velocidad). La actina convierte la baja actividad de la miosina ATPasa en la mayor actividad de la ATPasa de la actomiosina acelerando la disociación de estos productos de reacción de la miosina.
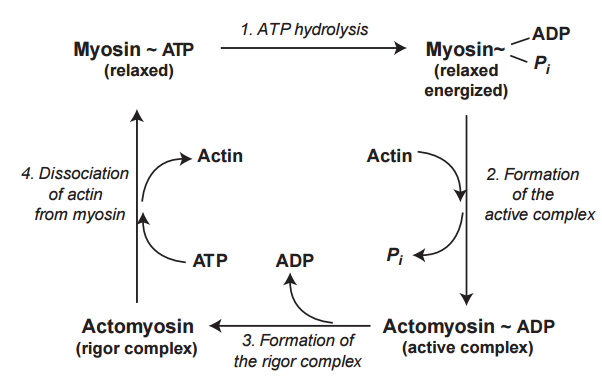
Las reacciones clave del ciclo de puentes cruzados se pueden resumir en cuatro pasos: dos en los que la actina y la miosina se separan (relajados y relajados, energizados), y dos en los que los puentes cruzados de miosina se unen a la actina (complejos activos y de rigor) (Figs. 17 y 18). En ambos casos, donde la miosina se une a ATP o a ADP y Pi, el músculo está relajado porque los puentes cruzados no están unidos a la actina. Los dos estados en los que los puentes cruzados están unidos a la actina son bastante diferentes entre sí. En el complejo activo, la energía de ATP permanece en el puente cruzado, mientras que la formación del complejo de rigor, que se encuentra en un estado de baja energía, gasta la energía química del complejo activo para cambiar la posición del puente cruzado unido a actina.
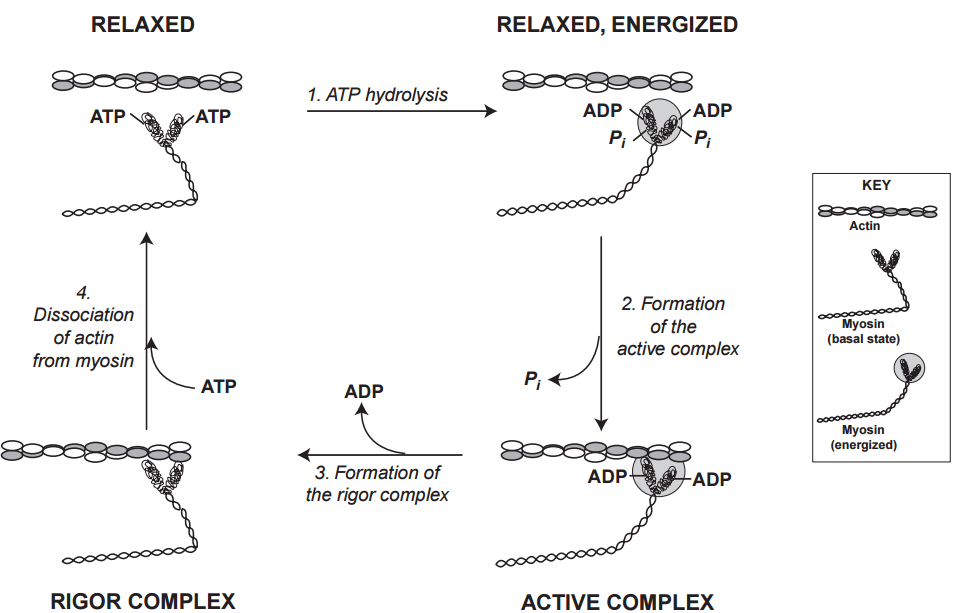
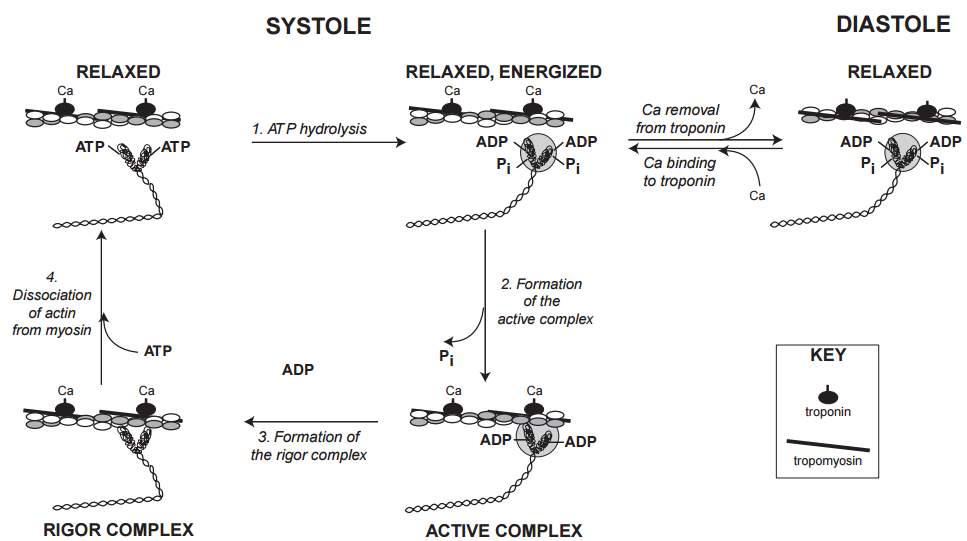
Al elegir dónde entrar en el ciclo de puentes cruzados, seguimos la convención de la fisiología, que comienza el ciclo cardíaco en la diástole. Esta descripción, por lo tanto, comienza con el corazón en el estado relajado, donde la unión del ATP a la miosina ha disociado el puente cruzado del filamento delgado. Los cuatro pasos que se muestran en la Figura 17 son: (1) hidrólisis del ATP unido a la miosina, (2) formación del complejo activo con actina y liberación de Pi, (3) formación del complejo de rigor y liberación de ADP, y (4) disociación de actina y miosina. Las actomiosinas que carecen de las proteínas reguladoras permanecen activas incluso a concentraciones muy bajas de calcio, por lo que el ciclo de puente cruzado continúa siempre que haya un suministro adecuado de ATP.
Paso 1. Hidrólisis del ATP unido a la miosina
La alta concentración de ATP en el corazón en reposo forma un complejo miosina-ATP relajado que disocia los filamentos gruesos y delgados (Figs. 17 y 18), después de lo cual continúa el ciclo de puente cruzado cuando el sitio catalítico de la miosina hidroliza el ATP unido a la miosina. Este paso transfiere la energía del enlace terminal de fosfato del ATP a la miosina, donde la energía en el complejo relajado-energizado permanece en el puente cruzado y, por lo tanto, no se ha utilizado para realizar el trabajo. Como ocurre durante la reacción de la miosina ATPasa (ver arriba), los productos hidrolíticos, ADP y Pi inicialmente permanecen unidos a la miosina.
Paso 2. Formación del complejo activo con actina y liberación de Pi
La interacción de la actina con el puente cruzado relajado-energizado forma un complejo activo entre la actina y la miosina que libera Pi. Aunque el puente cruzado de miosina está unido a la actina en este complejo activo, la energía liberada por la hidrólisis de ADP no se ha gastado para realizar el trabajo, sino que permanece en el complejo actina-miosina-ADP. Esta energía se libera en el siguiente paso, lo que energiza el movimiento de puente cruzado que tira del filamento delgado hacia el centro del sarcómero.
Paso 3. Formación del complejo de rigor con actina y liberación de ADP
El corazón realiza un trabajo mecánico cuando la liberación del ADP unido a la miosina permite que la energía del complejo activo cambie la posición del puente cruzado. Esto forma el complejo de rigor en el que el puente cruzado de miosina, todavía firmemente unido a la actina, se encuentra en un estado de baja energía. Por lo tanto, el complejo de rigor es muy diferente del complejo activo. La liberación de ADP de la actomiosina, al igual que la liberación de ADP de la miosina (ver arriba), es limitante de la velocidad en el ciclo de puente cruzado.
Los complejos de rigor persisten cuando un músculo se queda muy sin energía. En el músculo esquelético, esta es la causa del rigor mortis, mientras que en el corazón, la formación de enlaces de rigor causa contractura isquémica. Antes del desarrollo de agentes cardiopléjicos eficaces, que detienen el corazón en un estado relajado durante la cirugía a corazón abierto mediante la inhibición de las interacciones actina-miosina, a veces aparecía una contractura isquémica irreversible durante el bypass cardiopulmonar prolongado (el «síndrome del corazón de piedra»). Menos dramática, pero más común clínicamente, es la disminución de la distensibilidad diastólica causada por la formación de enlaces de rigor en corazones isquémicos hambrientos de energía y corazones en falla.
Paso 4. Disociación de actina y miosina
La finalización del ciclo de puente cruzado requiere que el ATP se una nuevamente a la miosina. Esto ocurre en una reacción rápida en la que la reunión del ATP al complejo de rigor separa los enlaces que unen el puente cruzado con el filamento delgado. La disociación del complejo de rigor explica el efecto «plastificante» del ATP descrito anteriormente.
Papel del ATP en la contracción y la relajación
Las reacciones del ciclo de puentes cruzados que se muestran en las figuras 17 y 18 explican dos formas en que el ATP participa en la contracción y la relajación: la hidrólisis del ATP por miosina activada por actina energiza la contracción (pasos 1-3), mientras que la unión del ATP a la miosina es esencial para la relajación (paso 4). Se necesitan altas concentraciones de ATP, en el rango milimolar, para disociar los puentes cruzados de la actina, mientras que se necesitan niveles micromolares de ATP mucho más bajos para energizar la actividad de la miosina ATPasa.
La capacidad del ATP para relajar el corazón no requiere el gasto de energía de enlace de fosfato, como lo demuestra la capacidad de los análogos de ATP no hidrolizables para disociar la actina y la miosina in vitro. Por el contrario, se requiere la hidrólisis del enlace de fosfato de alta energía del ATP para el ciclo entre puentes.
Regulación del ciclo de puentes cruzados por calcio
Al ciclo de puentes cruzados que se muestra en las figuras 17 y 18 se deben agregar dos pasos para explicar el papel del calcio en la activación de la contracción cardíaca. En el primero, que mantiene el corazón en un estado relajado, el calcio se elimina de la troponina C, lo que permite que la tropomiosina y el complejo troponina eviten que la actina interactúe con la miosina (Fig. 19, derecha). Esto detiene el ciclo en el paso donde los puentes cruzados de miosina se energizan pero no se unen a los filamentos delgados. En el segundo, la unión del calcio a la troponina C permite que el ciclo se reanude porque las proteínas reguladoras ya no impiden que los puentes cruzados interactúen con la actina.
El ciclo de puentes cruzados también puede modificarse mediante cambios de isoformas que involucran las cadenas pesadas de miosina que alteran las interacciones cooperativas entre las proteínas del filamento delgado, y por cambios postraduccionales como la fosforilación de la cadena ligera de miosina.
Regulación del ciclo de puente cruzado por carga
Hill interpretó su observación de que la tasa de liberación de energía al contraer el músculo es inversamente proporcional a la carga, ya que la evidencia sugiere que la carga determina la distribución de los «puntos activos» entre dos estados diferentes: uno en el que circulan libremente pero no desarrollan tensión, el otro en el que mantienen la tensión pero no lo hacen. En la siguiente discusión, estos diferentes estados se explican en términos del ciclo entre puentes.
Puntos activos liberadores de energía química
La clave para entender la base bioquímica de la observación de Hill de que la tasa de liberación de energía es máxima cuando el músculo se contrae a carga cero la proporcionó el hallazgo de que la velocidad máxima de acortamiento (Vmax) de diferentes músculos se correlaciona estrechamente con la actividad ATPasa de sus miosinas (Bárány, 1967). Esto indicó que la velocidad máxima a la que los «hombrecitos» pueden correr a carga cero (Fig. 17) corresponde al paso 3 en el ciclo de puente cruzado (Figs. 18 y 19), que es el paso limitante de velocidad donde se libera ADP de la miosina. Siempre que se permita que los puentes cruzados circulen libremente, Vmax en un músculo dado es proporcional a la tasa de hidrólisis de ATP por su miosina purificada.
Puntos activos que mantienen la tensión
La capacidad de aumentar la carga para ralentizar la tasa de liberación de energía puede explicarse porque el aumento de la carga inhibe la ruptura de los enlaces de rigor que unen la miosina y la actina, lo que ralentiza el movimiento de los puentes cruzados a lo largo de los filamentos delgados. La estabilización de los enlaces de rigor inhibe la disociación de la actina y la miosina (paso 4 en el ciclo de puente cruzado mostrado en las Figs. 18 y 19); esto es análogo a atar a un grupo de «hombrecitos» a un poste para evitar que sus pies se muevan (Fig. 16). Esta analogía ayuda a explicar por qué los determinantes de la tasa de ciclado entre puentes no son los mismos que los que determinan la fuerza de los enlaces de rigor, y por qué la velocidad máxima de acortamiento a carga cero (Vmax) no se correlaciona con la tensión isométrica máxima (P0). El número de puentes transversales activos no influye en la velocidad máxima de acortamiento a carga cero por la misma razón que el cambio en el número de «hombrecitos» no modifica la velocidad a la que el grupo puede correr cuando la cuerda se rompe (Fig. 19).
La curva fuerza-velocidad
La discusión anterior explica por qué las intersecciones de la curva fuerza-velocidad (Fig. 15) están determinadas por diferentes propiedades de las proteínas contráctiles. La tensión isométrica máxima (P0), que está determinada por el número de enlaces de rigor entre los puentes cruzados y la actina, refleja el número de moléculas de troponina C unidas al calcio. Por esta razón, la cantidad de calcio liberada durante el acoplamiento excitación-contracción y la afinidad cálcica de la troponina son los principales determinantes de P0. Por otro lado, la velocidad máxima de acortamiento (Vmax) está determinada por la tasa de rotación de los ciclos entre puentes y, por lo tanto, es independiente del número de puentes cruzados activos siempre que la carga sea cero. El reclutamiento de interacciones adicionales entre actina y miosina aumenta el P0, pero no puede aumentar la velocidad de acortamiento en un músculo descargado. Está claro que dos mecanismos independientes, el número de puentes cruzados activos y su tasa de recambio, determinan la contractilidad miocárdica, que puede definirse como la capacidad del corazón para realizar el trabajo en cualquier longitud de reposo. Es necesario considerar solo los diferentes tipos de cuerpo de los levantadores de pesas y velocistas de clase mundial para darse cuenta de que estos no tienen por qué estar estrechamente relacionados entre sí.