Venid a mí ahora, musas que vivís en el Olimpo, porque sois diosas, estáis en todas partes y sabéis todas las cosas, mientras que nosotros sólo oímos hablar de la gloria, pero no la conocemos verdaderamente. ¿Quiénes eran los líderes de los griegos, quiénes los gobernantes? No podría decir los nombres ni el número de todos los hombres, aunque tuviera diez lenguas, diez bocas, una voz incansable y un corazón de bronce, a menos que vosotras, musas olímpicas, hijas de Zeus que lleváis la égida, me recordéis a los hombres que vinieron a Troya, así que ahora contaré a los jefes de las naves, y todos sus números.
—Homero (Ilíada. Libro 2, 484-493. tr. P.B. Katz)
Al igual que el Libro 2 de la Ilíada de Homero, este capítulo incluye una lista de las muchas proteínas del citoesqueleto que se encuentran en los miocitos cardíacos. Como ocurre con cualquier lista, el papel y la importancia de cada entrada pueden ser difíciles de apreciar. Sin embargo, los descubrimientos realizados en la última década han dejado claro que las proteínas del citoesqueleto son importantes en la patogénesis de las enfermedades humanas; Generan y transmiten señales desadaptativas que contribuyen al deterioro progresivo de los corazones indecisos, y se han identificado mutaciones en muchas de estas proteínas como causas de miocardiopatías y muerte súbita cardíaca. Las siguientes páginas están destinadas a proporcionar una breve introducción a muchas de estas proteínas, junto con un marco mediante el cual se pueden organizar estas importantes moléculas. Debido a que los objetivos generales de este texto introductorio requieren que las descripciones de cada proteína sean breves.
Los miocitos cardíacos no son simplemente bolsas llenas de líquido en las que las enzimas y los orgánulos celulares como los miofilamentos, el retículo sarcoplásmico, los núcleos y las mitocondrias flotan libremente en el citosol; En cambio, una arquitectura celular compleja es mantenida por un marco de proteínas llamado citoesqueleto. Al igual que las vigas de un edificio moderno, estas proteínas estructurales mantienen los constituyentes celulares en su lugar, organizan proteínas funcionalmente relacionadas y facilitan las interacciones mecánicas con las células adyacentes y la matriz extracelular. Además de estas funciones estructurales, el citoesqueleto participa en la señalización celular y hace una contribución importante a las vías de transducción de señales que modifican el tamaño y la forma del corazón. El citoesqueleto, por lo tanto, no es simplemente un sistema de vigas que mantiene la forma de la célula; Debido a su papel en la señalización celular, el citoesqueleto se ve con mayor precisión como un marco estructural que también sirve como un sistema telefónico.
En los miocitos cardíacos, el citoesqueleto organiza las relaciones espaciales entre las estructuras intracelulares, transmite la tensión desarrollada por las proteínas contráctiles de un sarcómero a otro y a la superficie celular, y une las células con otras células y con la matriz extracelular. El citoesqueleto también ayuda al corazón a adaptar su arquitectura en respuesta a la deformación celular y a los cambios en el estrés mecánico. Al modificar el tamaño, la forma y la composición del corazón, la señalización del citoesqueleto desempeña un papel clave en la adaptación de la forma a la función. Esto se observa en la activación de vías de señalización específicas por varios tipos de deformación del citoesqueleto, lo que contribuye a la aparición de diferentes fenotipos de hipertrofia cardíaca y ayuda a explicar por qué la sobrecarga de presión causa hipertrofia concéntrica (observada en la estenosis aórtica donde se aumenta el estrés sistólico), y la sobrecarga de volumen causa hipertrofia excéntrica (como ocurre en la insuficiencia aórtica donde se aumenta el estrés diastólico). Estas respuestas proliferativas son especialmente importantes en los corazones indecisos, donde la señalización del citoesqueleto contribuye a los diferentes tipos de hipertrofia inducida por sobrecarga. Aunque inicialmente son beneficiosas, estas respuestas proliferativas generalmente se vuelven desadaptativas cuando la sobrecarga se mantiene. La señalización del citoesqueleto desempeña un papel en la determinación del pronóstico de la insuficiencia cardíaca sistólica, donde la señalización transcripcional deletérea contribuye a la dilatación ventricular progresiva, llamada remodelación, que acorta la supervivencia. Por estas razones, las proteínas del citoesqueleto pueden servir como dianas para la terapia dirigida a modificar las respuestas de crecimiento desadaptativas en corazones enfermos. También es probable que los fármacos que pueden modificar el comportamiento de estas proteínas ayuden a los pacientes con miocardiopatías familiares, muchas de las cuales son causadas por mutaciones en las proteínas del citoesqueleto.
Las funciones mecánicas y de señalización del citoesqueleto son posibles gracias a las interacciones entre docenas de proteínas. Algunas de estas proteínas son en gran medida estructurales, mientras que otras proteínas asociadas con el citoesqueleto, incluidas las proteínas quinasas, las fosfatasas y los factores de transcripción, funcionan principalmente en la transducción de señales. Sin embargo, muchas proteínas del citoesqueleto cumplen funciones mecánicas y de señalización, por lo que las designaciones «estructural» y «señalización» en la siguiente discusión son arbitrarias. En muchos sentidos, estas proteínas son como las ruedas delanteras de un automóvil, que sujetan el vehículo a la carretera y participan en la dirección.
Filamentos citoesqueléticos
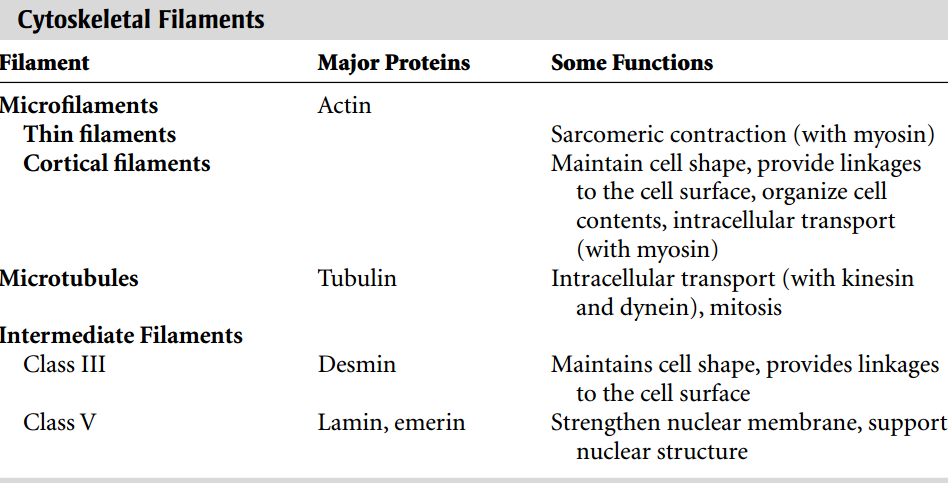
El citoesqueleto contiene tres tipos de fibra intracelular (Tabla 1). Los microfilamentos de actina se encuentran en dos estructuras: los filamentos finos de los sarcómeros y los microfilamentos. Estos últimos conectan las proteínas contráctiles, la membrana plasmática y otros elementos del citoesqueleto entre sí, conectan el citoesqueleto con la matriz extracelular y anclan las células entre sí. Los microtúbulos, que están formados principalmente por tubulina, transportan orgánulos y estructuras vesiculares dentro de los miocitos cardíacos y participan en la mitosis que ocasionalmente se observa en estas células terminalmente diferenciadas. Matrices especializadas de microtúbulos participan en los movimientos de cilios y flagelos, pero estos no se encuentran en los miocitos cardíacos adultos. El corazón contiene dos tipos de filamentos intermedios. Los filamentos intermedios de clase III contienen desmina y forman fuertes estructuras en forma de remache, llamadas desmosomas, que ayudan a mantener la arquitectura celular, vincular las células entre sí y unir las células a la matriz extracelular. Los filamentos intermedios de clase V, que contienen lamina, sostienen la membrana nuclear. A diferencia de los microfilamentos y los microtúbulos, los filamentos intermedios no participan en el movimiento celular ni en el transporte intracelular. Sin embargo, todas estas fibras del citoesqueleto participan en la señalización celular.
Proteínas del citoesqueleto asociadas a los miofilamentos
Nuestra visión del sarcómero ha cambiado drásticamente desde la década de 1950, cuando se propuso por primera vez la hipótesis del filamento deslizante para la contracción muscular. En ese momento, se pensaba que los sarcómeros estaban formados por dos proteínas, actina y miosina; En la década de 1970, después de que se reconocieran las funciones de la tropomiosina y el complejo troponina, este número aumentó a seis. Sin embargo, los estudios clásicos de Huxley y Hanson (1960) demostraron que aunque las bandas A desaparecían cuando la miosina se extraía de las fibras musculares, y que la extracción posterior de la actina eliminaba las bandas I, la eliminación de estas proteínas no causaba que las fibras se deshicieran. En cambio, los sarcómeros permanecieron intactos y las líneas Z conservaron su alineación normal. Durante casi 30 años, estas observaciones, aunque no se olvidaron, generalmente se pasaron por alto. No fue hasta la década de 1990 que se apreció el papel de las proteínas del citoesqueleto, que mantuvieron la estructura del sarcómero después de que se eliminaron las proteínas contráctiles. Inicialmente, se creía que el citoesqueleto simplemente proporcionaba un soporte mecánico que ayudaba a mantener la estructura del sarcómero y transmitir la tensión desarrollada por las proteínas contráctiles a los sarcómeros adyacentes, otros miocitos y la matriz extracelular. Sin embargo, ahora está claro que las proteínas del citoesqueleto también regulan las longitudes de los filamentos gruesos y delgados y cumplen una serie de funciones de señalización vitales. Aún más importante clínicamente ha sido el reconocimiento de que las alteraciones de estas funciones de señalización son importantes en las enfermedades humanas.
Proteínas del citoesqueleto de los filamentos gruesos
Los filamentos gruesos, que alguna vez se pensó que estaban compuestos completamente de miosina, ahora se sabe que contienen una serie de proteínas del citoesqueleto. Algunos se incorporan a estos filamentos donde se unen directamente a la miosina. Un número aún mayor de proteínas del citoesqueleto forman agregados que unen los filamentos gruesos a las estructuras cercanas y participan en la señalización celular. La complejidad resultante dificulta la creación de imágenes visuales que describan las interacciones entre estas proteínas; Por este motivo, las siguientes descripciones de estas interacciones utilizan diagramas y listas.
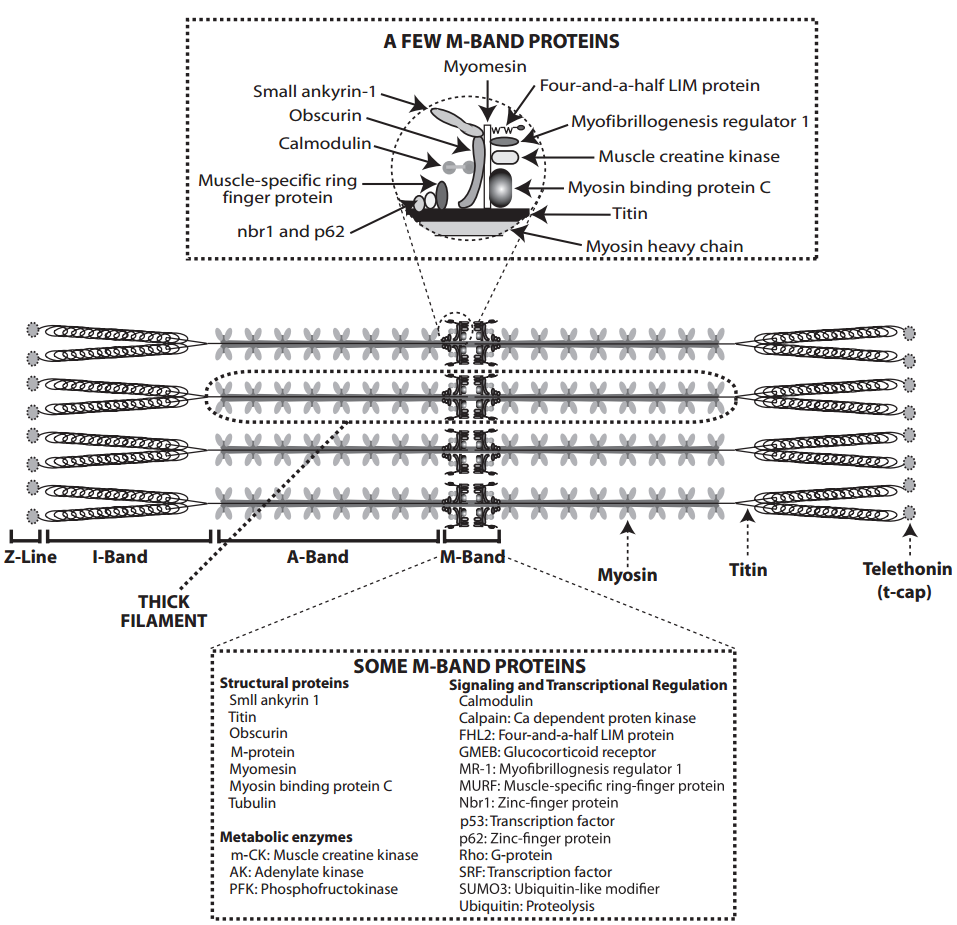
La titina, una enorme proteína con un peso molecular de 3.000.000 que se extiende desde las líneas Z hasta el centro del filamento grueso (Fig. 1), apoya la estructura sarcomérica y contribuye a la alta rigidez en reposo del miocardio. Las regiones de titina que se incorporan a los filamentos gruesos añaden rigidez a estas estructuras, mientras que una región más dócil en las bandas I contribuye a la elasticidad del corazón. La fosforilación de la titina por PKA reduce la rigidez del sarcómero y, por lo tanto, facilita el llenado ventricular cuando se aumenta la actividad adrenérgica, como durante el ejercicio.
Dos isoformas de titina, N2B y N2BA, que difieren en la región flexible de la molécula, se encuentran en los ventrículos humanos adultos. El N2BA, que normalmente es la isoforma dominante, es más obediente que el N2B. Los pacientes con insuficiencia cardíaca con ventrículos izquierdos dilatados («insuficiencia cardíaca sistólica») sobreexpresan la isoforma N2BA más cumplidora, mientras que aquellos cuyos ventrículos izquierdos son rígidos y tienen cavidades más pequeñas («insuficiencia cardíaca diastólica») tienen un mayor contenido de la isoforma N2B más rígida. Las mutaciones en la titina se asocian con miocardiopatías dilatadas e hipertróficas.
La titina forma fibras transversales con una serie de otras proteínas del citoesqueleto en las bandas M en el centro de los filamentos gruesos (Fig. 1). Estos incluyen la proteína C de unión a miosina (proteína C), la proteína M y la miomesina, que proporcionan estabilidad mecánica lateral al sarcómero, y la creatina quinasa muscular, la adenilato quinasa y la fosfofructoquinasa, que pueden participar en modificaciones dependientes de la longitud de la producción de energía. La oscurina, otra proteína de banda M unida a la titina, conecta los sarcómeros con el retículo sarcoplásmico a través de una pequeña anquirina-1. La ubiquitina y el modificador similar a la ubiquitina SUMO3 regulan la degradación de proteínas. Otras proteínas de banda M participan en la señalización celular; estos incluyen calmodulina, regulador de miofibrilogénesis 1, proteína LIM de cuatro y medio (FHL), los factores de transcripción p53, proteína del dedo anular específico del músculo (MURF-1) y las dos proteínas de dedo de zinc (NBR1 y p62). Las proteínas de banda M proporcionan un ejemplo de un «punto caliente» donde las interacciones entre las proteínas estructurales y reguladoras generan respuestas proliferativas.
Las interacciones entre las proteínas del citoesqueleto que se muestran en la Figura 5-1 sugieren varias formas en que las proteínas de la banda M podrían mediar respuestas específicas a la deformación celular. Por ejemplo, MURF, FHL y las dos proteínas de dedo de zinc (nbr1 y p62) regulan la transcripción génica y la síntesis de proteínas, lo que podría permitir que estas proteínas del citoesqueleto modifiquen el tamaño, la forma y la composición del corazón en respuesta a tensiones mecánicas anormales. Las interacciones de las proteínas de la banda M con la obscurina, la anquirina-1 pequeña y el retículo sarcoplásmico podrían contribuir a cambios dependientes de la longitud en la liberación de calcio por estas membranas internas.
Las diferentes respuestas de las proteínas del citoesqueleto orientadas paralela y perpendicularmente al eje largo del sarcómero probablemente expliquen por qué el estiramiento transversal y longitudinal de los miocitos cardíacos evoca diferentes respuestas focales de adhesión quinasa (Senyo et al., 2007), y la activación de diferentes proteínas quinasas activadas por mitógenos cuando los miocitos cardíacos se estiran en sístole y en diástole (Yamamoto et al., La activación de diferentes vías de transducción de señales citoesqueléticas por el aumento del estrés sistólico y diastólico también puede explicar cómo la sobrecarga crónica de presión causa hipertrofia concéntrica, como ocurre cuando la estenosis aórtica aumenta el estrés sistólico, y cómo la sobrecarga de volumen causa hipertrofia excéntrica, como ocurre cuando la insuficiencia aórtica aumenta el estrés durante la diástole (Katz y Konstam, 2009).
Proteínas del citoesqueleto de los filamentos finos
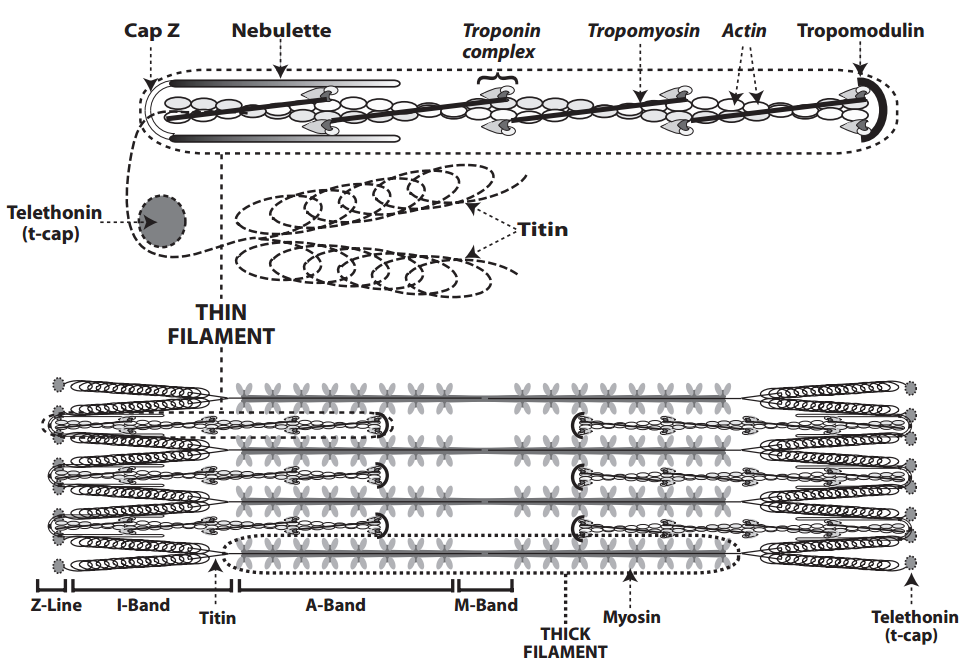
La actina puede considerarse tanto como parte del citoesqueleto como una proteína contráctil. Como la primera, a veces llamada actina cortical, la actina se encuentra en los microfilamentos (ver arriba), mientras que como actina sarcomérica esta proteína constituye la columna vertebral de los filamentos delgados. Dos proteínas del citoesqueleto recubren los extremos de los filamentos delgados; la tropomodulina, que se encuentra en los extremos que se interdigitan con las bandas A, y el casquillo Z (β-actinina), que ancla los otros extremos de los filamentos finos en las líneas Z (Fig. 2). Además de unir los filamentos finos a otras proteínas, la tropomodulina y la cap-Z regulan la longitud del filamento fino y participan en la señalización proliferativa. La nebuleta, una proteína del citoesqueleto que corre a lo largo de los filamentos delgados desde la línea Z hasta las bandas I, interactúa con una variedad de proteínas de señalización, la mayoría de las cuales se encuentran en las líneas Z.
Proteínas del citoesqueleto de las líneas Z
Las líneas Z (o discos Z) son estructuras rígidas en las que los filamentos delgados de los sarcómeros adyacentes se entretejen con una serie de proteínas del citoesqueleto que transmiten la tensión desarrollada por las proteínas contráctiles a las fascias adheridas de los discos intercalados que unen las células adyacentes (Fig. 3). Las líneas Z también anclan una serie de proteínas que están unidas a los filamentos del citoesqueleto que se conectan a la membrana plasmática, el retículo sarcoplásmico y otras estructuras celulares. Bandas rígidas formadas por desmina y α-actinina rodean las líneas Z en estructuras llamadas costameres que se asemejan a las varas de un barril. La desmina, la proteína principal de los costámeros, pertenece a una familia de proteínas de filamentos intermedios que incluye la vimentina, que apoya las células del tejido conectivo, las queratinas que se encuentran en las células epiteliales, los neurofilamentos que ayudan a organizar la estructura de los axones, la proteína ácida fibrilar glial en los astrocitos y otras células gliales, y las láminas que sostienen la superficie interna de las membranas nucleares. La desmina une las líneas Z a filamentos intermedios que se conectan a los desmosomas en el disco intercalado y, por lo tanto, participa en la transmisión de tensión entre los miocitos cardíacos adyacentes. Como la desmina carece de dominios de señalización, es probable que esta proteína no modifique directamente la señalización celular; Sin embargo, al transmitir la tensión a otras proteínas del citoesqueleto, la desmina puede desempeñar un papel indirecto en la transducción de señales.
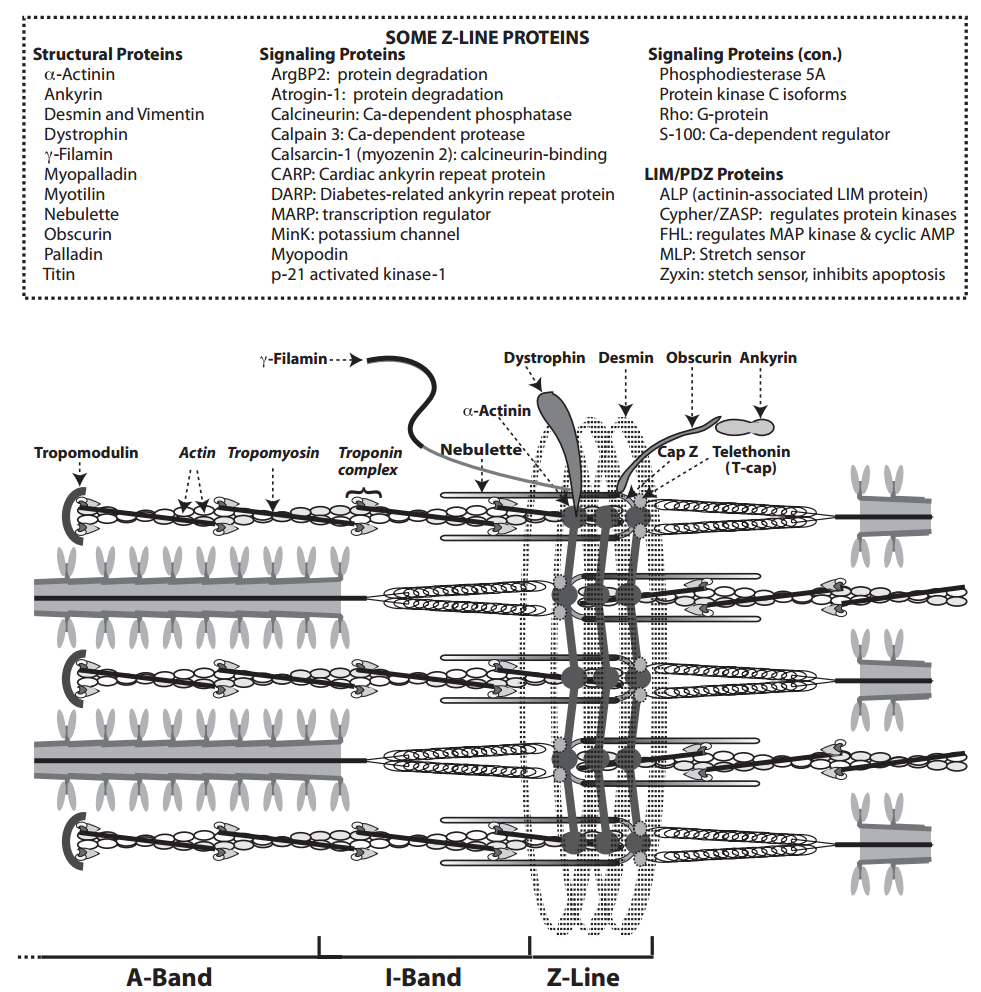
Las líneas Z están conectadas a la membrana plasmática por distrofina, -filamina, miotilina y microfilamentos de actina, mientras que la obscurina, en concierto con la pequeña anquirina-1, conecta las líneas Z con el retículo sarcoplásmico. Otras proteínas del citoesqueleto de la línea Z cuyas funciones son en gran medida estructurales incluyen la titina, la teletón, la gorra Z, la tropomodulina y la nebuleta. Las proteínas de la línea Z que cumplen funciones de señalización y estructurales incluyen varias proteínas LIM (ver más abajo) y el complejo paladin-miopaladina, que forma un andamio de señalización.
Las proteínas del citoesqueleto en la línea Z que participan en la señalización proliferativa incluyen proteínas quinasas, un supresor de tumores llamado miopodina, calcineurina, una proteína de unión a calcineurina llamada calsarcina (proteína sarcomérica asociada a la calcineurina) y S100, una proteína de unión al calcio que regula la miogénesis (Fig. 3). La degradación de proteínas está regulada por la proteína de unión a arginina 2 (ArgBP2), que se encuentra en los andamios de señalización intracelular, y la atrogina, un ligando de ubiquitina.
Las proteínas de repetición de anquirina muscular (MARP), que incluyen CARP (proteína de repetición de anquirina cardíaca) y DARP (proteína de repetición de anquirina relacionada con la diabetes), unen los elementos del citoesqueleto entre sí y conectan las células miocárdicas en los discos intercalados; Estas proteínas también regulan la transcripción de genes. MinK, una subunidad reguladora de un canal de potasio dependiente de voltaje de la membrana plasmática, une las líneas Z a los túbulos t y puede ayudar a integrar señales generadas por estiramiento mecánico y cambio de potencial eléctrico a través del plasma y las membranas tubulares t.
Las proteínas LIM/PDZ, una familia de proteínas del citoesqueleto que cumplen funciones estructurales y de señalización, contienen una o más secuencias de aminoácidos llamadas LIM (llamadas así por lin-11 y mec-3 que se encuentran en el gusano redondo C. elegans e Isl-1, una proteína de unión a insulina que se encuentra en ratas). Las proteínas LIM contienen un doble dedo de zinc y una secuencia rica en cisteína, y una secuencia llamada PDZ (llamada así por PSD-95/SAP90, una proteína postsináptica, Discs-large, una proteína de unión de Drosophila, y ZO-1, una proteína de unión estrecha). Además de sus funciones estructurales, algunas de las proteínas LIM/PDZ incorporadas en los módulos de proteínas asociados a la membrana proporcionan «andamios» para la señalización proliferativa. Las proteínas LIM/PDZ que se encuentran en la línea Z incluyen la proteína LIM asociada a la actinina (ALP), que se une a la -actinina y participa en las respuestas de crecimiento activadas por estiramiento, la LIM específica del músculo (mlp) y la zyxin, que proporcionan enlaces a la membrana plasmática y responden al estiramiento del sarcómero; Zyxin también puede inhibir la apoptosis. Otras proteínas LIM/PDZ de la línea Z son cypher/ZASP, una proteína enigma que regula las fosforilaciones de proteínas, y la proteína LIM de cuatro y medio (FHL) que regula las respuestas al AMP cíclico.
Proteínas del citoesqueleto asociadas a la membrana
Varias proteínas del citoesqueleto unen estructuras intracelulares a proteínas intrínsecas de la membrana plasmática (Fig. 4). Al igual que las asociadas con los sarcómeros, la mayoría de estas proteínas del citoesqueleto cumplen funciones estructurales y de señalización.
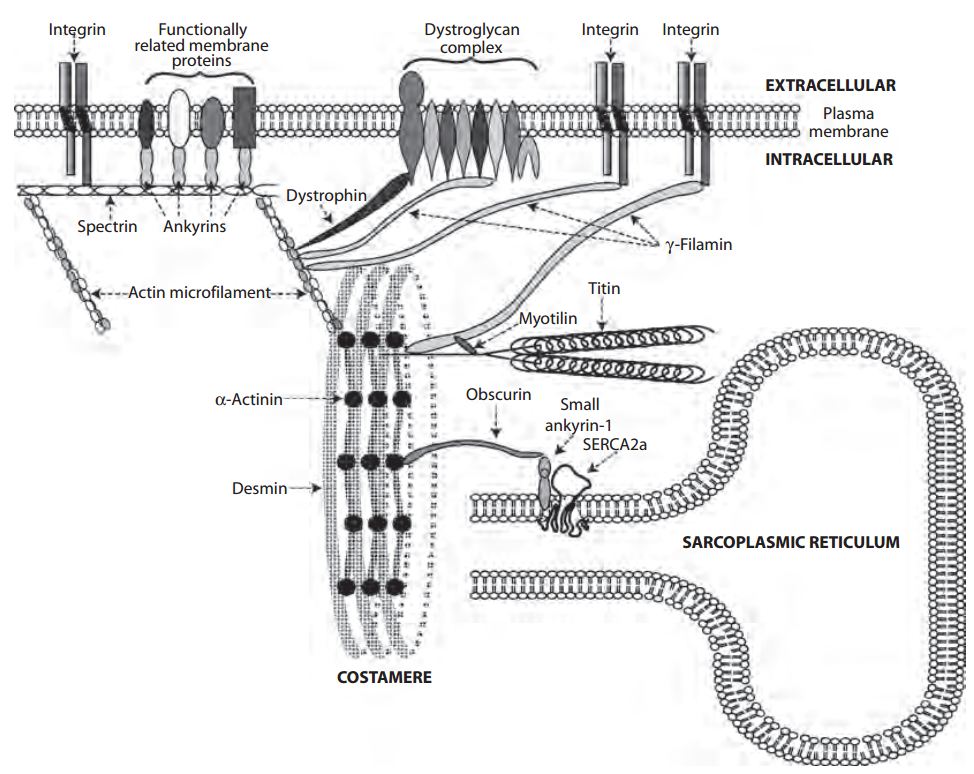
Anquirina
Las anquirinas, que contienen 24 copias de una secuencia de 33 aminoácidos llamada «repetición de anquirina», unen una variedad de proteínas de la membrana plasmática, incluidos receptores, moléculas de adhesión celular, canales iónicos, bombas de iones e intercambiadores de iones, con el citoesqueleto de actina/espectrina y entre sí. La pequeña anquirina-1, un miembro de esta familia, une el retículo sarcoplásmico con la osculina en las bandas M y las líneas Z. Las anquirinas contienen un dominio que se une a las proteínas de membrana, un dominio de unión a espectrina que se une al citoesqueleto de actina-espectrina, un dominio de muerte y un dominio C-terminal que se une a la oscuretina y cumple una variedad de funciones reguladoras. El dominio de unión a la membrana forma enlaces con una variedad de proteínas de membrana, a menudo en agregados multiproteicos que participan en la señalización proliferativa. El dominio de la muerte puede desempeñar un papel en la apoptosis.
Las anquirinas organizan e integran la función de la membrana mediante la creación de microdominios que acercan proteínas funcionalmente relacionadas entre sí. Por ejemplo, al colocalizar los canales de sodio dependientes de voltaje, la bomba de sodio ATPasa y el intercambiador de sodio/calcio, las anquirinas ayudan a coordinar los flujos de sodio a través de la membrana plasmática. Las anquirinas también organizan las interacciones entre los canales de calcio de la membrana plasmática («receptores de dihidropiridina») y los canales de liberación de calcio intracelular en el retículo sarcoplásmico («receptores de rianodina»).
Espectrina
Las espectrinas, que son proteínas tetrámeras formadas por 2 α-subunidades y 2 β-subunidades, forman una red en el lado citosólico de la membrana plasmática que está unida a microfilamentos de actina y anquirinas (Fig. 4). Los especrinas también participan en la señalización celular; algunos contienen un dominio de unión al calcio EF-hand, otros una secuencia de aminoácidos similar a la que se encuentra en las tirosina quinasas reguladoras. La compartimentación dentro del citoesqueleto de espectrina es en parte responsable de la organización mediada por anquirina de las proteínas de membrana descrita anteriormente.
Obscurina
La obscurina conecta la titina y la nebuleta en la línea Z, y la titina en la línea M, a la pequeña anquirina-1 que está unida al retículo sarcoplásmico (Fig. 4). Además de esta función estructural, la obscurina regula la formación de sarcómeros y participa en la transducción de señales, por ejemplo, a través de interacciones con la calmodulina y el Rho, una proteína G monomérica. El nombre de obscurina fue elegido debido al gran tamaño de esta proteína, su estructura compleja y las pequeñas cantidades que se encuentran en el músculo.
Filamina
La filamina une los microfilamentos de actina al complejo de sarcoglicanos en la membrana plasmática; su participación en la señalización celular se evidencia por interacciones con moléculas de adhesión focal y una proteína LIM llamada migfilina. γ-Filamina, la isoforma cardíaca, une las líneas Z a las integrinas y sarcoglicanos en la membrana plasmática.
Miotilina
La miotilina, que se une a la actina sarcomérica, la α-actinina y la γ-filamina en la línea Z, es una de las proteínas que unen el citoesqueleto a las integrinas de la membrana plasmática. Además de su papel estructural, la miotilina interactúa con las proteínas de señalización del citoesqueleto, incluida la calsarcina, un regulador de la calcineurina.
Proteínas del citoesqueleto en los discos intercalados
Los miocitos cardíacos están conectados entre sí por discos intercalados. Estas estructuras compuestas contienen uniones de brecha que permiten que la corriente eléctrica fluya a través del disco intercalado, y dos estructuras que proporcionan enlaces mecánicos entre los miocitos cardíacos adyacentes: los adherentes a la fascia (también llamados uniones adherentes o adherencias focales) y los desmosomas.
Fascia Adherens
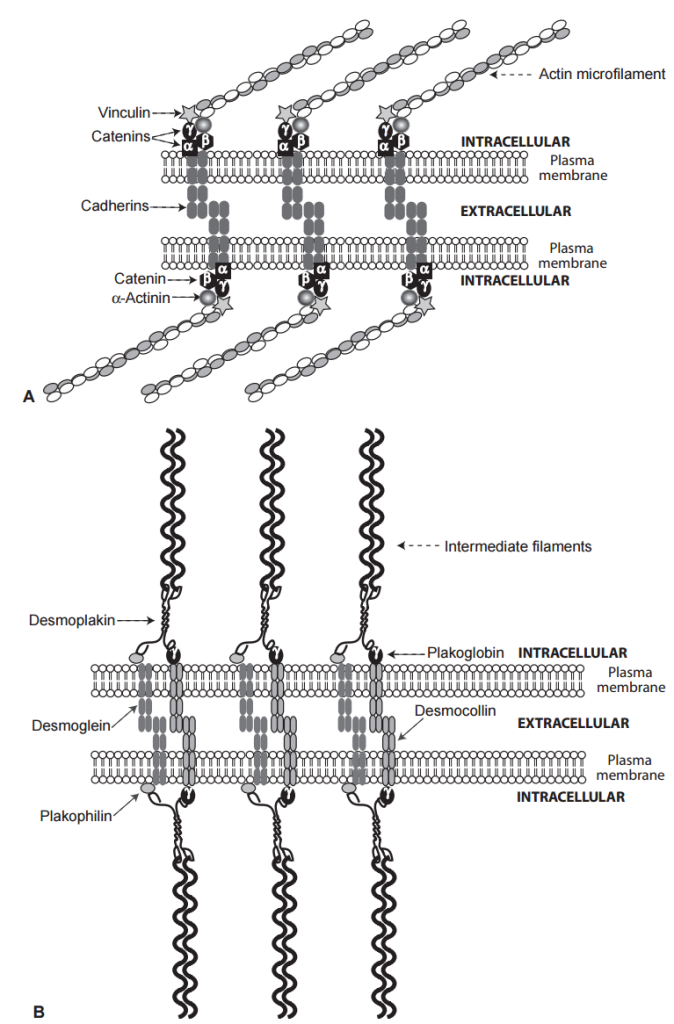
La fascia se adhiere a los microfilamentos de actina de las células adyacentes a través de conexiones entre miembros similares de una familia de proteínas, llamadas cadherinas, que se mantienen unidas por enlaces dependientes del calcio (Fig. 5A). Los complejos formados por α-, β- y γ-cateninas (esta última también se denomina plakoglobina) funcionan como proteínas de anclaje que unen los dominios intracelulares de las cadherinas en la fascia adherida a la α-actinina y vinculina, que conectan las fascias adheridas a los microfilamentos de actina. Las cateninas, que son miembros de una familia de proteínas de señalización llamadas Wnt, participan en las vías de señalización mediadas por proteínas G que desempeñan un papel importante en la hipertrofia cardíaca inducida por sobrecarga.
Desmosomas
Los desmosomas, que están unidos a filamentos intermedios, proporcionan conexiones fuertes, en forma de remache, entre las células. A diferencia de la fascia adherente, en la que las cadherinas de las células adyacentes son similares, dos cadherinas diferentes, llamadas desmogleína y desmocolina, forman una conexión heterotípica en los desmosomas (Fig. 5B). Las cadherinas de los desmosomas están unidas a la plakoglobina (γ-catenina) y a la placofilina, que son miembros de la familia de proteínas Wnt. Una proteína grande llamada desmoplaquina conecta este complejo multiproteico con la desmina en los filamentos intermedios.
Un síndrome clínico llamado miocardiopatía arritmogénica del ventrículo derecho, que puede ser causado por mutaciones en varios de los genes que codifican proteínas en el tracto de salida del ventrículo derecho, puede considerarse como una enfermedad de los desmosomas (Dokuparti et al., 2005).
Proteínas del citoesqueleto que unen las células a la matriz extracelular
Las proteínas del citoesqueleto descritas anteriormente difieren de las que unen las células a la matriz extracelular. Estos últimos incluyen el complejo de glicoproteína distrofina e integrinas, los cuales conectan microfilamentos de actina a proteínas de la matriz extracelular. La filamina, que también une los microfilamentos de actina a las proteínas de la membrana plasmática, interactúa con la titina y la miotilina en las líneas Z.
El complejo de glicoproteínas distrofinas
La membrana plasmática está anclada a las proteínas de la matriz extracelular por el complejo de glicoproteína distrofina, que está conectado a los microfilamentos de actina (Fig. 6). Los distroglicanos, que atraviesan la membrana plasmática y se unen a proteínas de la matriz extracelular como la laminina y la fibronectina, están conectados dentro del citosol con la distrobrevina y las sintrofinas en un agregado multiproteico que une la distrofina con la membrana plasmática. Dentro de este último, el distroglicano forma un complejo con una familia de glicoproteínas llamadas sarcoglicanos y al sarcospan.
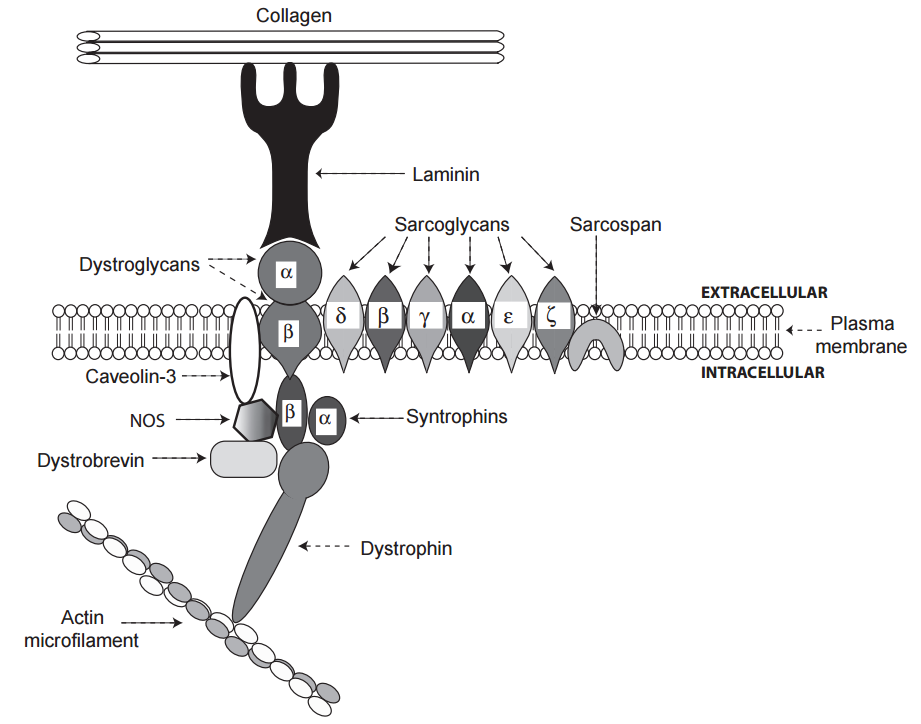
El distroglicano, junto con la distrofina, forma un complejo con la distrobrevina y las sintrofinas que participa en varios sistemas de señalización. La distrobrevina, un sustrato para las fosforilaciones reguladoras, contiene un dominio de unión al calcio y, junto con la caveolina-3, regula la producción de óxido nítrico por la óxido nítrico sintetasa (NOS). La caveolina-3, que, al igual que la anquirina, puede integrar las actividades de las moléculas de señalización funcionalmente relacionadas, interactúa con el distroglicano en el complejo de glicoproteína distrofina para mediar la transducción de señales a través de la membrana plasmática. Las mutaciones en la distrofina, el distroglicano y otras proteínas de este complejo pueden causar miocardiopatías dilatadas al desestabilizar las uniones célula-matriz, y las mutaciones en la distrobrevina se han implicado en la no compactación de la pared ventricular izquierda. La interrupción de los enlaces de la distrofina puede exacerbar la dilatación progresiva en los corazones que fallan.
Integrinas
Las integrinas, una familia de moléculas de adhesión celular que unen las células a la matriz extracelular, forman heterodímeros formados por diferentes subunidades de α y β cuyas propiedades determinan la especificidad de unión y los efectos de señalización de esta molécula de adhesión celular. Tanto las subunidades α como las β se unen a las proteínas de la matriz extracelular, pero solo las subunidades β se unen al citoesqueleto. Los dominios intracelulares de las integrinas se unen a los microfilamentos de actina a través de proteínas adaptadoras que incluyen -actinina, vinculina, tensina y talina; La paxilina, otra proteína intracelular que puede unirse a este complejo, es un sustrato para las fosforilaciones reguladoras que influyen en la adhesión celular. Las integrinas se unen a las proteínas de la matriz extracelular, como la fibronectina, la laminina y la vitronectina, que junto con los proteoglicanos, como el heparan, unen las integrinas al colágeno (Fig. 7A).

Además de su papel estructural, las integrinas participan en una variedad de vías de señalización proliferativa (Fig. 7B). Aunque las integrinas carecen de actividad enzimática, estas moléculas de adhesión celular permiten que las tensiones mecánicas regulen las vías de las proteínas quinasas activadas por mitógenos (MAP). Muchos de estos efectos proliferativos están mediados por pequeñas proteínas G como Rho, Ras y Ras, y por proteínas quinasas no receptoras que están unidas al citoesqueleto. Estos últimos incluyen las quinasas de tirosina quinasas asociadas a la adhesión focal (FAK), la tirosina quinasa 2 rica en prolina (PYK2) y la c-Src-quinasa (CSK), y las serina/treonina quinasas como la quinasa ligada a integrinas (ILK), la quinasa activada por p21 (PAK) y la proteína quinasa Cε (PKCε). Muchas de estas vías de señalización median respuestas de crecimiento desadaptativas que contribuyen al mal pronóstico en pacientes con insuficiencia cardíaca. Sin embargo, algunas proteínas de señalización ligadas a integrinas desempeñan un papel protector en los corazones sobrecargados; estos incluyen una vía vinculada a la melusina que, a través de interacciones con la proteína de dominio LIM muscular (MLP), puede atenuar la respuesta de crecimiento desadaptativa y reducir la apoptosis en corazones sobrecargados de presión.
Proteínas del núcleo del citoesqueleto
Los núcleos están rodeados por una envoltura que interactúa con el citoesqueleto para posicionar el núcleo dentro de las células eucariotas, controlar los movimientos de los cromosomas y participar en la división celular. La envoltura nuclear está formada por dos membranas: una membrana externa que es continua con la membrana del retículo endoplásmico y una membrana interna que es continua con la membrana externa en los poros nucleares. Los enlaces de tubulina, filamentos intermedios y microfilamentos de actina proporcionan soporte mecánico para el núcleo e inician una variedad de señales celulares en respuesta a tensiones mecánicas en la envoltura nuclear (Fig. 8).
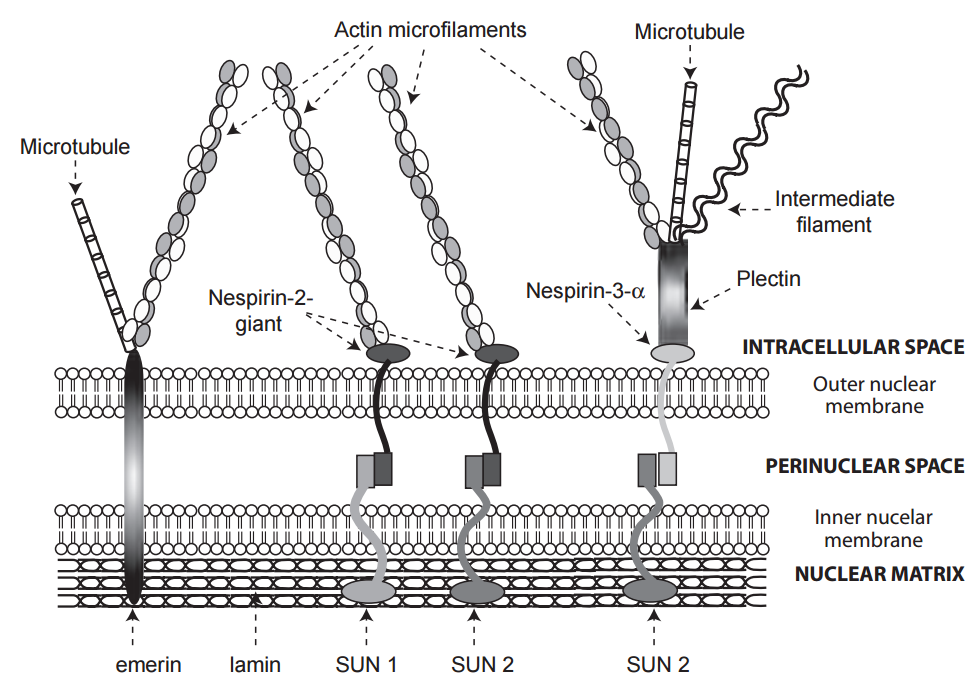
Varias proteínas de la envoltura nuclear interactúan con el citoesqueleto. Estos incluyen lamina, una proteína de filamento intermedio de clase V, que forma una malla debajo de la membrana interna dentro de la matriz nuclear. Las proteínas ligadas a la lamina conectadas al citoesqueleto incluyen la emerina, que se une tanto a los microtúbulos como a los microfilamentos de actina en el citosol. Las proteínas SUN (llamadas así por el gen de levadura Sad1 y el gen UNC-84 de C. elegans) ubicadas dentro de la membrana interna se conectan a nesprins que abarcan el espacio perinuclear; estos últimos, que se encuentran en ambas membranas nucleares, son miembros de una familia de proteínas KASH (homólogas a Klarsicht, ANC-1, Syne en Drosophila, C. elegans y humanos, respectivamente). Al igual que la emerina, las proteínas SUN y la emerina unen el citoesqueleto a la lamina. Las proteínas grandes que contienen una bobina helicoidal enrollada, llamadas plectinas, sirven como conectores que unen los tres tipos de filamento del citoesqueleto con las nesprinas y otras proteínas del citoesqueleto.
Resumen
La capacidad de la deformación del citoesqueleto para «detectar» las tensiones mecánicas en los miocitos cardíacos desempeña un papel importante en la determinación del tamaño, la forma y la composición del corazón. Este control local del tamaño, la forma y la composición de las células mediante la señalización del citoesqueleto es en gran parte responsable de la notable adaptación de la forma a la función en el corazón normal (Katz y Katz, 1989), cuya estructura permite que sus violentas contracciones impulsen la sangre a través de los ventrículos sin causar turbulencia; Esto explica por qué los soplos no se escuchan en individuos normales.
La activación de las respuestas proliferativas por deformación del citoesqueleto contribuye a la respuesta hipertrófica en corazones sobrecargados y desempeña un papel importante en la determinación de los diferentes fenotipos de hipertrofia observados en las enfermedades cardíacas (véase el capítulo 18). Entre las más conocidas de estas respuestas de crecimiento se encuentran la capacidad de sobrecarga crónica de presión en pacientes con estenosis aórtica e hipertensión sistémica para iniciar respuestas proliferativas que causan hipertrofia concéntrica, que normaliza el estrés de la pared, y la sobrecarga crónica de volumen para aumentar el volumen de la cámara iniciando hipertrofia excéntrica en pacientes con insuficiencia mitral y aórtica. Las respuestas específicas del citoesqueleto a las tensiones anormales causadas por las anomalías miofibrilares y de las proteínas del citoesqueleto también pueden explicar cómo las diferentes mutaciones que afectan a varias proteínas pueden causar miocardiopatías hipertróficas y dilatadas familiares.